2015四川高三下学期人教版高中化学月考试卷
| 1. | 详细信息 |
|
化学与生活密切相关,下列说法不正确的是() A. 人体内不含消化纤维素的消化酶,因此食物纤维对人体无用 B. 碳酸氢钠可用于治疗胃酸过多和焙制糕点 C. 油脂从化学成分上讲属于酯类化合物,是人类的主要营养物质之一 D. 维生素有20多种,它们多数在人体内不能合成,需要从食物中摄取
|
|
| 2. | 详细信息 |
|
下列实验所对应的离子方程式正确的是() A. 向NaAlO2溶液中通入少量CO2:AlO2﹣+CO2+2H2O═Al(OH)3↓+HCO3﹣ B. 向沸水中滴加饱和的氯化铁溶液:Fe3++3H2O═Fe(OH)3↓+3H+ C. 在碳酸氢钡溶液中加入过量的氢氧化钠溶液:Ba2++2HCO3﹣+2OH﹣═BaCO3↓+CO32﹣+2H2O D. 向FeCl2溶液中加入少量K3[Fe(CN)6]溶液:4Fe2++2[Fe(CN)6]4﹣═Fe4[Fe(CN)6]2↓
|
|
| 3. | 详细信息 |
|
设NA为阿伏加德罗常数的值,下列叙述正确的是() A. 60g SiO2中含有NA个SiO2分子 B. 标准状况下,2.24L NH3和CH4的混合气体,所含电子总数为2NA C. 1mol CO2与含1mol NaOH的溶液反应后,溶液中HCO3﹣数为NA D. 1mol C5H12分子中共价键总数为16NA
|
|
| 4. | 详细信息 |
|
下列操作会导致实验结果偏高的是() A. 中和热测定实验中,用铜制环形搅拌器代替环形玻璃搅拌棒,所测中和热的数值 B. 中和滴定测定盐酸浓度,量取20.00mL盐酸时未用待测液润洗酸式滴定管 C. 用托盘天平称量10.5g某物质,砝码和药品的位置放反,所称药品的质量 D. 配制一定物质的量浓度溶液时,用量筒量取浓溶液体积仰视读数,所配溶液的浓度
|
|
| 5. | 详细信息 |
|
短周期元素R、T、X、Y、Z在元素周期表的相对位置如表,它们的最外层电子数之和为24.则下列判断正确的是() R T X Y Z A. X位于元素周期表中第三周期第ⅥA族 B. Z元素的气态氢化物为极性分子 C. Y元素最高价氧化物对应水化物为强酸 D. 五种元素中原子半径最大的是R
|
|
| 6. | 详细信息 |
|
与图中相对应的叙述是()
A. 由图甲表示的反应速率随温度变化的关系可知该反应的△H>0 B. 图乙表示pH相同的盐酸与醋酸中分别加入水后溶液pH的变化,其中曲线a对应的是醋酸 C. 图丙表示该反应为放热反应,且催化剂能改变反应的焓变 D. 图丁表示向Na2CO3溶液中逐滴滴加稀盐酸,生成CO2与所加盐酸物质的量的关系
|
|
| 7. | 详细信息 |
|
化工生产中常用MnS作沉淀剂除去工业废水中的Cu2+:Cu2+(aq)+MnS(s)⇌CuS(s)+Mn2+(aq),下列说法错误的是() A. 相同条件下,MnS的Ksp比CuS的Ksp大 B. 该反应的平衡常数K= C. 该反应达到平衡时c(Mn2+)=c(Cu2+) D. 往平衡体系中加入少量CuSO4固体后,c(Mn2+)变大
|
|
| 8. | 详细信息 |
|
某配位化合物的水溶液为深蓝色,由原子序数依次增大的A、B、C、D、E五种元素组成,其原子个数比为l4:4:5:1:1.其中C、D元素同主族且原子序数D为C的二倍,E元素的外围电子排布为(n﹣1)d n+6nsl,回答下列问题. (1)元素D在周期表中的位置是 . (2)该配位化合物的化学式为 . (3)C元素可与A元素形成两种常见的化合物,其原子个数比分别为1:1和l:2,两种化合物可任意比互溶,解释其主要原因为 . (4)A元素与B元素可形成分子式为A2B2的某化合物,该化合物的分子具有平面结构,则其结构式为 . (5)已知E的晶胞结构如下图所示,则E的配位数 ;EDC4常作电镀液,其中DC42﹣的空间构型是 ,其中D原子的杂化轨道类型是 .
|
|
| 9. | 详细信息 |
|
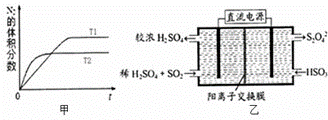
为有效控制雾霾,各地积极采取措施改善大气质量,研究并有效控制空气中的氮氧化物、碳氧化物和硫氧化物含量显得尤为重要. (1)汽车内燃机工作时会引起N2和O2的反应:N2+O2═2NO,是导致汽车尾气中含有NO的原因之一. ①在T1、T2温度下,一定量的NO发生分解反应时N2的体积分数随时间变化如图甲所示,根据图象判断反应N2(g)+O2(g)═2NO(g)的△H 0(填“>”或“<”). ②在T3温度下,向2L密闭容器中充入10mol N2与5mol O2,50秒后达到平衡,测得NO的物质的量为2mol,则该反应的速率v(N2)= .该温度下,若开始时向上述容器中充入N2与O2均为1mol,则达到平衡后N2的转化率为 . (2)利用如图乙所示装置(电极均为惰性电极)可吸收SO2,用阴极排出的溶液可吸收NO2. ①阳极的电极反应式为 . ②在碱性条件下,用阴极排出的溶液吸收NO2,使其转化为无害气体,同时有SO32﹣生成.该反应中氧化剂与还原剂的物质的量之比为 . (3)一定条件下可用甲醇与CO反应生成醋酸消除CO污染.常温下,将a mol•L﹣1的醋酸与b mol•L﹣1 Ba(OH)2溶液等体积混合,充分反应后,溶液中存在2c(Ba2+)═c(CH3COO﹣),则该混合溶液中醋酸的电离常数Ka= (用含a和b的代数式表示). (4)引起雾霾的PM2.5微细粒子包含(NH4)2SO4、NH4NO3、有机颗粒物及扬尘等,任写一种与SO42﹣互为等电子体的分子 .
|
|
| 10. | 详细信息 |
|
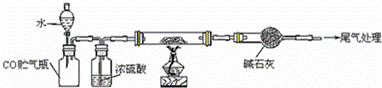
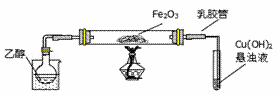
某研究性学习小组用下列装置(铁架台等支撑仪器略)探究氧化铁与乙醇的反应,并检验反应产物. (1)为快速得到乙醇气体,可采取的方法是 ; 若实验时小试管中的溶液已经开始发生倒吸,你采取的措施是 (填写编号); a.取下小试管 b.移去酒精灯 c.将导管从乳胶管中取下 d.以上都可以 (2)盛Cu(OH)2悬浊液的试管中可能出现的现象为 . (3)如图实验,观察到红色的Fe2O3全部变为黑色固体(M),充分反应后停止加热.为了检验M的组成,进行下列实验. ①M能被磁铁吸引;加入足量稀硫酸,振荡,固体全部溶解,未观察到有气体生成; ②经检验溶液中有Fe2+和Fe3+; 关于M 中铁元素价态的判断正确的是d(填写编号). a.一定有+3价和+2价铁,一定无0价铁 b.一定有+3价、+2价和0价铁 c.一定有+3价和0价铁,一定无+2价铁 d.一定有+3和+2价铁,可能有0价铁 (4)若M的成份可表达为FeXOY,用CO还原法定量测定其化学组成.称取a g M样品进行定量测定,实验装置和步骤如下:
①组装仪器;②点燃酒精灯;③加入试剂; ④打开分液漏斗活塞;⑤检查气密性;⑥停止加热;⑦关闭分液漏斗活塞;⑧….正确的操作顺序是 (填写编号) a.①⑤④③②⑥⑦⑧b.①③⑤④②⑦⑥⑧c.①⑤③④②⑥⑦⑧d.①③⑤②④⑥⑦⑧ (5)若实验中每步反应都进行完全,反应后M样品质量减小b g,则FexOy中
|
|
| 11. | 详细信息 |
|
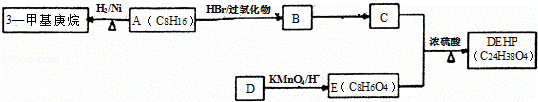
塑化剂又称增塑剂,是一种增加材料的柔软性或使材料液化的添加剂,不能用于食品、酒类等行业. 已知:① DEHP(C24H38O4)是增塑剂的一种,可通过下列流程制备,其中A的主链上有6个碳原子,D是对二甲苯的一种同分异构体,E的苯环上存在2种不同化学环境的氢原子.
(1)3﹣甲基庚烷的某同分异构体分子中只存在1种不同化学环境的氢原子,用系统命名法命名为 (2)写出B→C的化学反应方程式,请注明反应条件和反应类型. B→C: ;反应类型: ; (3)E的结构简式是 ;DEHP的结构简式是 ; (4)F是E的一种同分异构体,具有如下特征: a.是苯的邻位二取代物; b.遇FeCl3溶液呈紫色; c.能与碳酸氢钠溶液反应. 写出F分子中官能团的名称为 ; (5)G与E形成的混和物,只要物质的量一定,不论二者比例如何,燃烧耗氧是一定值.则满足条件的相对分子质量最小的G的分子式为 .
|
|