2018江苏高二上学期苏教版高中化学期末考试
| 1. | 详细信息 |
|
门捷列夫的突出贡献是( ) A. 提出原子学说 B. 提出分子学说 C. 发现元素周期律 D. 发现能量守恒定律
|
|
| 2. | 详细信息 |
|
近几年,国际上提出了“预防污染”这一概念,绿色化学是“预防污染”的根本手段。针对“吸烟”而言,下列活动属于实施绿色化学活动的是( ) A. 处理废弃物——烟灰、烟蒂 B. 治理污染点——通风,排除烟雾 C. 减少有毒物——使用过滤嘴、低焦油烟 D. 杜绝污染物——禁烟、戒烟
|
|
| 3. | 详细信息 |
|
核电是一种高效能源,也是一种高危能源。例如会泄露出 A. 131 B. 53 C. 25 D. 78
|
|
| 4. | 详细信息 |
|
下列各组中的两种微粒,互为同位素的是 A. H2O和H2O2 B. D2和T2 C. 12C和14C D. O2和O3
|
|
| 5. | 详细信息 |
|
以下能级符号不正确的是 ( ) A. 3s B. 3p C. 3d D. 3f
|
|
| 6. | 详细信息 |
|
下列分子的电子式书写正确的是 ( ) A. 氨 C. 氮
|
|
| 7. | 详细信息 |
|
下列各原子或离子的电子排列式错误的是 ( ) A. Na+ 1s22s22p6 B. F¯ 1s22s22p6 C. N3+ 1s22s22p6 D. O2¯ 1s22s22p6
|
|
| 8. | 详细信息 |
|
下列分子中含有“手性碳原子”的是( ) A. CBr2F2 B. CH3CH2CH2OH C. CH3CH2CH3 D. CH3CH(NO2)COOH
|
|
| 9. | 详细信息 |
|
下列关于氢原子电子云图的说法正确的是 ( ) A. 通常用小黑点来表示电子的多少,黑点密度大,电子数目大。 B. 黑点密度大,单位体积内电子出现的机会大。 C. 通常用小黑点来表示电子绕核作高速圆周运动。 D. 电子云图是对运动无规律性的描述。
|
|
| 10. | 详细信息 |
|
道尔顿的原子学说曾经起了很大作用。他的学说中,包含有下述三个论点:①原子是不能再分的粒子;②同种元素的原子的各种性质和质量都相同;③原子是微小的实心球体。从现代观点看,你认为这三个论点中不确切的( ) A. 只有③ B. 只有①③ C. 只有②③ D. 有①②③
|
|
| 11. | 详细信息 |
|
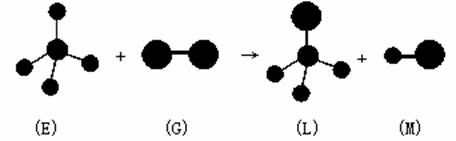
关于下列反应,说法正确的是:(图中共有三种原子)
A. 反应过程中E中共价键断裂,G中共价键保持不动 B. E中存在非极性键 C. M分子有可能是HCl D. 上述反应的类型是加成反应
|
|
| 12. | 详细信息 |
|
实验测得气态BeCl2为共价分子,两个Be—Cl键间的夹角为180°,由此可判断BeCl2属于( ) A. 由极性键形成的极性分子 B. 由极性键形成的非极性分子 C. 由非极性键形成的极性分子 D. 由非极性键形成的非极性分子
|
|
| 13. | 详细信息 |
|
下列轨道表示式能表示氮原子的最低能量状态的是 ( ) A. B. C. D.
|
|
| 14. | 详细信息 |
|
下列卤化氢分子中键长最短的是 ( ) A. HF B. HCl C. HBr D. HI
|
|
| 15. | 详细信息 |
|
下列说法不正确的是( ) A. 离子键没有方向性和饱和性 B. 并不是只有活泼的金属和非金属化合才形成离子键 C. 离子键的实质是静电作用 D. 静电作用只有引力
|
|
| 16. | 详细信息 |
|
某元素的原子最外电子层排布是5s25p1,该元素或其化合物不可能具有的性质是( ) A. 该元素单质是导体 B. 该元素单质在一定条件下能与盐酸反应 C. 该元素的氧化物的水合物显碱性 D. 该元素的最高化合价呈+5价
|
|
| 17. | 详细信息 |
|
下列说法中错误的是( ) A. SO2、SO3都是极性分子 B. 在NH C. 元素电负性越大的原子,吸引电子的能力越强 D. 原子晶体中原子以共价键结合,具有键能大、熔点高、硬度大的特征
|
|
| 18. | 详细信息 |
|
据某科学杂志报道,国外有一研究发现了一种新的球形分子,它的分子式为C60Si60,其分子结构好似中国传统工艺品“镂雕”,经测定其中包含C60,也有Si60结构。下列叙述正确的是( ) A. 该物质有很高的熔点、很大的硬度 B. 该物质形成的晶体属分子晶体 C. 该物质分子中Si60被包裹在C60里面 D. 该物质的摩尔质量为2400
|
|
| 19. | 详细信息 |
|
A、B、C、D、E是同一周期的五种主族元素,A和B的最高价氧化物对应的水化物均呈碱性,且碱性B>A,C和D的电负性C>D;E是这五种元素中原子半径最小的元素,则它们的原子序数由小到大的顺序是 A. A、B、C、D、E B. E、C、D、B、A C. B、A、D、C、E D. C、D、A、B、E
|
|
| 20. | 详细信息 |
|
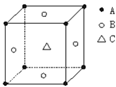
某物质的晶体中,含A、B、C三种元素,其排列方式如右图所示(其中前后两面心上的B原子不能画出),晶体中A、B、C的原子个数比依次为 ( )
A. 1:3:1 B. 2:3:1 C. 2:2:1 D. 1:3:3
|
|
| 21. | 详细信息 |
|
与Ne的核外电子排布相同的离子跟与Ar的核外电子排布相同的离子所形成的离子化合物是( ) A. MgBr2 B. Na2S C. KCl D. SO2
|
|
| 22. | 详细信息 |
|
氮化硼是一种新合成的结构材料,它是一种超硬、耐磨、耐高温的物质。下列各组物质熔化时所克服的微粒间作用力与氮化硼熔化所克服的微粒间的作用力相同的是( ) A. 硝酸钠和金刚石 B. 晶体硅和水晶 C. 冰和干冰 D. 苯和碘
|
|
| 23. | 详细信息 |
|
下列说法中正确的是( ) A. 冰融化时,分子中H—O键发生断裂 B. 原子晶体中,共价键越强,熔点越高 C. 分子晶体中,共价键键能越大,该分子晶体的熔、沸点一定越高 D. 分子晶体中,分子间作用力越大,该物质越稳定
|
|
| 24. | 详细信息 |
|
共价键、离子键和范德华力是粒子之间的三种作用力。下列晶体:①Na2O2、②SiO2、③石墨、④金刚石、⑤NaCl、⑥白磷中,含有两种作用力的是( ) A. ①②③ B. ①③⑥ C. ②④⑥ D. ①②③⑥
|
|
| 25. | 详细信息 |
|
用NA表示阿佛加德罗常数,下列说法正确的是 A. 22.4L H2的物质的量约为1mol B. 标准状况下,11.2L H2O的物质的量约为0.5 mol C. 1 L 1mol/L的MgCl2溶液中Cl-的物质的量浓度为 2mol/L D. 0.1mol铁与足量的盐酸完全反应,铁失去的电子数为0.3NA
|
|
| 26. | 详细信息 |
|
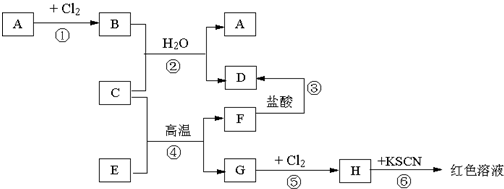
已知A~H是中学化学中的常见物质,A、C、G是金属,E、F是氧化物, B溶于水得蓝色溶液,E为红棕色粉末,它们有如下图所示的关系(反应中生成的水已略去)。
试回答下列问题。 (1)推断填写物质化学式:A是________ ,D是_________,E是_________,H是_________。 (2)F的类别是_________(选填“酸性氧化物”、“碱性氧化物”或“两性氧化物”)。 (3)反应④的化学方程式为___________________________________________。
|
|
| 27. | 详细信息 |
|
短周期主族元素A、B、C、D的原子序数依次增大,其中A、C同主族,B、C、D同周期,A原子的最外层电子数是次外层电子数的3倍,B是短周期元素中原子半径最大的主族元素。试回答下列问题: (1)A的元素符号___________;B的元素名称___________; (2)D的原子的电子式____________;C原子的电子排布式___________________。 (3)A、B、C三种元素形成的简单离子的半径由大到小的顺序是_____________。 (4)CA2与D元素的单质在水溶液中反应的化学方程式是_______________________。
|
|
| 28. | 详细信息 |
|
氰化钾是一种由剧毒的物质,贮存和使用时必须注意安全。已知:KCN+H2O2=KOCN+H2O,回答下列问题: (1)OCN-中所含三种元素的第一电离能从大到小的顺序为__________(用元素符号表示,下同),电负性从大到小的顺序为_______,基态氮原子外围电子排布式为______。 (2)H2O2中的共价键类型为__(填“σ键”或“π键”),其中氧原子的杂化轨道类型为______;分子中4个原子_______(填“在”或“不在”)同一条直线下;H2O2易溶于水除它们都是极性分子外,还因为____________________________________________________。 (3)与OCN-键合方式相同且互为等电子体的分子为______(任举一例);在与OCN-互为等电子体的微粒中,由一种元素组成的阴离子是_______。
|
|