2020еӣӣе·қй«ҳдёҖдёҠеӯҰжңҹдәәж•ҷзүҲ(2019)й«ҳдёӯеҢ–еӯҰжңҹжң«иҖғиҜ•
| 1. | иҜҰз»ҶдҝЎжҒҜ |
|
дёӢеҲ—еҗ„з»„еҲҶж•Јзі»пјҢйңҖз”ЁдёҒиҫҫе°”ж•Ҳеә”еҢәеҲҶзҡ„жҳҜ(гҖҖгҖҖ) AпјҺжә¶ж¶ІдёҺжөҠж¶ІВ В В В BпјҺиғ¶дҪ“дёҺиғ¶дҪ“ В В В В CпјҺжә¶ж¶ІдёҺиғ¶дҪ“ В В В В В DпјҺжә¶ж¶ІдёҺжә¶ж¶І
|
|
| 2. | иҜҰз»ҶдҝЎжҒҜ |
|
дёӢеҲ—е®һйӘҢеҹәжң¬ж“ҚдҪңжӯЈзЎ®зҡ„жҳҜ(гҖҖгҖҖ) AпјҺзЁҖйҮҠжө“зЎ«й…ёж—¶пјҢе°Ҷж°ҙжІҝеҷЁеЈҒзј“ж…ўжіЁе…Ҙжө“зЎ«й…ёдёӯ BпјҺиҝҮж»Өж—¶пјҢжјҸж–—йҮҢж¶ІдҪ“зҡ„ж¶ІйқўиҰҒй«ҳдәҺж»Өзәёзҡ„иҫ№зјҳ CпјҺиғ¶еӨҙж»ҙз®Ўзҡ„з®ЎеҸЈзӣҙжҺҘдјёе…ҘиҜ•з®ЎйҮҢж»ҙеҠ ж¶ІдҪ“пјҢд»Ҙе…ҚеӨ–жә… DпјҺе®һйӘҢе®ӨеҸ–з”Ёж¶ІдҪ“иҚҜе“ҒеҒҡе®һйӘҢж—¶пјҢеҰӮжІЎжңүиҜҙжҳҺз”ЁйҮҸпјҢдёҖиҲ¬еҸ–1пҪһ2 mL
|
|
| 3. | иҜҰз»ҶдҝЎжҒҜ |
|
дёӢеҲ—е…ідәҺзЎ…еҸҠе…¶еҢ–еҗҲзү©зҡ„иҜҙжі•дёӯпјҢжӯЈзЎ®зҡ„жҳҜ(гҖҖгҖҖ) в‘ зЎ…жҳҜжһ„жҲҗдёҖдәӣеІ©зҹіе’Ңзҹҝзү©зҡ„еҹәжң¬е…ғзҙ гҖҖв‘Ўж°ҙжіҘгҖҒзҺ»з’ғгҖҒж°ҙжҷ¶йҘ°зү©йғҪжҳҜзЎ…й…ёзӣҗеҲ¶е“ҒгҖҖв‘ўй«ҳзәҜеәҰзҡ„зЎ…еҚ•иҙЁе№ҝжіӣз”ЁдәҺеҲ¶дҪңе…үеҜјзәӨз»ҙгҖҖв‘Јйҷ¶з“·жҳҜдәәзұ»еә”з”ЁеҫҲж—©зҡ„зЎ…й…ёзӣҗжқҗж–ҷ AпјҺв‘ в‘Ў В В В В В BпјҺв‘Ўв‘ў В В В В В CпјҺв‘ в‘ЈВ В В В В DпјҺв‘ўв‘Ј
|
|
| 4. | иҜҰз»ҶдҝЎжҒҜ |
|
дёӢеҲ—е®һйӘҢж“ҚдҪңеқҮиҰҒз”ЁзҺ»з’ғжЈ’пјҢе…¶дёӯзҺ»з’ғжЈ’дҪңз”ЁзӣёеҗҢзҡ„жҳҜ(гҖҖгҖҖ) в‘ иҝҮж»ӨВ В В В В В в‘Ўи’ёеҸ‘В В В В В В в‘ўжә¶и§ЈВ В В В В В в‘Јеҗ‘е®№йҮҸ瓶дёӯиҪ¬з§»ж¶ІдҪ“ AпјҺв‘ е’Ңв‘ЎВ В В В В В В BпјҺв‘ е’Ңв‘ўВ В В В В В В CпјҺв‘ўе’Ңв‘ЈВ В В В В В В DпјҺв‘ е’Ңв‘Ј
|
|
| 5. | иҜҰз»ҶдҝЎжҒҜ |
|
йңҖиҰҒеҠ е…Ҙж°§еҢ–еүӮжүҚиғҪе®һзҺ°дёӢеҲ—еҸҚеә”зҡ„жҳҜ(гҖҖгҖҖ) AпјҺCl2вҶ’ClпјҚВ В В В В В В В В В В В В В В В BпјҺHпјӢвҶ’H2 CпјҺMnO2вҶ’Mn2пјӢ В В В В В В В В В В В В В В DпјҺZnвҶ’Zn2пјӢ
|
|
| 6. | иҜҰз»ҶдҝЎжҒҜ | ||||||||||||||||||||||||||||||
|
дёӢеҲ—зү©иҙЁзҡ„еҲҶзұ»жӯЈзЎ®зҡ„жҳҜ(гҖҖгҖҖ)
|
|||||||||||||||||||||||||||||||
| 7. | иҜҰз»ҶдҝЎжҒҜ |
|
дёӢеҲ—еҗ„з»„дёӯзҡ„зҰ»еӯҗиғҪеӨҹеӨ§йҮҸе…ұеӯҳдәҺеҗҢдёҖжә¶ж¶Ідёӯзҡ„жҳҜ(гҖҖгҖҖ) AпјҺCO CпјҺOHпјҚгҖҒNO
|
|
| 8. | иҜҰз»ҶдҝЎжҒҜ |
|
дёӢеҲ—еҢ–еӯҰеҸҚеә”дёӯпјҢдёҚеұһдәҺзҰ»еӯҗеҸҚеә”зҡ„жҳҜ(гҖҖгҖҖ) AпјҺеңЁж°ҙжә¶ж¶ІдёӯпјҡCH3COOHпјӢNH3В·H2O===CH3COONH4пјӢH2O BпјҺеңЁж°ҙжә¶ж¶ІдёӯпјҡCu(OH)2пјӢ2HNO3===Cu(NO3)2пјӢ2H2O CпјҺFe2O3пјӢ3CO DпјҺеңЁж°ҙжә¶ж¶ІдёӯпјҡCaSO4пјӢNa2CO3===CaCO3вҶ“пјӢNa2SO4
|
|
| 9. | иҜҰз»ҶдҝЎжҒҜ |
|
дёӢеҲ—зҰ»еӯҗж–№зЁӢејҸдёҚжӯЈзЎ®зҡ„жҳҜ(гҖҖгҖҖ) AпјҺNa2CO3жә¶ж¶ІдёҺи¶ійҮҸзӣҗй…ёеҸҚеә”пјҡCO BпјҺFeCl2жә¶ж¶Іе’ҢCl2еҸҚеә”пјҡ2Fe2пјӢпјӢCl2===2Fe3пјӢпјӢ2ClпјҚ CпјҺй’ дёҺж°ҙеҸҚеә”пјҡNaпјӢH2O===NaпјӢпјӢOHпјҚпјӢH2вҶ‘ DпјҺNaHCO3жә¶ж¶ІдёҺзЁҖзЎқй…ёеҸҚеә”пјҡHCO
|
|
| 10. | иҜҰз»ҶдҝЎжҒҜ |
|
з”ЁNAиЎЁзӨәйҳҝдјҸеҠ еҫ·зҪ—еёёж•°зҡ„еҖјпјҢдёӢеҲ—еҸҷиҝ°жӯЈзЎ®зҡ„жҳҜ(гҖҖгҖҖ) AпјҺж ҮеҮҶзҠ¶еҶөдёӢпјҢ22.4LH2Oеҗ«жңүзҡ„еҲҶеӯҗж•°дёәNA BпјҺж ҮеҮҶзҠ¶еҶөж—¶пјҢдҪ“з§ҜеқҮдёә22.4 Lзҡ„O2дёҺCO2еҗ«жңүзӣёеҗҢзҡ„еҲҶеӯҗж•° CпјҺйҖҡеёёзҠ¶еҶөдёӢпјҢNAдёӘN2еҲҶеӯҗеҚ жңүзҡ„дҪ“з§Ҝдёә22.4L DпјҺзү©иҙЁзҡ„йҮҸжө“еәҰдёә0.5mol/Lзҡ„MgCl2жә¶ж¶ІдёӯпјҢеҗ«жңүClпјҚдёӘж•°дёәNA
|
|
| 11. | иҜҰз»ҶдҝЎжҒҜ |
|
й…ҚеҲ¶дёҖе®ҡзү©иҙЁзҡ„йҮҸжө“жёЎзҡ„NaOHжә¶ж¶Іж—¶пјҢдҪҝжүҖй…ҚеҲ¶зҡ„жә¶ж¶Іжө“еәҰеҒҸе°Ҹзҡ„ж“ҚдҪңжҳҜ(гҖҖгҖҖ) в‘ е°ҶNaOHеӣәдҪ“ж”ҫеңЁзәёдёҠз§°йҮҸпјҢеҶҚиҪ¬з§»еҲ°зғ§жқҜдёӯжә¶и§Ј в‘Ўзғ§жқҜдёӯNaOHжә¶ж¶Із§»е…Ҙе®№йҮҸ瓶еҗҺжІЎжңүжҙ—ж¶Өзғ§жқҜ в‘ўе®һйӘҢз”Ёзҡ„е®№йҮҸ瓶жҙ—еҮҖеҗҺжңӘе№ІзҮҘпјҢйҮҢйқўеҗ«жңүе°‘йҮҸж°ҙ в‘Је®ҡе®№ж—¶иҜ»еҸ–е®№йҮҸ瓶液йқўйҮҮз”ЁдҝҜи§Ҷ AпјҺв‘ в‘ЎВ В В В В В В В BпјҺв‘ўв‘ЈВ В В В В В В CпјҺв‘ в‘ўВ В В В В В В DпјҺв‘Ўв‘Ј
|
|
| 12. | иҜҰз»ҶдҝЎжҒҜ |
|
й…ҚеҲ¶100 mL 0.2 mol/L NaClжә¶ж¶ІпјҢдёҚдјҡз”ЁеҲ°дёӢеҲ—д»ӘеҷЁдёӯзҡ„е“ӘдёҖз§Қ(гҖҖгҖҖ) AпјҺеҲҶж¶ІжјҸж–—В В В В В В В В В В В В В В В В В В BпјҺзғ§жқҜ CпјҺзҺ»з’ғжЈ’В В В В В В В В В В В В В В В В В В В В DпјҺе®№йҮҸ瓶
|
|
| 13. | иҜҰз»ҶдҝЎжҒҜ |
|
жҹҗжә¶ж¶Із»ҸеҲҶжһҗпјҢе…¶дёӯеҸӘеҗ«жңүNaпјӢгҖҒKпјӢгҖҒCa2пјӢгҖҒClпјҚгҖҒNO AпјҺ0.1 molВ·LпјҚ1В В В В В В В В В В В В В В В В В В В В В В В BпјҺ0.3 molВ·LпјҚ1 CпјҺ0.2 molВ·LпјҚ1В В В В В В В В В В В В В В В В В В В В В В В DпјҺ0.4 molВ·LпјҚ1
|
|
| 14. | иҜҰз»ҶдҝЎжҒҜ |
|
жҹҗжә¶ж¶Ідёӯеҗ«жңүиҫғеӨ§йҮҸзҡ„ClпјҚгҖҒCO в‘ ж»ҙеҠ Mg(NO3)2жә¶ж¶ІгҖҖв‘ЎиҝҮж»ӨгҖҖв‘ўж»ҙеҠ AgNO3жә¶ж¶ІгҖҖв‘Јж»ҙеҠ Ba(NO3)2жә¶ж¶І AпјҺв‘ в‘Ўв‘Јв‘Ўв‘ў В В В В В В В В В В В В В В BпјҺв‘Јв‘Ўв‘ в‘Ўв‘ў CпјҺв‘ в‘Ўв‘ўв‘Ўв‘Ј В В В В В В В В В В В В В В DпјҺв‘Јв‘Ўв‘ўв‘Ўв‘
|
|
| 15. | иҜҰз»ҶдҝЎжҒҜ |
|
жҸҗзәҜдёӢеҲ—зү©иҙЁйҷӨеҺ»е…¶дёӯзҡ„жқӮиҙЁ(жӢ¬еҸ·дёӯдёәжқӮиҙЁ)пјҢжүҖз”ЁиҜ•еүӮе’Ңж–№жі•дёҚжӯЈзЎ®зҡ„жҳҜ(гҖҖгҖҖ) AпјҺH2SO4(HCl)пјҡAgNO3жә¶ж¶ІгҖҒиҝҮж»Ө BпјҺKNO3(K2SO4)пјҡBa(NO3)2жә¶ж¶ІгҖҒиҝҮж»Ө CпјҺCu(CuO)пјҡзӣҗй…ёгҖҒиҝҮж»Ө DпјҺCaCO3(CaO)пјҡж°ҙгҖҒиҝҮж»Ө
|
|
| 16. | иҜҰз»ҶдҝЎжҒҜ |
|
дёӢеҲ—е®һйӘҢи§ӮеҜҹи®°еҪ•з»“и®әжңүиҜҜзҡ„жҳҜ(гҖҖгҖҖ) AпјҺж–°еҲ¶ж°Ҝж°ҙдёӯж»ҙеҠ зҙ«иүІзҹіи•Ҡжә¶ж¶Іе…ҲеҸҳзәўеҗҺиӨӘиүІ BпјҺй’ еңЁз©әж°”дёӯеҠ зғӯпјҢй’ еқ—е…ҲзҶ”жҲҗе…үдә®зҡ„银зҷҪиүІе°ҸзҗғеҗҺзҮғзғ§пјҢеҸ‘еҮәй»„иүІзҒ«з„° CпјҺз”ЁжҙҒеҮҖй“ӮдёқиҳёеҸ–жҹҗжә¶ж¶ІеңЁзҒ«з„°дёҠзҒјзғ§пјҢзҒ«з„°е‘Ҳй»„иүІпјҢжә¶ж¶ІдёӯжңүдёҖе®ҡNaпјӢж— KпјӢ DпјҺеңЁзӣӣNa2O2еӣәдҪ“зҡ„иҜ•з®Ўдёӯе…ҲеҗҺж»ҙе…Ҙж°ҙе’Ңй…ҡй…һжә¶ж¶ІпјҢжә¶ж¶ІжңҖз»Ҳе‘Ҳж— иүІ
|
|
| 17. | иҜҰз»ҶдҝЎжҒҜ | |||||||||||||||
|
дёӢеҲ—е®һйӘҢж“ҚдҪңжҲ–е®һйӘҢзҺ°иұЎдёҺйў„жңҹе®һйӘҢзӣ®зҡ„жҲ–жүҖеҫ—е®һйӘҢз»“и®әдёҖиҮҙзҡ„жҳҜ(гҖҖгҖҖ)
|
||||||||||||||||
| 18. | иҜҰз»ҶдҝЎжҒҜ |
|
е·ІзҹҘеёёжё©дёӢеңЁжә¶ж¶ІдёӯеҸҜеҸ‘з”ҹеҰӮдёӢдёӨдёӘзҰ»еӯҗеҸҚеә”пјҡ Ge4пјӢпјӢFe2пјӢ===Fe3пјӢпјӢGe3пјӢпјҢSn2пјӢпјӢ2Fe3пјӢ===2Fe2пјӢпјӢSn4пјӢ з”ұжӯӨеҸҜд»ҘзЎ®е®ҡFe2пјӢгҖҒGe3пјӢгҖҒSn2пјӢдёүз§ҚзҰ»еӯҗзҡ„иҝҳеҺҹжҖ§з”ұејәеҲ°ејұзҡ„йЎәеәҸжҳҜ(гҖҖгҖҖ) AпјҺSn2пјӢгҖҒFe2пјӢгҖҒGe3пјӢВ В В В В В В В В В В В BпјҺSn2пјӢгҖҒGe3пјӢгҖҒFe2пјӢ CпјҺGe3пјӢгҖҒFe2пјӢгҖҒSn2пјӢ В В В В В В В В В В В В DпјҺFe2пјӢгҖҒSn2пјӢгҖҒGe3пјӢ
|
|
| 19. | иҜҰз»ҶдҝЎжҒҜ |
|
жұүд»ЈеҷЁзү©дёҠзҡ„йўңж–ҷвҖңжұүзҙ«вҖқиҮід»Ҡе°ҡжІЎжңүеҸ‘зҺ°е…¶иҮӘ然еӯҳеңЁзҡ„и®°иҪҪгҖӮ20дё–зәӘ80е№ҙ代科еӯҰ家иҝӣиЎҢи¶…еҜјжқҗж–ҷз ”з©¶ж—¶пјҢеҒ¶з„¶еҸ‘зҺ°е…¶жҲҗеҲҶдёәзҙ«иүІзҡ„зЎ…й…ёй“ңй’Ў(еҢ–еӯҰејҸпјҡBaCuSi2OxпјҢCuдёә пјӢ2д»·)пјҢдёӢеҲ—жңүе…івҖңжұүзҙ«вҖқзҡ„иҜҙжі•дёӯдёҚжӯЈзЎ®зҡ„жҳҜ(гҖҖгҖҖ) AпјҺз”Ёзӣҗзҡ„еҪўејҸиЎЁзӨәпјҡBaSiO3В·CuSiO3В BпјҺз”Ёж°§еҢ–зү©еҪўејҸиЎЁзӨәпјҡBaOВ·CuOВ·2SiO2 CпјҺжҳ“жә¶дәҺејәй…ёгҖҒејәзўұВ В В В В В В В В В В В В В DпјҺжҖ§иҙЁзЁіе®ҡпјҢдёҚжҳ“иӨӘиүІ
|
|
| 20. | иҜҰз»ҶдҝЎжҒҜ |
|
иў«з§°дёәдёҮиғҪиҝҳеҺҹеүӮзҡ„NaBH4(NaBH4дёӯHдёәпјҚ1д»·)иғҪжә¶дәҺж°ҙ并е’Ңж°ҙеҸҚеә”пјҢNaBH4пјӢ2H2O===NaBO2пјӢ4H2вҶ‘пјҢдёӢеҲ—жңүе…іиҜҘеҸҚеә”зҡ„иҜҙжі•дёӯпјҢжӯЈзЎ®зҡ„жҳҜ(гҖҖгҖҖ) AпјҺNaBH4ж—ўжҳҜж°§еҢ–еүӮеҸҲжҳҜиҝҳеҺҹеүӮВ В В BпјҺNaBH4жҳҜж°§еҢ–еүӮпјҢH2OжҳҜиҝҳеҺҹеүӮ CпјҺзЎје…ғзҙ иў«ж°§еҢ–пјҢж°ўе…ғзҙ иў«иҝҳеҺҹВ В В DпјҺиў«ж°§еҢ–зҡ„е…ғзҙ дёҺиў«иҝҳеҺҹзҡ„е…ғзҙ иҙЁйҮҸжҜ”дёә1вҲ¶1
|
|
| 21. | иҜҰз»ҶдҝЎжҒҜ |
|
дёӢеҲ—жә¶ж¶ІдёӯClпјҚзҡ„зү©иҙЁзҡ„йҮҸжө“еәҰдёҺ50mL 1 mol/L AlCl3жә¶ж¶ІдёӯClпјҚзҡ„зү©иҙЁзҡ„йҮҸжө“еәҰзӣёзӯүзҡ„жҳҜ(гҖҖгҖҖ) AпјҺ75mL 1.5 mol/L MgCl2жә¶ж¶І В В В В В В BпјҺ150mL 2 mol/L KClжә¶ж¶І CпјҺ100mL 1 mol/L NaClжә¶ж¶ІВ В В В В В В В DпјҺ25mL 2 mol/L AlCl3жә¶ж¶І
|
|
| 22. | иҜҰз»ҶдҝЎжҒҜ | |||
|
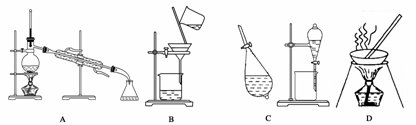
AгҖҒBгҖҒCгҖҒDжҳҜдёӯеӯҰеёёи§Ғзҡ„ж··еҗҲзү©еҲҶзҰ»жҲ–жҸҗзәҜзҡ„еҹәжң¬иЈ…зҪ®гҖӮ
иҜ·ж №жҚ®ж··еҗҲзү©еҲҶзҰ»жҲ–жҸҗзәҜзҡ„еҺҹзҗҶпјҢеӣһзӯ”еңЁдёӢеҲ—е®һйӘҢдёӯйңҖиҰҒдҪҝз”Ёе“Әз§ҚиЈ…зҪ®гҖӮе°ҶAгҖҒBгҖҒCгҖҒDеЎ«е…ҘйҖӮеҪ“зҡ„з©әж јдёӯгҖӮ (1)йҷӨеҺ»Ca(OH)2жә¶ж¶ІдёӯжӮ¬жө®CaCO3______________________________пјӣ (2)д»Һзўҳж°ҙдёӯжҸҗеҸ–зўҳ__________________________________________пјӣ (3)з”ЁиҮӘжқҘж°ҙеҲ¶еҸ–и’ёйҰҸж°ҙ___________________________________пјӣ (4)еҲҶзҰ»жӨҚзү©жІ№е’Ңж°ҙ_______________________________________пјӣ (5)йҷӨеҺ»зІ—зӣҗдёӯзҡ„жіҘжІҷ__________________________________________пјӣ (6)дёҺжө·ж°ҙжҷ’зӣҗеҺҹзҗҶзӣёз¬Ұзҡ„жҳҜ__________________________________________гҖӮ
|
||||
| 23. | иҜҰз»ҶдҝЎжҒҜ |
|
зҺ°жңүдёӢеҲ—дёғз§Қзү©иҙЁ:в‘ й“қгҖҖв‘Ўи”—зі–В В в‘ўCO2гҖҖв‘ЈH2SO4гҖҖв‘ӨBa(OH)2гҖҖ в‘ҘзәўиӨҗиүІзҡ„ж°ўж°§еҢ–й“Ғиғ¶дҪ“гҖҖв‘ҰHCl (1)дёҠиҝ°зү©иҙЁдёӯеұһдәҺз”өи§ЈиҙЁзҡ„жңү________гҖӮ(еЎ«еәҸеҸ·) (2)еҗ‘в‘Ҙзҡ„жә¶ж¶ІдёӯйҖҗжёҗж»ҙеҠ в‘Ұзҡ„жә¶ж¶І,зңӢеҲ°зҡ„зҺ°иұЎжҳҜВ В В В В В В В В В В В В В В В В В В В В В В гҖӮ (3) Ba(OH)2е’ҢHClеңЁж°ҙжә¶ж¶ІдёӯеҸ‘з”ҹеҸҚеә”,е…¶еҢ–еӯҰж–№зЁӢејҸдёә: 2HCl+Ba(OH)2====BaCl2+2H2O,еҲҷиҜҘеҸҚеә”зҡ„зҰ»еӯҗж–№зЁӢејҸдёә__________________________________________гҖӮ (4)в‘Ұзҡ„жө“жә¶ж¶ІдёҺй«ҳй”°й…ёй’ҫеҸ‘з”ҹеҸҚеә”зҡ„еҢ–еӯҰж–№зЁӢејҸдёә:2KMnO4+16HCl(жө“)==== 2MnCl2+2KCl+5Cl2вҶ‘+8H2O,иҜҘеҸҚеә”дёӯзҡ„ж°§еҢ–еүӮжҳҜ_______,ж°§еҢ–дә§зү©жҳҜВ В В В В В В гҖӮ
|
|
| 24. | иҜҰз»ҶдҝЎжҒҜ | |||
|
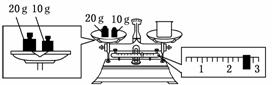
е®һйӘҢе®Өж¬Із”ЁNaOHеӣәдҪ“й…ҚеҲ¶1.0 molВ·LпјҚ1зҡ„NaOHжә¶ж¶І240 mLпјҡ (1)й…ҚеҲ¶жә¶ж¶Іж—¶пјҢдёҖиҲ¬еҸҜд»ҘеҲҶдёәд»ҘдёӢеҮ дёӘжӯҘйӘӨпјҡ в‘ з§°йҮҸгҖҖв‘Ўи®Ўз®—гҖҖв‘ўжә¶и§ЈгҖҖв‘Јж‘ҮеҢҖгҖҖв‘ӨиҪ¬з§»гҖҖв‘Ҙжҙ—ж¶Ө в‘Ұе®ҡе®№гҖҖ⑧еҶ·еҚҙгҖҖ е…¶жӯЈзЎ®зҡ„ж“ҚдҪңйЎәеәҸдёә_______гҖӮжң¬е®һйӘҢеҝ…йЎ»з”ЁеҲ°зҡ„д»ӘеҷЁжңүеӨ©е№ігҖҒиҚҜеҢҷгҖҒзҺ»з’ғжЈ’гҖҒзғ§жқҜгҖҒ_______гҖӮ (2)жҹҗеҗҢеӯҰж¬Із§°йҮҸNaOHзҡ„иҙЁйҮҸпјҢд»–е…Ҳз”ЁжүҳзӣҳеӨ©е№із§°йҮҸзғ§жқҜзҡ„иҙЁйҮҸпјҢеӨ©е№іе№іиЎЎеҗҺзҡ„зҠ¶жҖҒеҰӮеӣҫжүҖзӨәгҖӮзғ§жқҜзҡ„е®һйҷ…иҙЁйҮҸдёә______gпјҢиҰҒе®ҢжҲҗжң¬е®һйӘҢиҜҘеҗҢеӯҰеә”з§°еҮә______g NaOHгҖӮ
(3)дҪҝз”Ёе®№йҮҸ瓶еүҚеҝ…йЎ»иҝӣиЎҢзҡ„дёҖжӯҘж“ҚдҪңжҳҜ______гҖӮ (4)еңЁй…ҚеҲ¶иҝҮзЁӢдёӯпјҢе…¶д»–ж“ҚдҪңйғҪжҳҜжӯЈзЎ®зҡ„пјҢдёӢеҲ—ж“ҚдҪңдјҡеј•иө·иҜҜе·®еҒҸй«ҳзҡ„жҳҜ______гҖӮ AпјҺиҪ¬з§»жә¶ж¶Іж—¶дёҚж…Һжңүе°‘йҮҸжҙ’еҲ°е®№йҮҸ瓶еӨ–йқўВ В В В BпјҺе®ҡе®№ж—¶дҝҜи§ҶеҲ»еәҰзәҝ CпјҺжңӘеҶ·еҚҙеҲ°е®Өжё©е°ұе°Ҷжә¶ж¶ІиҪ¬з§»еҲ°е®№йҮҸ瓶并е®ҡе®№ DпјҺе®ҡе®№еҗҺеЎһдёҠ瓶еЎһеҸҚеӨҚеҖ’иҪ¬ж‘ҮеҢҖпјҢйқҷзҪ®еҗҺпјҢж¶ІйқўдҪҺдәҺеҲ»еәҰзәҝпјҢеҶҚеҠ ж°ҙиҮіеҲ»еәҰзәҝ
|
||||
| 25. | иҜҰз»ҶдҝЎжҒҜ |
|
е®һйӘҢе®ӨйҮҢеёёз”Ёжө“зӣҗй…ёдёҺдәҢж°§еҢ–й”°еҸҚеә”жқҘеҲ¶еҸ–е°‘йҮҸзҡ„ж°Ҝж°”пјҢеҸҚеә”зҡ„еҢ–еӯҰж–№зЁӢејҸ дёәпјҡMnO2пјӢ4HCl(жө“) иҜ·еӣһзӯ”дёӢеҲ—й—®йўҳпјҡ (1)еҶҷеҮәиҜҘеҸҚеә”зҡ„зҰ»еӯҗеҸҚеә”ж–№зЁӢејҸ_____________________________________гҖӮ (2)еҸӮеҠ еҸҚеә”зҡ„дәҢж°§еҢ–й”°зҡ„иҙЁйҮҸдёә____________гҖӮ (3)еҸҚеә”дёӯиў«ж°§еҢ–зҡ„HClзҡ„зү©иҙЁзҡ„йҮҸдёә ____________гҖӮ (4)е®һйӘҢе®ӨеӨҮз”Ёзҡ„жө“зӣҗй…ёиҙЁйҮҸеҲҶж•°дёә36.5%пјҢеҜҶеәҰдёә1.19 gВ·cmпјҚ3пјҢдёәдҪҝз”Ёж–№дҫҝпјҢиҜ·и®Ўз®—еҮәиҜҘжө“зӣҗй…ёзҡ„зү©иҙЁзҡ„йҮҸжө“еәҰ______________гҖӮ
|
|
| 26. | иҜҰз»ҶдҝЎжҒҜ | |||
|
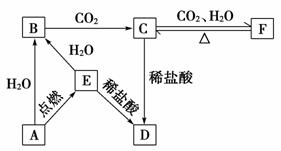
еҰӮеӣҫжүҖзӨәпјҢдёӢеҲ—еҗ„йЎ№еҸҳеҢ–зҡ„жңӘзҹҘзү©з„°иүІеҸҚеә”еқҮе‘Ҳй»„иүІпјҢEдёәж·Ўй»„иүІзІүжң«гҖӮ
еӣһзӯ”дёӢеҲ—й—®йўҳгҖӮ (1)еҶҷеҮәAвҶ’Bзҡ„еҢ–еӯҰж–№зЁӢејҸВ В В В В В В В В В В В В В В В В В В В В В В В В В В В В В В В В гҖӮ (2)еҶҷеҮәCвҶ’Dзҡ„зҰ»еӯҗж–№зЁӢејҸ__________________________________гҖӮ (3)еңЁBвҶ’Cзҡ„еҸҳеҢ–дёӯпјҢжүҖеҫ—Cзҡ„жә¶ж¶ІеҫҖеҫҖдёҚзәҜпјҢе…¶дёӯзҡ„жқӮиҙЁ(дёҚеҢ…жӢ¬ж°ҙ)еҸҜиғҪжҳҜ________________пјҢдё»иҰҒеҺҹеӣ жҳҜ_________________________________гҖӮ
|
||||
- 2018-2019е№ҙй«ҳдёҖеүҚеҚҠжңҹжңҹдёӯиҖғиҜ•еҢ–еӯҰиҖғйўҳеҗҢжӯҘи®ӯз»ғпјҲеҶ…и’ҷеҸӨиҮӘжІ»еҢәжӯЈй•¶зҷҪж——еҜҹжұ—ж·–дёӯеӯҰпјү
- йІҒ科зүҲйҖүжӢ©жҖ§еҝ…дҝ®1第2з« еҢ–еӯҰеҸҚеә”зҡ„ж–№еҗ‘гҖҒйҷҗеәҰдёҺйҖҹзҺҮ 第2иҠӮ еҢ–еӯҰеҸҚеә”зҡ„йҷҗеәҰ иҜҫж—¶1 еҢ–еӯҰе№іиЎЎеёёж•° е№іиЎЎиҪ¬еҢ–
- 2019-2020е№ҙй«ҳдәҢдёӢжңҹжңҹдёӯиҖғиҜ•еҢ–еӯҰиҜ•еҚ·пјҲжөҷжұҹзңҒе®ҒжіўеёӮеҢ—д»‘дёӯеӯҰпјү
- еӣӣе·қзңҒжҲҗйғҪеёӮз®ҖйҳіеёӮйҳіе®үдёӯеӯҰ2020-2021е№ҙй«ҳдёҖдёҠеҶҢжңҹдёӯиҖғиҜ•еҢ–еӯҰиҜ•еҚ·еңЁзәҝз»ғд№
- йҷ•иҘҝзңҒжҰҶжһ—еёӮ第еҚҒдәҢдёӯеӯҰ2021еұҠй«ҳдёүдёҠеҚҠе№ҙ第дёүж¬ЎжңҲиҖғеҢ–еӯҰиҜ•еҚ·еңЁзәҝз»ғд№
- йҷҶиүҜеҺҝ第八дёӯеӯҰй«ҳдәҢеҢ–еӯҰдёҠеҶҢжңҹжң«иҖғиҜ•йўҳеёҰзӯ”жЎҲе’Ңи§Јжһҗ
- й»„йҷөдёӯеӯҰ2018е№ҙй«ҳдәҢеҢ–еӯҰдёҠеҶҢжңҹдёӯиҖғиҜ•еёҰеҸӮиҖғзӯ”жЎҲдёҺи§Јжһҗ
- й«ҳдёҖдёҠеҶҢжңҹжң«иҖғиҜ•еҢ–еӯҰдё“йўҳи®ӯз»ғпјҲ2019-2020е№ҙеұұдёңзңҒж»•е·һеёӮ第дёҖдёӯеӯҰпјү