2019高一上学期人教版(2019)高中化学月考试卷
| 1. | 详细信息 |
|
8月12日天津港危险品仓库发生的爆炸事故,再次警示人们化学试剂一定要安全存放。下列在实验室中关于试剂存放叙述正确的是( ) A. 白磷不易挥发,不需要密闭存放 B. 氢氧化钠溶液应保存在带玻璃塞的细口试剂瓶中 C. 氰化物的包装标签上应贴上如图所示的标志 D. 在量筒内稀释浓硫酸后,倒入试剂瓶并贴上浓度标签
|
|
| 2. | 详细信息 |
|
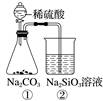
某同学用如图所示的装置及药品进行酸性强弱比较的实验,下列说法不正确的是( )
A. ①和②中发生的反应均为复分解反应 B. 向Na2SiO3饱和溶液中滴酚酞溶液无明显现象 C. 一段时间后②中有胶冻状物质生成 D. 该实验能证明酸性强弱的顺序:硫酸>碳酸>硅酸
|
|
| 3. | 详细信息 |
|
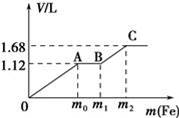
向300 mL 1 mol·L-1的稀硝酸中,加入5.6 g铁粉,充分反应后,铁粉全部溶解(假设还原产物只有NO),下列说法不正确的是( ) A. 最终所得溶液中既有Fe2+又有Fe3+ B. 最终溶液中,硝酸无剩余 C. 标准状况下生成NO的体积为1.68 L D. 再向最终所得溶液中滴加稀硝酸,无明显变化
|
|
| 4. | 详细信息 |
|
在隔绝空气的情况下,9.2 g铁、镁、铝混合物溶解在一定量某浓度的稀硝酸中,当金属完全溶解后收集到4.48 L(标准状况下)NO气体。在反应后的溶液中加入足量的烧碱溶液,可生成氢氧化物沉淀的质量为( ) A. 18.6 g B. 20 g C. 19.4 g D. 24 g
|
|
| 5. | 详细信息 |
|
下列做法会对人体健康造成较大危害的是( ) A. 用大量SO2漂白馒头 B. 用小苏打 C. 用食醋清洗热水瓶胆内壁附着的水垢 D. 用消毒液(有效成分
|
|
| 6. | 详细信息 |
|
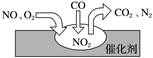
随着我国汽车年销量的大幅增加,空气环境受到了很大的污染。汽车尾气装置里,气体在催化剂表面吸附与解吸作用的过程如图所示,下列说法正确的是( )
A. 反应中NO为氧化剂,N2为氧化产物 B. 汽车尾气的主要污染成分包括CO、NO和N2 C. NO和O2必须在催化剂表面才能反应 D. 催化转化总化学方程式为2NO+O2+4CO4CO2+N2
|
|
| 7. | 详细信息 |
|
某铁的氧化物(FexO)1.52 g溶于足量盐酸中,向所得溶液中通入标准状况下112 mL Cl2,恰好将Fe2+完全氧化。下列说法正确的是( ) A. FexO溶于足量盐酸后只生成了FeCl3和H2O B. 标准状况下112 mL Cl2的物质的量是5 mol C.x=0.8 D. 通入Cl2后,发生反应的离子方程式:Fe2++Cl2
|
|
| 8. | 详细信息 |
|
下列说法不正确的是( ) ①钠、氢气都能在氯气中燃烧生成白色烟雾 ②铜丝在氯气中燃烧,生成蓝绿色的氯化铜 ③液氯就是氯气的水溶液,它能使干燥的有色布条褪色 ④久置的氯水,因氯气几乎完全挥发掉,剩下的就是水 A. ① B. ①和② C. ①和④ D. ①②③④
|
|
| 9. | 详细信息 |
|
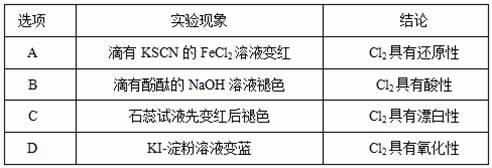
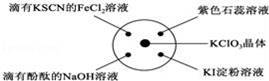
已知:KClO3+6HCl(浓)
A. A B. B C. C D. D
|
|
| 10. | 详细信息 |
|
在探究新制饱和氯水成分的实验中,下列根据实验现象得出的结论不正确的是( ) A. 氯水的颜色呈浅黄绿色,说明氯水中含有Cl2 B. 向氯水中滴加硝酸酸化的AgNO3溶液,产生白色沉淀,说明氯水中含有Cl﹣ C. 向氯水中加入NaHCO3粉末,有气泡产生,说明氯水中含有H+ D. 向FeCl2溶液中滴加氯水,溶液颜色变成棕黄色,说明氯水中含有HClO
|
|
| 11. | 详细信息 |
|
已知金属钠的活泼性非常强,甚至在常温时能和水发生反应2Na+2H2O===2NaOH+H2↑。现将9.2克钠、7.2克镁、8.1克铝分别放入100克10.95%的盐酸中,同温同压下产生气体的质量比是( ) A. 1∶2∶3 B. 4∶3∶3 C. 8∶6∶9 D. 1∶1∶1
|
|
| 12. | 详细信息 |
|
在FeCl3、CuCl2、FeCl2的混合溶液中,Fe3+、Cu2+和Fe2+的物质的量之比为3∶2∶1,现加入适量铁粉,使溶液中三种离子物质的量浓度之比变化为1∶2∶4,则参加反应的铁粉与原溶液Fe3+的物质的量之比为( ) A. 2∶1 B. 1∶2 C. 1∶3 D. 1∶4
|
|
| 13. | 详细信息 |
|
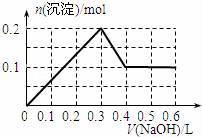
向100 mL 1.0 mol•L﹣1的AlCl3溶液中逐滴加入0.5 mol•L﹣1的NaOH溶液至过量,生成沉淀的物质的量与加入NaOH的量的理论曲线图正确的是( ) A. . C. .
|
|
| 14. | 详细信息 |
|
下列有关钠的化合物说法正确的是( ) A. 将NaOH浓溶液滴加到饱和FeCl3溶液中制备Fe(OH)3胶体 B. 用加热法除去NaHCO3固体中混有的Na2CO3 C. 灼烧白色粉末,火焰呈黄色,证明原粉末中有Na+,一定没有K+ D. Na2O2可用于呼吸面具中氧气的来源
|
|
| 15. | 详细信息 |
|
下列关于金属钠性质的叙述中,正确的是( ) A. 钠是密度小、硬度大、熔点高的银白色金属 B. 钠在纯净的氧气中充分燃烧,生成白色固体Na2O C. 将金属钠放入CuSO4溶液中,可观察到大量红色的铜析出 D. 将金属钠放入水中立即熔化成小球,说明金属钠熔点低,且反应放出热量
|
|
| 16. | 详细信息 |
|
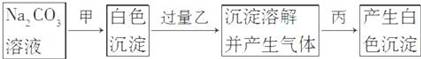
有甲、乙、丙三种溶液,进行如下操作:
则甲、乙、丙三种溶液可能是( ) A. BaCl2、H2SO4、MgCl2 B. CaCl2、HNO3、BaCl2 C. CaCl2、HNO3、NaCl D. BaCl2、HCl、Na2SO4
|
|
| 17. | 详细信息 |
|
用NA代表阿伏加德罗常数,下列说法中正确的是( ) A. 1 mol H2含有的分子数目为2NA B. 0.5 mol H2SO4所含的原子总数目为0.5NA C. 1 mol O3含有的氧原子数为2NA D. 0.5 mol H2O含有NA个氢原子和0.5NA个氧原子
|
|
| 18. | 详细信息 |
|
下列实验操作正确的是( ) A. 当某实验没有明确的药品用量说明时,为看到明显现象,取用药品越多越好 B. 取用细口瓶里的试液时,先拿下瓶塞,倒放在桌面上,然后标签朝外拿起瓶子,瓶口要紧挨着试管口,使液体缓缓地倒入试管 C. 胶头滴管量取完一种试液后,可直接量取另一种不与其反应的试液 D. 取用粉末状固体或固体小颗粒时,应用药匙或纸槽,取用块状固体时,应用镊子夹取
|
|
| 19. | 详细信息 |
|
下列实验操作与安全事故的处理中错误的是( ) A. 使用水银温度计测量烧杯中水浴温度时,不慎打破水银球,用滴管将水银吸出放入水封的小瓶中,残破的温度计插入装有硫粉的广口瓶中 B. 用试管夹从试管底部由下往上夹住距试管口约 C. 点燃酒精灯前一定要将酒精添满 D. 把玻璃管插入橡皮塞口时,用厚布护手,紧握用水湿润的玻璃管插入端,缓慢旋进孔中
|
|
| 20. | 详细信息 |
|
如图所示装置进行实验,将液体A逐滴加入到固体B中,下列叙述中不正确的是( )
A. 若A为醋酸,B为贝壳(粉状),C为澄清石灰水溶液,则C中溶液变浑浊 B. 若A为浓盐酸,B为锌粒,C中盛滴有酚酞的NaOH溶液,则C中溶液褪色 C. 若A为双氧水,B为MnO2,C中为NaOH溶液,D为防倒吸装置 D. 实验中仪器D可起到防倒吸的作用
|
|
| 21. | 详细信息 |
|
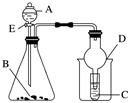
已知氨气、氯化氢极易溶于水。实验室用下图所示装置干燥收集气体R,并吸收多余尾气,则R是( )
A. CH4 B. HCl C. CO D. NH3
|
|
| 22. | 详细信息 |
|
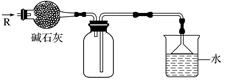
现有一瓶甲和乙的混合物,已知甲和乙的某些性质如下表:
据此,将甲和乙互相分离的最佳方法是( ) A. 萃取法 B. 升华法 C. 蒸馏法 D. 分液法
|
|
| 23. | 详细信息 |
|
海藻中含有丰富的碘元素。如图是实验室从海藻里提取碘的流程的一部分。下列判断正确的是( )
A. 步骤④的操作是过滤 B. 可用淀粉溶液检验步骤②的反应是否进行完全 C. 步骤①、③的操作分别是过滤、萃取 D. 步骤③中加入的有机溶剂可能是酒精或四氯化碳
|
|
| 24. | 详细信息 |
|
向50 mL稀H2SO4与稀HNO3的混合溶液中逐渐加入铁粉,假设加入铁粉的质量与产生气体的体积(标准状况)之间的关系如图所示,且每一段只对应一个反应。下列说法正确的是( )
A. 开始时产生的气体为H2 B. AB段发生的反应为置换反应 C. 所用混合溶液中c(HNO3)=0.5 mol•L﹣1 D. 参加反应铁粉的总质量m2=5.6 g
|
|
| 25. | 详细信息 |
|
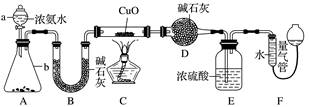
某课外活动小组欲利用CuO与NH3反应,研究NH3的某种性质并测定其组成,设计了如下实验装置(夹持装置未画出)进行实验。请回答下列问题: (1)仪器a的名称为 ;仪器b中可选择的试剂为 。 (2)实验室中,利用装置A,还可制取的无色气体是 (填字母)。 A.Cl2B.O2C.CO2D.NO2 (3)实验中观察到装置C中黑色CuO粉末变为红色固体,量气管有无色无味的气体,上述现象证明NH3具有 性,写出相应的化学方程式 。 (4)E装置中浓硫酸的作用 。 (5)读取气体体积前,应对装置F进行的操作: 。 (6)实验完毕,若测得干燥管D增重mg,装置F测得气体的体积为nL(已折算成标准状况),则氨分子中氮、氢的原子个数比为 (用含m、n字母的代数式表示)。
|
|
| 26. | 详细信息 |
|
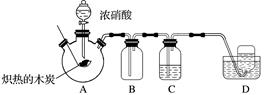
某化学小组采用如图所示装置,对浓硝酸与木炭的反应进行探究(已知:4HNO34NO2↑+O2↑+2H2O)。
请回答下列问题: (1)检查装置气密性后,将燃烧匙中的木炭在酒精灯上加热至红热状态,伸入三口烧瓶中,并塞紧瓶塞,滴加浓硝酸,可观察到三口烧瓶中气体的颜色为________,产生该气体的化学方程式是________________________________________________________________________。 (2)装置C中盛有足量Ba(OH)2溶液,炽热的木炭与浓硝酸反应后可观察到C中出现白色沉淀,该白色沉淀为____________(填化学式)。 (3)装置B的作用是________________________________________________________。 (4)装置D中收集到了无色气体,部分同学认为是NO,还有部分同学认为是O2。 ①下列对该气体的检验方法合适的是________。 A.敞口观察装置D中集气瓶内气体的颜色变化 B.将湿润的蓝色石蕊试纸伸入集气瓶内,观察蓝色石蕊试纸是否变红 C.将带火星的木条伸入集气瓶中,观察木条是否复燃 ②如果D中集气瓶中收集的无色气体是氧气,则氧气的来源是________________。
|
|
| 27. | 详细信息 |
|
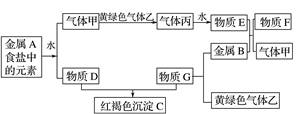
现有金属单质A、B和气体甲、乙、丙及物质C、D、E、F、G,它们之间能发生如图反应(图中有些反应的产物和反应的条件没有全部标出)。
请根据以上信息回答下列问题: (1)写出下列物质的化学式:乙 ,F 。 (2)写出下列反应的离子方程式: ①金属A和水反应 。 ②红褐色沉淀C与物质E反应 。 ③F与黄绿色气体乙反应 。 ④实验室常用氢氧化钠吸收实验过程中的黄绿色气体乙,写出用氢氧化钠溶液吸收该气体的离子方程式 。 (3)将G溶液逐滴加入到沸水中会产生一种红褐色的液体。你认为该液体中的分散质粒子直径在 之间,验证的简单方法是: 。
|
|
| 28. | 详细信息 |
|
某课外活动小组进行Fe(OH)3胶体的制备实验并检验其性质。 (1)若将饱和FeCl3溶液分别滴入下列物质中,能形成胶体的是________(填字母)。 A.冷水 B.沸水 C.NaOH浓溶液 D.NaCl浓溶液 (2)现有甲、乙、丙三名同学进行Fe(OH)3胶体的制备: ①甲同学的操作:取一小烧杯,加入25 mL蒸馏水加热至沸腾,向沸水中逐滴加入1~2 mL FeCl3饱和溶液,继续煮沸至混合液呈红褐色,停止加热。 请评价该操作是否正确______。 ②乙直接加热饱和FeCl3溶液,请评价是否正确______。 ③丙向沸水中滴加饱和FeCl3溶液,为了使反应进行充分,煮沸10分钟,请评价是否正确________。 (3)写出制备Fe(OH)3胶体的化学方程式:___________________________________________ ________________________________________________________________________。 证明有Fe(OH)3胶体生成的实验操作是_____________________________________________ ________________________________________________________________________。 该操作利用胶体的性质是________。 (4)Fe(OH)3胶体稳定存在的主要原因是_____________________________________(填字母,下同)。 A.胶体粒子直径小于1 nm B.胶体粒子带正电荷 C.胶体粒子作布朗运动 D.胶体粒子能透过滤纸 (5)Fe(OH)3胶体区别于FeCl3溶液最本质的特征是________。 A.Fe(OH)3胶体粒子的直径在1~100 nm之间 B.Fe(OH)3胶体具有丁达尔效应 C.Fe(OH)3胶体是均一的分散系 D.Fe(OH)3胶体的分散质能透过滤纸 (6)若取少量制得的胶体加入试管中,加入硫酸铵溶液,现象是_________________________, 这种现象称为胶体的________。
|
|


 B
B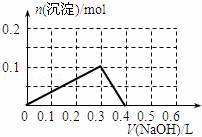
 D
D