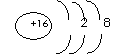高一上学期人教版高中化学月考试卷
| 1. | 详细信息 |
|
A.质量数是60 B.质子数是60 C.中子数是33 D.电子数是27
|
|
| 2. | 详细信息 |
|
下列说法正确的是 A.需要加热的化学反应都是吸热反应 B.中和反应都是放热反应 C.原电池是将电能转化为化学能的一种装置 D.水力发电是将化学能转化为电能的过程
|
|
| 3. | 详细信息 |
|
氢氧燃料电池已用于航天飞机。以30%KOH溶液为电解质溶液的这种电池在使用时的电极反应如下: 2H2 + 4OH- - 4e- = 4H2O,O2 + 2H2O + 4e- = 4OH- 据此作出判断,下列说法中错误的是 A.H2在负极发生氧化反应 B.供电时的总反应为:2H2 + O2 = 2H2O C.产物为无污染的水,属于环境友好电池 D.燃料电池的能量转化率可达100%
|
|
| 4. | 详细信息 |
|
下列实验中,反应速率加快是由催化剂引起的是 A.将炭块粉碎成粉末状,可使燃烧更加充分 B.过氧化氢中加入几滴氯化铁溶液,即可较快放出气体 C.在炭粉中加入氯酸钾,点燃时燃烧更为剧烈 D.用锌与稀硫酸反应制备氢气时,加入少量浓硫酸加快反应
|
|
| 5. | 详细信息 |
|
下列有关化学用语使用正确的是
C.一氯乙烷的结构式CH3Cl D.原子核内有10个中子的氧原子:
|
|
| 6. | 详细信息 |
|
元素周期表中某区域的一些元素多用于制造半导体材料,它们是 A.左、下方区域的金属元素 B.金属元素和非金属分界线附近的元素 C.右、上方区域的非金属元素 D.稀有气体元素
|
|
| 7. | 详细信息 |
|
反应4A(g)+5B(g)=4C(g)+4D(g)在0.5L密闭容器中进行,30s后A减少了0.90mol,则此反应的速率可表示为 A.v(A)= 0.030mol/(L ·s) B.v(B)=0.075mol/(L· s) C.v(C)=0.030mol/(L· s) D.v(D)=0.030mol/(L· s)
|
|
| 8. | 详细信息 |
|
下列化合物中,既有离子键,又有共价键的是 A.H2O B.CaCl2 C.KOH D.NH3
|
|
| 9. | 详细信息 |
|
A、B、C、D、E是同一周期的五种主族元素,A和B的最高价氧化物对应的水化物均呈碱性,且碱性B>A,C和D的气态氢化物的稳定性C>D;E是这五种元素中简单离子半径最小的元素,则它们的原子序数由大到小的顺序是 A.A、B、C、D、E B.C、D、E、A、B C.B、A、D、C、E D.C、D、A、B、E
|
|
| 10. | 详细信息 |
|
下列关于实验现象的描述不正确的是 A.铜锌原电池中铜是正极 B.把铜片和铁片紧靠在一起浸入稀硫酸中,铜片表面出现气泡 C.把铜片插入三氯化铁溶液中,在铜片表面出现一层铁 D.把锌粒放入盛有盐酸的试管中,加几滴氯化铜溶液,气泡放出速率加快
|
|
| 11. | 详细信息 |
|
有下列物质:① NaOH固体;② 浓硫酸;③ NH4NO3晶体;④ CaO固体。现将它们分别装入有水的锥形瓶里,立即塞紧带U形管的塞子,发现U形管内的滴有红墨水的水面呈形如右图所示状态,判断加入的物质可能是 A.①②③④ B.①②④ C.②③④ D.①②③
|
|
| 12. | 详细信息 |
|
主族元素X、Y、Z的离子为aX+、bY2—、cZ—,半径大小关系是X+<Z—<Y2—下列说法不正确的是 A.b一定小于c B.单质的还原性X>Z C. Y2—的还原性大于Z— D.X、Y可处于同周期或X在Y的下周期
|
|
| 13. | 详细信息 |
|
下列各组物质的性质及粒子的性质变化正确的是 A.稳定性H2S>HCl>HBr>HI B.还原性Na+>S2->Br ->Cl‾ C.离子半径Cl->K+>S2->S D.酸性HClO4 >H2SO4>H2CO3>HClO
|
|
| 14. | 详细信息 |
|
键能是指破坏(或形成)1mol化学键所吸收(或放出)的能量。化学反应就是旧键的断裂和新键形成的过程。现查得:H-H、Cl-Cl和H-Cl的键能分别为436KJ/mol、243KJ/mol和431KJ/mol,请用此数据估计,由Cl2、H2生成1molHCl时的热效应 A.放热183KJ B.放热91.5KJ C.吸热183KJ D.吸热91.5KJ
|
|
| 15. | 详细信息 |
|
.关于含高能量的正离子N5+的化合物N5ASF6,下列叙述中错误的是 A.N5+共有34个核外电子 B.N5+中氮原子间以共价键结合 C.化合物N5ASF6中AS的化合价为+1价 D.化合物N5ASF6中F的化合价为 -1价
|
|
| 16. | 详细信息 |
|
在一个不传热的密闭容器中发生可逆反应:A2(g)+B2(g)≒2AB(g),达到平衡的标志是 A.容器的总压强不随时间而变化 B.容器内气体的密度不再改变 C.单位时间内有nmolA2生成的同时有nmolB2消耗 D. v正(A2)= 2v逆(AB)
|
|
| 17. | 详细信息 |
|
应用元素周期律分析下列推断,其中正确的组合是 ①碱金属单质的熔点随原子序数的增大而降低 ②砹(At)是VIIA族,其氢化物的稳定性大于HC1 ③硒(Se)的最高价氧化物对应水化物的酸性比硫酸弱 ④第二周期非金属元素的气态氢化物溶于水后,水溶液均为酸性 ⑤铊(TI)与铝同主族,其单质既能与盐酸反应又能与氢氧化钠溶液反应 ⑥第三周期金属元素的最高价氧化物对应水化物,其碱性随原子序数的增大而减弱 A.①③④ B.①③⑥ C.③④⑤ D.②④⑥
|
|
| 18. | 详细信息 |
|
在离子 RO3n- 中, 共有 x 个核外电子, R 原子的质量数为 A, 则 R 原子核内含有的中子数目是: A. A – x + n + 48 B. A – x + n + 24 C. A – x - n – 24 D. A + x - n – 24
|
|
| 19. | 详细信息 |
|
正电子、负质子等都属于反粒子,他们和普通电子、质子的质量、电荷数均相同,而电性相反。1997年年初和年底,欧洲和美国的科研机构先后宣布,他们分别制造出7个和9个反氢原子,这是人类探索反物质的一大进步。你推测反氢原子的结构是 A. 由一个带正电荷的质子和一个带负电荷的电子构成 B. 由一个带负电荷的质子和一个带正电荷的电子构成 C. 由一个不带电荷的中子和一个带负电荷的电子构成 D. 由一个带负电荷的质子和一个带负电荷的电子构成
|
|
| 20. | 详细信息 |
|
A.五种元素一定都是非金属元素 B.五种元素的原子最外层电子数一定都大于2 C.X的氢化物的沸点一定比Z的氢化物的沸点高 D.R的最高价氧化物对应的水化物一定是强酸
|
|
| 21. | 详细信息 |
|
以下反应① NH4NO3溶于水 ②燃烧木炭取暖 ③炸药爆炸 ④酸与碱的中和反应 ⑤生石灰与水作用制熟石灰 ⑥ Ba(OH)2·8H2O与NH4Cl的反应中,属于放热反应的是 ,写出吸热反应的化学方程式__ __ __。
|
|
| 22. | 详细信息 |
|
反应A + 3B = 2C + 2D。在四种不同的情况下的反应速率分别为: ①υ(A)=0.15mol/(L·s) ②υ(B)=0.6mol/(L·s) ③υ(C)=0.4mol/(L·s) ④υ(D)=0.45mol/(L·s) 该反应进行的快、慢顺序为__ 。(填序号)
|
|
| 23. | 详细信息 |
|
按已知的原子结构规律,82号元素X应是第___________周期___________族元素,它的最高正价氧化物的化学式为______________。
|
|
| 24. | 详细信息 |
|
电子表所用的某种钮扣电池的电极材料为Zn和Ag2O,电解质溶液为KOH,其电极反应式为: Zn + 2OH—-2e— = ZnO + H2O Ag2O + H2O + 2e— = 2Ag + 2OH— 电池的负极是______________,正极发生的是_______________反应(填反应类型),总反应式为 。
|
|
| 25. | 详细信息 |
|
在下列几种简单的原电池中,按要求填空: (1)将锌、铜用导线连接后共同浸入2mol/L的稀硫酸中,正极电极反应式为_____________________________,发生 反应(填氧化或还原);电子从 经外电路到 (填锌或铜),溶液中H+ 向 移动(填正极或负极),放电一段时间后,正极区pH值 (填变大、变小或不变)。 (2)将铜片和铁片用导线连接后插入三氯化铁溶液中,也有电流通过电流表。 画出该电池结构的示意图,在图上标出正、负极,电解质和电子流向 写出负极电极反应式为_________________, 总反应的离子方程式为_____ 。 (3)将铁片和石墨电极用导线连接后插入氯化钠溶液中,也有电流通过电流表,请写出负极电极反应式____________,正极电极反应式为_____________。
|
|
| 26. | 详细信息 |
|
已知X、Y、Z、W四种元素分布在元素周期表中的三个不同短周期元素里,且原子序数依次增大。X、W同主族,Y、Z为同周期的相邻元素。W原子的质子数等于Y、Z原子最外层电子数之和。Y的氢化物分子中有3个共价键。Z原子最外层电子数是次外层电子数的3倍。试推断: (1)X、Y两种元素的符号:X 、Y ; (2)W在元素周期表中的位置是 ; (3)由X、Y、Z所形成的共价化合物的化学式是 ,它与W的最高氧化物的水化物的溶液反应时的离子方程式是 。
|
|
| 27. | 详细信息 |
|
在500℃容积为2L的密闭容器中充入2mol SO2和1mol O2, 发生下面反应:2SO2(g)+O2(g) ① SO2的转化率为______; ② O2的平衡浓度为________; ③SO2的平均反应速率为________。
|
|
| 28. | 详细信息 |
|
有A、B、C、D四种短周期元素, 它们的原子序数由A到D依次增大, 已知A和B原子有相同的电子层数, 且A的L层电子数是K层电子数的两倍, C燃烧时呈现黄色火焰, C的单质在点燃条件下与B的单质充分反应, 可以得到与D单质颜色相同的淡黄色固态化合物, 试根据以上叙述回答: 1.元素名称: A ________ B __________ C __________ D ___________ 2.写出AB2 的电子式为 ________________________; 3.用电子式表示化合物 C2D 的形成过程 _________________________________。
|
|