2019甘肃高二上学期人教版(2019)高中化学期末考试
| 1. | 详细信息 |
|
将0.l mol/L醋酸溶液加水稀释,下列说法正确的是 ( ) A.溶液中c(H+)和c(OH-)都减小 B.溶液中c(H+)增大 C.醋酸电离平衡向左移动
|
|
| 2. | 详细信息 |
|
下列溶液加热蒸干后,能析出溶质固体的是 ( ) A. AlCl3 B. KHCO3 C. Fe2(SO4)3 D. NH4HCO3
|
|
| 3. | 详细信息 |
|
. 已知反应:①101 kPa时,2C(s)+O2(g)====2CO(g);ΔH=-221 kJ·mol-1 ②稀溶液中,H+(aq)+OH-====(aq)H2O(l);ΔH=-57.3 kJ·mol-1 下列结论正确的是 ( ) A.碳的燃烧热大于110.5 kJ·mol-1 B.①的反应热为221 kJ·mol-1 C.稀硫酸与稀NaOH溶液反应的中和热为-57.3 kJ·mol-1 D.稀醋酸与稀NaOH溶液反应生成1 mol水,放出57.3 kJ热量
|
|
| 4. | 详细信息 |
|
下列说法中正确的是 ( ) A.在纯水中,c(H+) = c(OH-) = 10-7 mol/L,呈中性 B.常温下溶液中,若c(H+) > 10-7 mol/L,则c(H+) > c(OH-),呈酸性 C.c(H+)越大,则pH越大,溶液的碱性越强 D.pH为0的溶液,其中只有H+而无OH-
|
|
| 5. | 详细信息 |
|
把a.b.c.d四块金属片浸入稀硫酸中,用导线两两相连组成原电池。若a.b相连时,a为负极;c.d相连时,电流由d到c;a.c相连时,c极上产生大量气泡;b.d相连时,b上有大量气泡产生。则四种金属的活动性顺序由强到弱的为 ( ) A. a>b>c>d B. a>c>d>b C. c>a>b>d D. b>d>c>a
|
|
| 6. | 详细信息 |
|
可逆反应:2NO2(g) ①单位时间内生成n molO2的同时生成2n molNO2 ②单位时间内生成n molO2 的同时,生成2n mol NO ③用NO2、NO、O2 的物质的量浓度变化表示的反应速率的比为2 : 2 : 1的状态 ④混合气体的颜色不再改变的状态 ⑤混合气体的密度不再改变的状态 ⑥ 混合气体的平均相对分子质量不再改变的状态 A.①④⑥ B.②③⑤ C.①③④ D.①②③④⑤⑥
|
|
| 7. | 详细信息 | |||
|
在新制的氯水中存在平衡:Cl2+H2O H++Cl-+HClO 若向氯水中投入少量碳酸钙粉末,溶液中发生的变化是: ( ) A.pH值增大,HClO浓度减小 B.pH值减小,HClO浓度增大 C.pH值增大,HClO浓度增大 D.pH值减小,HClO浓度减小
|
||||
| 8. | 详细信息 |
|
化学用语是学习化学的重要工具,下列用来表示物质变化的化学用语中,正确的是 ) A.电解饱和食盐水时,阳极的电极反应式为:2Cl - -2e -==Cl2 ↑ B.氢氧燃料电池的负极反应式:O2 + 2H2O + 4e- == 4OH - C.粗铜精炼时,与电源正极相连的是纯铜,电极反应式为:Cu-2e- == Cu2+ D.钢铁发生电化学腐蚀的正极反应式:Fe-2e - == Fe2+
|
|
| 9. | 详细信息 |
|
将4 mol A气体和2 mol B气体在2 L的容器中混合并在一定条件下发生如下反应:
①用物质A表示的反应平均速率为0.3 mol·L-1·s-1 ②用物质B表示的反应的平均速率为0.6 mol·L-1·s-1 ③2s时物质A的转化率为70% ④2s时物质B的浓度为0.7 mol·L-1 其中正确的是 ( ) A.①③ B.①④ C.②③ D.③④
|
|
| 10. | 详细信息 |
|
用两根铂丝作电极插入KOH溶液中,再分别向两极通入甲烷气体和氧气,可形成燃料电池,该电池放电时的总反应为:CH4+2KOH+2O2==K2CO3+3H2O,下列说法错误的是 ( ) A. 通甲烷的一极为负极,通氧气的一极为正极 B. 放电时通入氧气的一极附近溶液的pH升高 C. 放电一段时间后,KOH的物质的量不发生变化 D. 通甲烷的电极反应式是:CH4+10OH --8e-==CO32-+7H2O
|
|
| 11. | 详细信息 |
|
用惰性电极电解100mL饱和食盐水,一段时间后,在阴极得到112mL H2(标准状况),此时电解质溶液(体积变化忽略不计)的pH为 ( ) A. 13 B. 12 C. 8 D. 1
|
|
| 12. | 详细信息 |
|
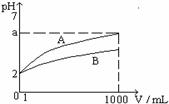
pH=2的A、B两种酸溶液各1mL, 分别加水稀释到1000mL,其溶液的pH与溶液体积(V)的关系如右图所示, 则下列说法正确的是 ( )
B.稀释后A酸溶液的酸性比B酸溶液强 C.a = 5时, A是弱酸, B是强酸 D.若A、B都是弱酸, 则5 > a > 2
|
|
| 13. | 详细信息 |
|
镍镉(Ni-Cd)可充电电池在现代生活中有广泛应用。已知某镍镉电池的电解质溶液为KOH溶液,其充、放电按下式进行:Cd + 2NiOOH + 2H2O Cd(OH)2 + 2Ni(OH)2 有关该电池的说法正确的是 ( ) A.充电时阳极反应:Ni(OH)2-e- + OH- == NiOOH + H2O B.充电过程是化学能转化为电能的过程 C.放电时负极附近溶液的碱性不变 D.放电时电解质溶液中的OH-向正极移动
|
|
| 14. | 详细信息 |
|
氢氰酸(HCN)的下列性质中,可以证明它是弱电解质的是 ( ) A. 1mol/L该酸溶液的pH约为3 B. HCN易溶于水 C. 10 mL1mol/LHCN恰好与10 mL 1mol/L NaOH溶液完全反应 D. 在相同条件下,HCN溶液的导电性比强酸溶液的弱
|
|
| 15. | 详细信息 |
|
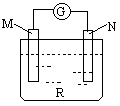
.如图:电流计的指针会偏转,M极变粗,N极变细符合这种现象的是 ( )
B.M是锌,N是铜,R是硫酸铜溶液 C.M是银,N是锌,R是硝酸银溶液 D.M是铁,N是铜,R是硝酸铜溶液
|
|
| 16. | 详细信息 |
|
常温下pH=3的二元弱酸H2R溶液与a L pH=11的NaOH溶液混合后,混合液的pH刚好等于7(假设反应前后体积不变),则对反应后混合液的叙述正确的是 ( ) A. c(R2-)+ c(OH-)=c(Na+)+c(H+) B.c(R2-)>c(Na+)>c(H+)=c(OH-) C. 2c(R2-)+ c(HR-)=c(Na+) D. 混合后溶液的体积为2a L
|
|
| 17. | 详细信息 |
|
在1LK2SO4和CuSO4的混合溶液中,c(SO42-)=2.0 mol·L-1,用石墨作电极电解此溶液,当通电一段时间后,两极均收集到22.4L(标准状况)气体,则原溶液中K+的物质的量浓度为 ( ) A. 2.0 mol·L-1 B. 1.5 mol·L-1 C. 1.0 mol·L-1 D. 0.5 mol·L-1
|
|
| 18. | 详细信息 |
|
下列四种溶液中,由水电离生成的氢离子浓度之比(①∶②∶③)是 ( ) ① pH = 0的盐酸 ② 0.1 mol/L的盐酸 ③ 0.01 mol/L的NaOH溶液 A.1∶10∶100 B.0∶1∶12 C.14∶13∶12 D.14∶13∶2
|
|
| 19. | 详细信息 |
|
已知:① C(s) + O2(g) == CO2(g); △H = -393.5 kJ•mol-1 ② 2CO(g) + O2(g) == 2CO2(g); △H = -566 kJ•mol-1 ③ TiO2(s) + 2Cl2(g) == TiCl4(s) + O2(g); △H = +141 kJ•mol-1 则TiO2(s) + 2Cl2(g) + 2C(s)== TiCl4(s) + 2CO(g) 的△H = _______________。
|
|
| 20. | 详细信息 |
|
常温下,0. 1mol/L下列溶液①NaHCO3 ②Na2CO3 ③NH4Cl ④NaCl ⑤CH3COONa五种溶液PH由大到小的排列顺序为 。
|
|
| 21. | 详细信息 |
|
今有a.盐酸 b.硫酸 c.醋酸三种酸,物质的量浓度为0.1 mol/L的三种酸溶液的pH由大到小的顺序是___________;如果取等体积的0.1 mol/L的三种酸溶液,用0.1 mol/L的NaOH溶液中和,当恰好完全反应时,消耗NaOH溶液的体积由大到小的顺序是______________。(用a、b、c表示)
|
|
| 22. | 详细信息 |
|
明矾可做净水剂的原因: (请用相关的化学用语和文字描述),若向明矾的水溶液中加入饱和的小苏打溶液,则观察到的现象是 ,有关的离子方程式 。
|
|
| 23. | 详细信息 |
|
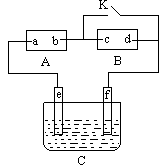
(1)电源A上的a为________极; (2)滤纸B上发生的总化学方程式为___ _______; (3)欲在电镀槽中实现铁上镀锌,接通K点,使c、d两点短路,则电极e上发生的反应为_____ _____,电极f上发生的反应为___________________,电镀槽中放的电镀液可以是________或________(只要求填两种电解质溶液)。
|
|
| 24. | 详细信息 | |||||||||
|
用酸式滴定管准确移取25.00mL某未知浓度的盐酸溶于一洁净的锥形瓶中,然后用0.20mol·L -1的氢氧化钠溶液(指示剂为酚酞).滴定结果如下:
(1)根据以上数据可以计算出盐酸的物质的量浓度为 mol·L-1. (2)达到滴定终点的标志是 (3)以下操作造成测定结果偏高的原因可能是 。 A. 滴定终点读数时,俯视滴定管的刻度,其它操作均正确 B. 滴定到终点读数时发现滴定管尖嘴处悬挂一滴溶液 C. 盛装未知液的锥形瓶用蒸馏水洗过,未用待测液润洗 D. 未用标准液润洗碱式滴定管
|
||||||||||
| 25. | 详细信息 |
|
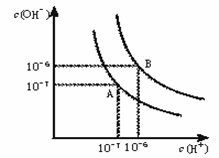
水的电离平衡曲线如下图所示。
(1)若以A点表示25℃时水在电离平衡时的离子浓度, 当温度升到100℃时,水的电离平衡状态到B点,则此时水的离子积从 增加到 。 (2)在100℃下,将pH=8的Ba(OH)2溶液与pH=5的稀盐酸混合,欲使混合溶液pH=7,则Ba(OH)2与盐酸的体积比为 。 (3)在某温度下,Ca(OH)2的溶解度为0.74 g,其饱和溶液密度设为1 g/mL,其离子积约为 。
|
|