天津九年级上学期人教版初中化学月考试卷
| 1. | 详细信息 |
|
金属材料在人类活动中已得到越来越广泛的应用.下列性质属于金属共性的是( ) A.硬度很大、熔点很高 B.是银白色的固体 C.易与酸反应产生氢气 D.能够导电、能够导热
|
|
| 2. | 详细信息 |
|
航天飞机表面覆盖石墨瓦,主要是利用石墨( ) A.具有导电性、防辐射 B.密度小,减轻机身重量 C.熔点高、化学性质稳定 D.硬度小,有润滑作用
|
|
| 3. | 详细信息 |
|
经测定一瓶气体中只含有C、O两种元素,这瓶气体不可能是( ) A.一种化合物 B.两种化合物 C.两种单质 D.一种单质和一种化合物的混合物
|
|
| 4. | 详细信息 |
|
下列过程中只发生物理变化的是( ) A.从铝土矿(主要成分是Al2O3)中提炼金属铝 B.秸秆、杂草、粪便等在沼气池中发酵 C.二氧化碳气体经加压、降温得到干冰 D.排放到空气中的二氧化硫形成酸雨
|
|
| 5. | 详细信息 |
|
物质的性质决定用途.下列物质的用途与物质化学性质无关的是( ) A.用铜丝做导线 B.二氧化碳用于灭火 C.稀有气体做金属焊接保护气 D.用生石灰做食品干燥剂
|
|
| 6. | 详细信息 |
|
下列现象和事实,可用金属活动性作出合理解释的是( ) ①金属镁在空气中比铝更易点燃,说明镁比铝活动性强; ②金属铝比金属锌更耐腐蚀,说明锌比铝活动性强; ③硫酸铜、石灰水配制农药波尔多液,不宜用铁制容器; ④金属锌与稀硫酸反应速率适中,更适于实验室制取氢气. A.①② B.③④ C.①③④ D.①②③④
|
|
| 7. | 详细信息 |
|
以下说法正确的是( ) ①工业上采用液化空气的方法制备氧气和氮气 ②氢气、甲烷在点燃前要检验气体的纯度 ③一般情况下,合金的熔点和硬度都比组成合金的纯金属高 ④氢氧化钠固体潮解、变质与水蒸气和二氧化碳有关 ⑤干冰灭火既能降温,又能隔绝空气,而且灭火后不会留痕迹 ⑥二氧化硫、氮氧化物、一氧化碳和二氧化碳都是大气污染物. A.②③⑤⑥ B.①②④⑥ C.①②④⑤ D.①③④⑤
|
|
| 8. | 详细信息 |
|
钠是一种银白色固体,放置在空气中会迅速与氧气反应生成氧化钠,把钠投入水中,与水剧烈反应,熔化成闪亮小球在水面上游动,生成了氢氧化钠和氢气.下列有关钠的叙述不正确的是( ) A.金属钠必须隔绝空气保存 B.钠与水反应放热,使钠熔化,钠是熔点最低的金属 C.钠和水反应的化学方程式为 2Na+2H2O=2NaOH+H2↑ D.把钠投入硫酸铜溶液中会产生无色无味的气体和蓝色沉淀
|
|
| 9. | 详细信息 |
|
已知一定温度下硫酸铜受热分解生成氧化铜、三氧化硫、二氧化硫和氧气;SO2、SO3都能被氢氧化钠溶液吸收.现进行如下实验:①加热10g硫酸铜粉末至完全分解,②将生成的气体通入足量的浓的氢氧化钠溶液.反应结束后称量①中固体质量变为5g,②中溶液增加了4.5g.该实验中硫酸铜分解的化学方程式是( ) A.3CuSO4 B.4CuSO4 C.5CuSO4 D.6CuSO4
|
|
| 10. | 详细信息 | |||||||||||||||
|
下列除杂方法正确的是( )
A.A B.B C.C D.D
|
||||||||||||||||
| 11. | 详细信息 | ||||||||||||||||||||
|
用如图实验装置制取干燥的气体正确的是( )
A.A B.B C.C D.D
|
|||||||||||||||||||||
| 12. | 详细信息 |
|
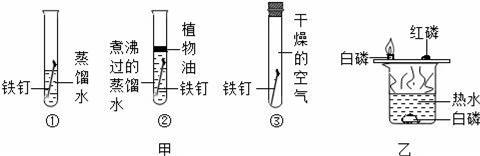
控制变量法是实验探究的重要方法.利用如图所示的实验不能实现的探究目的是( ) A.甲图中①②对比可探究铁的锈蚀与植物油是否有关 B.甲图中①③对比可探究铁的锈蚀与水是否有关 C.乙可探究可燃物的燃烧是否需要达到一定温度 D.乙可探究可燃物的燃烧是否需要与氧气接触
|
|
| 13. | 详细信息 |
|
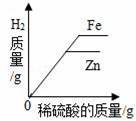
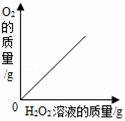
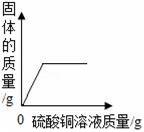
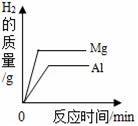
如图所示的四个图象,能正确反映对应变化关系的是( ) A. 等质量的铁、锌分别与质量分数相等且足量的稀硫酸反应 B. 向二氧化锰中加入过氧化氢溶液 C. 向一定质量铁粉和铜粉的混合物中加入硫酸铜溶液 D. 等质量的镁、铝分别与质量分数相等且足量的稀硫酸反应
|
|
| 14. | 详细信息 |
|
某碳酸钙和氧化钙组成的混合物中钙元素的质量分数为60%,将50g该混合物高温煅烧至固体质量不再改变,则生成二氧化碳的质量是( ) A.6g B.8g C.13.2g D.20g
|
|
| 15. | 详细信息 |
|
防锈和回收废旧金属都是保护金属资源的重要途径.为测定一种待回收的废铁中铁的锈蚀程度,某同学取该部分锈蚀的铁片样品(仅由铁和氧化铁组成),测得其中氧元素的含量为12%,则样品中已被锈蚀的铁元素占原金属铁的质量分数约为( ) A.28% B.31.8% C.46.7% D.70%
|
|
| 16. | 详细信息 |
|
生铁和钢含碳量 高.
|
|
| 17. | 详细信息 |
|
为验证 Fe、Mg、Ag 三种金属的活动性顺序.实验室提供的药品有:Mg(NO3)2 溶液、Fe(NO3)2溶液、AgNO3溶液、稀盐酸、银、铁、镁.选用上述药品中的三种,通过两步实验能验证活动性.选用的三种药品是 或 (写 出两组药品的组合,用化学式表示).
|
|
| 18. | 详细信息 |
|
在化学反应中,物质所含元素的化合价发生变化的反应就是氧化还原反应.例如:2Na+Cl2=2NaCl,反应前后Na、Cl的化合价发生了变化,该反应是氧化还原反应. 根据化合价是否发生变化分析,下列反应属于氧化还原反应的是( ) A.2Mg+O2 C.CaCO3 E.CuO+2HCl═CuCl2+H2O F.NaOH+HCl═NaCl+H2O
|
|
| 19. | 详细信息 |
|
.湿法冶金是我国古代劳动人民智慧的结晶,若向ag含杂质的铁粉(假设杂质不溶于水,也不与其他物质梵音)中加入160g溶质质量分数为10%的硫酸铜溶液,恰好完全反应后,过滤得到6.8g干燥固体,同时得到一种不饱和溶液(滤液损失忽略不计).请回答下列问题: (1)根据硫酸铜质量列出求解样品中铁的质量(x)的比例式 (2)a的数值为多少? (3)若向反应后的滤液中加入40.8g水,则所得溶液中溶质的质量分数为多少? (4)工业上若要得到120t上述铁粉,需要含杂质(杂质不含铁元素)20%的赤铁矿的质量是为多少?
|
|
| 20. | 详细信息 |
|
金刚石和石墨的性质不同的原因是 .
|
|
| 21. | 详细信息 |
|
化石燃料燃烧排放的气体会污染环境,其中含有形成酸雨的主要气体,其化学式为 .
|
|
| 22. | 详细信息 |
|
铝制品不易锈蚀的原因是 .
|
|
| 23. | 详细信息 |
|
学校研究性学习小组测定Cu﹣Fe合金和Fe﹣Al合金中铁的质量分数,实验室只提供一瓶未标明质量分数的稀硫酸和必要的仪器. 他们取其中一种合金的粉末56g与足量该硫酸充分反应,经测定,产生了气体a g.请讨论:当粉末为Cu﹣Fe合金时,a< ;当粉末为Fe﹣Al合金时 >a> .
|
|
| 24. | 详细信息 |
|
含有高价态元素的化合物,通常具有氧化性,如在氯化铁溶液中,氯化铁能将单质铜氧化成氯化铜,自身被还原成氯化亚铁.试回答下列问题: ①该反应的化学方程式可表示为 . ②向上述反应后的溶液中加入一定量的锌粉,充分反应后过滤,向滤渣中加入稀盐酸,有 气泡产生.则滤渣中一定含有的物质是 ,滤液中一定不含有的物质是 .向滤渣中加入稀盐酸,无气泡产生.则滤液中一定含有的物质是 ,滤液中可能含有的物质是 (填化学式).
|
|
| 25. | 详细信息 |
|
把质量为10g 的铁片放在50g 硫酸铜溶液中,过一会儿取出,洗净、干 燥、称重,铁片的质量增加到10.6g,问析出 克铜.原硫酸铜溶液的溶质的质量分数是 .
|
|
| 26. | 详细信息 | ||||||||||||||||
|
金属单质A和非金属单质B可生成化合物A2B,反应的化学方程式为2A+B
|
|||||||||||||||||
| 27. | 详细信息 |
|
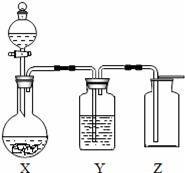
在实验室用如图所示装置进行 CO 和 CO2 的分离和干燥.现只有稀盐 酸、浓硫酸、氢氧化钠溶液,按要求填写下列空白. 操作过程:应先关闭 b,再打开 a,乙中排出 气体. 若获得另一种气体,丙中盛放的溶液为 ,操作为 .
|
|
| 28. | 详细信息 |
|
取0.18g炭在一定量氧气中燃烧,全部转化为一氧化碳和二氧化碳的混合气体.将混合气体通入足量石灰水中,充分反应后,得到0.5g碳酸钙.计算: (1)混合气体中二氧化碳的质量. (2)混合气体中一氧化碳的质量分数.
|
|
| 29. | 详细信息 |
|
化学方程式的书写 (1)酒精的燃烧 (2)化合反应且为吸热 (3)铝和硫酸铜溶液 .
|
|
| 30. | 详细信息 |
|
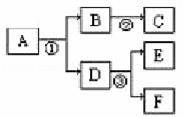
A~F是初中化学常见物质,相互转化关系如下(部分反应物或生成物及反应条件略). (1)若常温下,A、B、E、F为常见的无色气体,且A由两元素组成,其质量比为3:1,D为无色液体,C为白色沉淀.C的化学式 , 写出①反应的化学方程式 . (2)若A和F中含有相同的金属元素,A中两元素的 质量比为7:3,E是一种红色金属,E的化学式 ,写出③中发生反应的化学方程式 .
|
|
| 31. | 详细信息 |
|
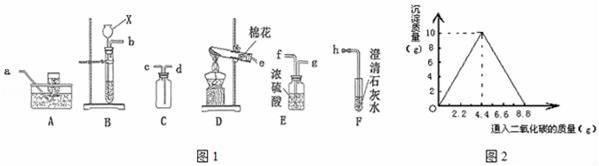
如图1是初中化学中常见的仪器和装置,请认真观察后回答有关问题.
(1)B装置中仪器X的名称是 . (2)实验室用高锰酸钾制取并用排水法收集氧气,可选择的装置是 (3)实验室用大理石和稀盐酸制取和收集一瓶干燥 二氧化碳,同时检验二氧化碳.请按照气流从左到右方向,用仪器接口字母表示连接顺序 ; (4)某实验小组在一定量的石灰水中通入CO2,产生沉淀的质量与通入CO2质量的关系如图2所示.已知反应:CaCO3+H2O+CO2=Ca(HCO3)2,其中CaCO3、Ca(HCO3)2 均属于盐且Ca(HCO3)2易溶于水. ①请描述实验过程中可观察到的现象 . ②请计算通CO2气体前石灰水中溶质Ca(OH)2 的质量 g. ③为使溶液的质量在整个实验过程中为最大值,理论上至少应通入CO2质量 g.(不考虑CO2气体在水中的溶解) ④向含有NaOH和Ca(OH)2的混合溶液中缓缓通入CO2直到过量.其现象为:沉淀 …. 请按照先后顺序写出相应生成盐的化学式: 、 、 、 .
|
|
| 32. | 详细信息 |
|
某同学用如图装置验证某混合气体中一定含有水蒸气、二氧化碳和一氧化碳 三种气体(假设每步操作中,参加反应的气体都完全反应或吸收).
(1)该同学验证三种气体一定存在.实验进行时,若要气体从左向右流动,则这几种仪器的连接顺序应是:混合气体→ → → →D→ → (填A、B、C或E,可以重复); (2)B装置中观察到的现象为 ; (3)实验中两次用到装置E,其目的分别是 , ; (4)混合气体通过A装置发生反应的化学方程式为 请你设计一种尾 气处理方案: .
|
|
| 33. | 详细信息 |
|
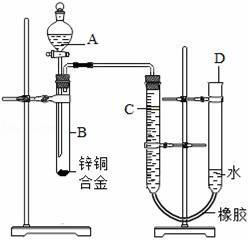
某学习小组用如图所示装置测定锌铜合金中锌、铜的质量分数. (1)实验前,先将锌铜合金在稀酸中浸泡片刻,其目的是: ; (2)实验操作步骤有:检查气密性,将药品和水装入各仪器中,连接 好装置后,再进行的操作还有: ①记录C的液面位置; ②将B中剩余固 体过滤,洗涤,干燥,称重; ③待B中不再有气体产生并恢复至室温后,记录C的液面位置; ④由A向B滴加足量试剂; ⑤检查气密性. 上述进行的操作的顺序是 (填序号);记录C的液面位置 时,除视线平视外,还应 ; (3)B中发生反应的化学方程式为 ; (4)若实验用锌铜合金的质量为a g,与酸充分反应后,B中剩余固体的质量为b g,则锌的质量分数为 ; (5)实验过程中,若未洗涤过滤所得的不溶物,则测得锌的质量分数将 (填“偏大”“偏小”或“不受影响”).
|
|