2020黑龙江高三上学期人教版(2019)高中化学期末考试
| 1. | 详细信息 |
|
陶瓷是火与土的结晶,是中华文明的象征之一,其形成、性质与化学有着密切的关系。下列说法错误的是( ) A.“雨过天晴云破处”所描述的瓷器青色,来自氧化铁 B.闻名世界的秦兵马俑是陶制品,由黏土经高温烧结而成 C.陶瓷是应用较早的人造材料,主要化学成分是硅酸盐 D.陶瓷化学性质稳定,具有耐酸碱侵蚀、抗氧化等优点
|
|
| 2. | 详细信息 |
|
关于化合物2−苯基丙烯( A.不能使稀高锰酸钾溶液褪色 B.可以发生加成聚合反应 C.分子中所有原子共平面 D.易溶于水及甲苯
|
|
| 3. | 详细信息 |
|
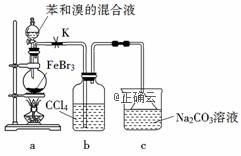
实验室制备溴苯的反应装置如图所示,关于实验操作或叙述错误的是( )
A.向圆底烧瓶中滴加苯和溴的混合液前需先打开K B.实验中装置b中的液体逐渐变为浅红色 C.装置c中的碳酸钠溶液的作用是吸收溴化氢 D.反应后的混合液经稀碱溶液洗涤、结晶,得到溴苯
|
|
| 4. | 详细信息 |
|
固体界面上强酸的吸附和离解是多相化学在环境、催化、材料科学等领域研究的重要课题。下图为少量HCl气体分子在253K冰表面吸附和溶解过程的示意图。下列叙述错误的是( )
A.冰表面第一层中,HCl以分子形式存在 B.冰表面第二层中, C.冰表面第三层中,冰的氢键网格结构保持不变 D.冰表面各层之间,均存在可逆反应
|
|
| 5. | 详细信息 |
|
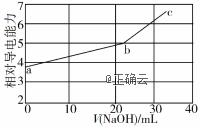
NaOH溶液滴定邻苯二甲酸氢钾(邻苯二甲酸氢钾
A.混合溶液的导电能力与离子浓度和种类有关 B. C.b点的混合溶液pH=7 D.c点的混合溶液中,
|
|
| 6. | 详细信息 |
|
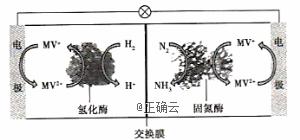
利用生物燃料电池原理研究室温下氨的合成,电池工作时MV2+/MV+在电极与酶之间传递电子,示意图如下所示。下列说法错误的是( )
A.相比现有工业合成氨,该方法条件温和,同时还可提供电能 B.阴极区,在氢化酶作用下发生反应H2+2MV2+=2H++2MV+ C.正极区,固氮酶为催化剂,N2发生还原反应生成NH3 D.电池工作时质子通过交换膜由负极区向正极区移动
|
|
| 7. | 详细信息 |
|
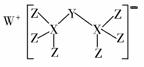
科学家合成出了一种新化合物(如图所示),其中W、X、Y、Z为同一短周期元素,Z核外最外层电子数是X核外电子数的一半。下列叙述正确的是( )
A.WZ的水溶液呈碱性 B.元素非金属性的顺序为X>Y>Z C.Y的最高价氧化物的水化物是中强酸 D.该新化合物中Y不满足8电子稳定结构
|
|
| 8. | 详细信息 |
|
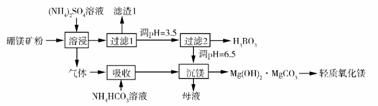
硼酸(
回答下列问题: 1.在95 ℃“溶侵”硼镁矿粉,产生的气体在“吸收”中反应的化学方程式为_________。 2.“滤渣1”的主要成分有_________。为检验“过滤1”后的滤液中是否含有 3.根据 4.在“沉镁”中生成
|
|
| 9. | 详细信息 |
|
硫酸铁铵[NH4Fe(SO4)2•xH2O]是一种重要铁盐。为充分利用资源,变废为宝,在实验室中探究采用废铁屑来制备硫酸铁铵,具体流程如下:
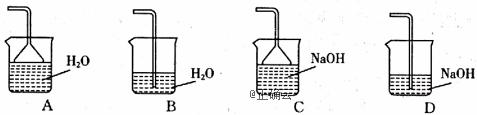
回答下列问题: 1.步骤①的目的是去除废铁屑表面的油污,方法是_________________。 2.步骤②需要加热的目的是_________________,温度保持80~95 ℃,采用的合适加热方式是_________________。铁屑中含有少量硫化物,反应产生的气体需要净化处理,合适的装置为_________________(填标号)。
3.步骤③中选用足量的 4.步骤⑤的具体实验操作有______________,经干燥得到硫酸铁铵晶体样品。 5.采用热重分析法测定硫酸铁铵晶体样品所含结晶水数,将样品加热到150 ℃时,失掉1.5个结晶水,失重5.6%。硫酸铁铵晶体的化学式为______________。
|
|
| 10. | 详细信息 |
|
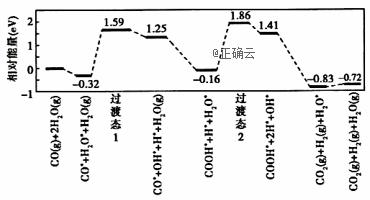
水煤气变换[ 1.Shibata曾做过下列实验:①使纯H2缓慢地通过处于721 ℃下的过量氧化钴CoO(s),氧化钴部分被还原为金属钴(Co),平衡后气体中H2的物质的量分数为0.0250。 ②在同一温度下用CO还原CoO(s),平衡后气体中CO的物质的量分数为0.0192。 根据上述实验结果判断,还原CoO(s)为Co(s)的倾向是CO_________H2(填“大于”或“小于”)。 2.721 ℃时,在密闭容器中将等物质的量的CO和H2O(g)混合,采用适当的催化剂进行反应,则平衡时体系中H2的物质的量分数为( ) A.<0.25 B.0.25 C.0.25~0.50 D.0.50 E.>0.50 3.我国学者结合实验与计算机模拟结果,研究了在金催化剂表面上水煤气变换的反应历程,如图所示,其中吸附在金催化剂表面上的物种用*标注。
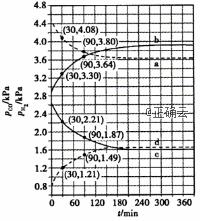
可知水煤气变换的ΔH________0(填“大于”“等于”或“小于”),该历程中最大能垒(活化能)E正=_________eV,写出该步骤的化学方程式_______________________。 4.Shoichi研究了467 ℃、489 ℃时水煤气变换中CO和H2分压随时间变化关系(如下图所示),催化剂为氧化铁,实验初始时体系中的
计算曲线a的反应在30~90 min内的平均速率
|
|
| 11. | 详细信息 | ||||||||||
|
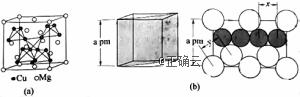
[化学——选修3:物质结构与性质] 在普通铝中加入少量Cu和Mg后,形成一种称为拉维斯相的 1.下列状态的镁中,电离最外层一个电子所需能量最大的是( ) A.[Ne] B.[Ne] C.[Ne] D.[Ne] 2.乙二胺( 3.一些氧化物的熔点如下表所示:
解释表中氧化物之间熔点差异的原因_______________。 4.图(a)是
|
|||||||||||
| 12. | 详细信息 |
|
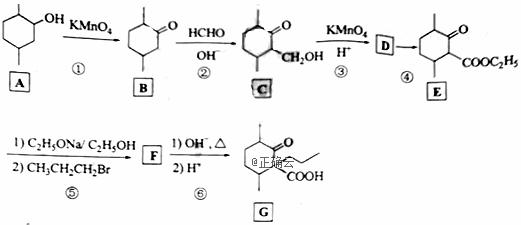
化合物G是一种药物合成中间体,其合成路线如下:
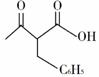
回答下列问题: 1.A中的官能团名称是_____________。 2.碳原子上连有4个不同的原子或基团时,该碳称为手性碳。写出B的结构简式,用星号(*)标出B中的手性碳_____________。 3.写出具有六元环结构、并能发生银镜反应的B的同分异构体的结构简式_____________。(不考虑立体异构,只需写出3个) 4.反应④所需的试剂和条件是______________。 5.⑤的反应类型是_________________。 6.写出F到G的反应方程式_______________。 7.设计由甲苯和乙酰乙酸乙酯(
|
|