2020еӣӣе·қй«ҳдәҢдёӢеӯҰжңҹдәәж•ҷзүҲ(2019)й«ҳдёӯеҢ–еӯҰжңҹдёӯиҖғиҜ•
| 1. | иҜҰз»ҶдҝЎжҒҜ | |||||||||||||||
|
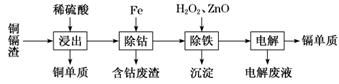
ж№ҝжі•зӮјй”Ңдә§з”ҹзҡ„й“ңй•үжёЈдё»иҰҒеҗ«й”ҢгҖҒй•ү(Cd)гҖҒй“ңгҖҒй“ҒгҖҒй’ҙ(Co)зӯүйҮ‘еұһеҚ•иҙЁгҖӮеҲ©з”Ёй“ңй•үжёЈеҸҜз”ҹдә§CuгҖҒCdеҸҠZnSO4В·7H2O зӯүпјҢе…¶з”ҹдә§жөҒзЁӢеҰӮеӣҫпјҡ
дёӢиЎЁжҳҜйғЁеҲҶйҮ‘еұһзҰ»еӯҗз”ҹжҲҗж°ўж°§еҢ–зү©жІүж·Җзҡ„pH(ејҖе§ӢжІүж·Җзҡ„pHжҢүйҮ‘еұһзҰ»еӯҗжө“еәҰдёә0.1 molВ·L-1и®Ўз®—)пјҡ
е·ІзҹҘжөёеҮәеҗҺзҡ„жә¶ж¶ІдёӯйҮ‘еұһе…ғзҙ йғҪд»ҘдәҢд»·йҳізҰ»еӯҗеҪўејҸеӯҳеңЁпјҢиҜ·еӣһзӯ”дёӢеҲ—й—®йўҳпјҡ (1)дёәеҠ еҝ«й“ңй•үжёЈзҡ„вҖңжөёеҮәвҖқйҖҹзҺҮеҸҜйҮҮз”Ёзҡ„жҺӘж–Ҫжңү________________________________(еҶҷеҮә1жқЎеҚіеҸҜ)гҖӮ (2)вҖңйҷӨй’ҙвҖқдёӯеҸ‘з”ҹеҸҚеә”зҡ„зҰ»еӯҗж–№зЁӢејҸжҳҜ__________________________________гҖӮ (3)вҖңйҷӨй“ҒвҖқж“ҚдҪңдёӯеҠ е…ҘH2O2еҸ‘з”ҹеҸҚеә”зҡ„зҰ»еӯҗж–№зЁӢејҸ___________________________пјҢеҠ е…ҘZnOзҡ„зӣ®зҡ„жҳҜи°ғиҠӮжә¶ж¶ІpHпјҢд»ҘйҷӨеҺ»жә¶ж¶Ідёӯзҡ„й“Ғе…ғзҙ пјҢи°ғиҠӮжә¶ж¶ІpHзҡ„иҢғеӣҙдёә_________гҖӮ (4)вҖңз”өи§ЈвҖқж“ҚдҪңдёӯпјҢеҫ—еҲ°йҮ‘еұһCdзҡ„з”өжһҒеҸҚеә”ејҸжҳҜ________________________гҖӮ (5)вҖңз”өи§ЈвҖқеҗҺзҡ„з”өи§Јеәҹж¶ІжҳҜZnSO4жә¶ж¶ІпјҢз”ЁиҜҘз”өи§Јеәҹж¶ІеҲ¶еӨҮZnSO4В·7H2Oзҡ„ж–№жі•жҳҜ__________________гҖҒиҝҮж»ӨгҖӮ
|
||||||||||||||||
| 2. | иҜҰз»ҶдҝЎжҒҜ |
|
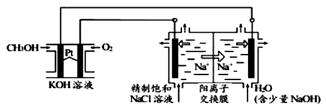
д»ҘCH3OHзҮғж–ҷз”өжұ дёәз”өжәҗз”өи§Јжі•еҲ¶еҸ–ClO2гҖӮдәҢж°§еҢ–ж°Ҝ(ClO2)дёәдёҖз§Қй»„з»ҝиүІж°”дҪ“пјҢжҳҜеӣҪйҷ…дёҠе…¬и®Өзҡ„й«ҳж•ҲгҖҒе№ҝи°ұгҖҒеҝ«йҖҹгҖҒе®үе…Ёзҡ„жқҖиҸҢж¶ҲжҜ’еүӮгҖӮ
(1)CH3OHзҮғж–ҷз”өжұ ж”ҫз”өиҝҮзЁӢдёӯпјҢз”өи§ЈиҙЁжә¶ж¶Ізҡ„pH______пјҲеЎ«вҖңеўһеӨ§вҖқгҖҒвҖңеҮҸе°ҸвҖқжҲ–вҖңдёҚеҸҳвҖқпјүпјҢжӯЈжһҒеҸҚеә”ејҸдёә______гҖӮ (2)еңЁйҳҙжһҒе®Өж°ҙдёӯеҠ е…Ҙе°‘йҮҸзҡ„NaOHзҡ„дҪңз”ЁжҳҜВ В В В В В В В В В В В В В В В В В В В В В В В В В В В В В В В пјҢдә§з”ҹзҡ„ж°”дҪ“дёәпјҡВ В В В В В пјҲеҢ–еӯҰејҸпјүгҖӮ (3)еӣҫдёӯз”өи§Јжұ з”ЁзҹіеўЁдҪңз”өжһҒпјҢеңЁдёҖе®ҡжқЎд»¶дёӢз”өи§ЈйҘұе’ҢйЈҹзӣҗж°ҙеҲ¶еҸ–ClO2пјҢйҳіжһҒдә§з”ҹClO2зҡ„з”өжһҒеҸҚеә”ејҸдёә______гҖӮ (4)з”өи§ЈдёҖж®өж—¶й—ҙпјҢд»ҺйҳҙжһҒеӨ„收йӣҶеҲ°зҡ„ж°”дҪ“жҜ”йҳіжһҒеӨ„收йӣҶеҲ°ж°”дҪ“еӨҡ10.08Lж—¶пјҲж ҮеҮҶзҠ¶еҶөпјҢеҝҪз•Ҙз”ҹжҲҗзҡ„ж°”дҪ“жә¶и§ЈпјүпјҢеҒңжӯўз”өи§ЈпјҢйҖҡиҝҮйҳізҰ»еӯҗдәӨжҚўиҶңзҡ„йҳізҰ»еӯҗдёә______molгҖӮ
|
|
| 3. | иҜҰз»ҶдҝЎжҒҜ |
|
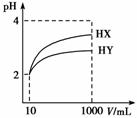
еёёжё©дёӢпјҢ10 mL pHеқҮдёә2зҡ„HXгҖҒHYдёӨз§ҚдёҖе…ғй…ёжә¶ж¶ІпјҢеҠ ж°ҙзЁҖйҮҠиҝҮзЁӢдёӯжә¶ж¶Ізҡ„pHйҡҸжә¶ж¶ІдҪ“з§ҜеҸҳеҢ–жӣІзәҝеҰӮеӣҫжүҖзӨәпјҢиҜ·еӣһзӯ”дёӢеҲ—й—®йўҳпјҡ
(1)10 mL pH=2зҡ„зӣҗй…ёеҠ ж°ҙзЁҖйҮҠеҲ°1000 mLпјҢpH=В В В В В В В гҖӮ (2)зү©иҙЁзҡ„йҮҸжө“еәҰеқҮдёә0.1 molВ·LвҲ’1зҡ„NaXе’ҢNaYжә¶ж¶ІпјҢpHиҫғеӨ§зҡ„жҳҜВ В В В В В В (еЎ«еҢ–еӯҰејҸпјҢдёӢеҗҢ)пјҢе…¶дёӯж°ҙзҡ„з”өзҰ»зЁӢеәҰиҫғе°Ҹзҡ„жҳҜВ В В В В В В гҖӮ (3)зӯүдҪ“з§ҜпјҢpHеқҮдёә2зҡ„дёүз§Қй…ёпјҡв‘ HXгҖҒв‘ЎHYгҖҒв‘ўHClеҲҶеҲ«иў«еҗҢжө“еәҰзҡ„NaOHжә¶ж¶Іе®Ңе…Ёдёӯе’ҢпјҢж¶ҲиҖ—NaOHжә¶ж¶Ізҡ„дҪ“з§Ҝз”ұеӨ§еҲ°е°ҸеҲҶеҲ«дёәпјҲеЎ«зј–еҸ·пјүВ В В В В В В В В гҖӮ (4)H2ZжҳҜдёҖз§ҚдәҢе…ғејұй…ёпјҢеёёжё©дёӢпјҢ0.1 molВ·LвҲ’1зҡ„H2Zжә¶ж¶ІдёӯеҠ е…ҘзӯүдҪ“з§ҜpH=13зҡ„KOHжә¶ж¶ІеҗҺпјҢжә¶ж¶Ізҡ„pH>7пјҢеҺҹеӣ еҸҜиғҪжҳҜВ В В В В В В В В В В В В В В В В В В В В В В В В В В В В В В В В В В В В В В В В В В В В В В гҖӮ
|
|
| 4. | иҜҰз»ҶдҝЎжҒҜ |
|
е·ІзҹҘKгҖҒKaгҖҒKwгҖҒKspеҲҶеҲ«иЎЁзӨәеҢ–еӯҰе№іиЎЎеёёж•°гҖҒејұй…ёзҡ„з”өзҰ»е№іиЎЎеёёж•°гҖҒж°ҙзҡ„зҰ»еӯҗз§Ҝеёёж•°гҖҒйҡҫжә¶з”өи§ЈиҙЁзҡ„жә¶еәҰз§Ҝеёёж•°гҖӮ (1)жңүе…ідёҠиҝ°еёёж•°зҡ„иҜҙжі•жӯЈзЎ®зҡ„жҳҜВ В В В гҖӮ aпјҺе®ғ们зҡ„еӨ§е°ҸйғҪйҡҸжё©еәҰзҡ„еҚҮй«ҳиҖҢеўһеӨ§ bпјҺе®ғ们йғҪиғҪеҸҚжҳ дёҖе®ҡжқЎд»¶дёӢеҜ№еә”еҸҜйҖҶиҝҮзЁӢиҝӣиЎҢзҡ„зЁӢеәҰ cпјҺеёёжё©дёӢпјҢCH3COOHеңЁж°ҙдёӯзҡ„KaеӨ§дәҺеңЁйҘұе’ҢCH3COONaжә¶ж¶Ідёӯзҡ„Ka (2)е·ІзҹҘ25в„ғж—¶CH3COOHе’ҢNH3В·H2Oз”өзҰ»еёёж•°зӣёзӯүпјҢеҲҷиҜҘжё©еәҰдёӢCH3COONH4жә¶ж¶Ізҡ„pH=В В В В В В пјҢжә¶ж¶ІдёӯзҰ»еӯҗжө“еәҰеӨ§е°Ҹе…ізі»дёәВ В В В В В В В В В В В В В В В В В В В В В В В В В В В В В В В гҖӮ (3)зЎқй…ёй“ңжә¶ж¶Іи’ёе№ІгҖҒзҒјзғ§еҗҺеҫ—еҲ°зҡ„еӣәдҪ“зү©иҙЁжҳҜВ В В В В В В В В В гҖӮ (4)жҳҺзҹҫеҮҖж°ҙеҺҹзҗҶВ В В В В В В В В В В В В В В В В В В В В В В В В В В В В В В В В В В В В гҖӮ(з”ЁзҰ»еӯҗж–№зЁӢејҸиЎЁзӨә) (5)е·ІзҹҘеңЁ25в„ғж—¶Ksp[AgCl)=1.8Г—10-10пјҢKsp(Ag2CrO4)=1Г—10-12гҖӮ25в„ғж—¶пјҢеҗ‘жө“еәҰеқҮдёә0.02molВ·L-1зҡ„NaClе’ҢNa2CrO4ж··еҗҲжә¶ж¶ІдёӯйҖҗж»ҙеҠ е…ҘAgNO3жә¶ж¶ІпјҢе…ҲжһҗеҮәВ В В В В В (еЎ«еҢ–еӯҰејҸ)жІүж·ҖпјҢеҪ“дёӨз§ҚжІүж·Җе…ұеӯҳж—¶пјҢ
|
|
| 5. | иҜҰз»ҶдҝЎжҒҜ |
|
еёёжё©дёӢпјҢжңүдёӨз§Қжә¶ж¶Іпјҡв‘ 0.1 molВ·LвҲ’1 CH3COOHжә¶ж¶ІВ в‘Ў0. (1)жә¶ж¶Ів‘ зҡ„pH______7(еЎ«вҖңеӨ§дәҺвҖқгҖҒвҖңе°ҸдәҺвҖқжҲ–вҖңзӯүдәҺвҖқ)пјҢйҶӢй…ёз”өзҰ»е№іиЎЎеёёж•°Ka=В В В В В В В В В В В (иЎЁиҫҫејҸ)гҖӮ (2)жә¶ж¶Ів‘ в‘ЎзӯүдҪ“з§Ҝж··еҗҲеҗҺжә¶ж¶Іе‘Ҳ______жҖ§пјҢж··еҗҲжә¶ж¶Ізҡ„зү©ж–ҷе®ҲжҒ’е…ізі»дёәпјҡ________________________________гҖӮ (3)дёӢеҲ—иҜҙжі•жӯЈзЎ®зҡ„жҳҜ________(еЎ«еәҸеҸ·)гҖӮ aпјҺдёӨз§Қжә¶ж¶Ідёӯc(CH3COOвҲ’)йғҪе°ҸдәҺ0.1 molВ·LвҲ’1 bпјҺдёӨз§Қжә¶ж¶Ідёӯc(CH3COOвҲ’)йғҪзӯүдәҺ0.1 molВ·LвҲ’1 cпјҺCH3COOHжә¶ж¶Ідёӯc(CH3COOвҲ’)е°ҸдәҺCH3COONaжә¶ж¶Ідёӯc(CH3COOвҲ’)
|
|
| 6. | иҜҰз»ҶдҝЎжҒҜ |
|
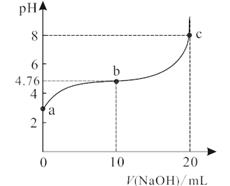
298В Kж—¶пјҢеҗ‘20В mL 0.1В mol/Lжҹҗй…ёHAжә¶ж¶ІдёӯйҖҗж»ҙеҠ е…Ҙ0.1В mol/LВ NaOHжә¶ж¶ІпјҢж··еҗҲжә¶ж¶Ізҡ„pHеҸҳеҢ–жӣІзәҝеҰӮеӣҫжүҖзӨәгҖӮдёӢеҲ—иҜҙжі•й”ҷиҜҜзҡ„жҳҜ
AпјҺHAдёәејұй…ё BпјҺbзӮ№жә¶ж¶Ідёӯпјҡc(AпјҚ)пјһc(Na+)пјһc(HA)пјһc(H+)пјһc(OHпјҚ) CпјҺbгҖҒcд№Ӣй—ҙдёҖе®ҡеӯҳеңЁc(Na+)пјқc(AпјҚ)зҡ„зӮ№ DпјҺжӣІзәҝдёҠaеҲ°cзӮ№пјҡж°ҙзҡ„з”өзҰ»зЁӢеәҰе…ҲеўһеӨ§еҗҺеҮҸе°Ҹ
|
|
| 7. | иҜҰз»ҶдҝЎжҒҜ |
|
еёёжё©дёӢпјҢзўій…ёзҡ„дёӨжӯҘз”өзҰ»еёёж•°еҲҶеҲ«дёәпјҡKa1гҖҒKa2пјҢе…ідәҺ0.1В mol/LВ NaHCO3жә¶ж¶Ізҡ„дёӢеҲ—иҜҙжі•й”ҷиҜҜзҡ„жҳҜ AпјҺжә¶ж¶Ідёӯзҡ„c(HCO BпјҺc(H+)пјӢc(H2CO3)пјқc(CO CпјҺNaHCO3зҡ„ж°ҙи§Је№іиЎЎеёёж•°Khпјқ DпјҺеҚҮй«ҳжё©еәҰжҲ–еҠ е…ҘNaOHеӣәдҪ“пјҢ
|
|
| 8. | иҜҰз»ҶдҝЎжҒҜ |
|
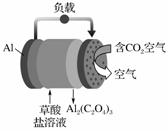
гҖҠ科еӯҰзҫҺеӣҪдәәгҖӢиҜ„еҮәзҡ„2016е№ҙеҚҒеӨ§еҲӣж–°жҠҖжңҜд№ӢдёҖжҳҜзўіе‘јеҗёз”өжұ пјҢеҺҹзҗҶеҰӮеӣҫжүҖзӨәпјҢеҲҷдёӢеҲ—жңүе…іиҜҙжі•жӯЈзЎ®зҡ„жҳҜ
AпјҺд»ҘжӯӨз”өжұ дёәз”өжәҗз”өи§ЈзІҫзӮјй“ңпјҢеҪ“жңү0.1 mol з”өеӯҗиҪ¬з§»ж—¶пјҢжңү3.2 gй“ңжә¶и§Ј BпјҺиҜҘз”өжұ зҡ„иҙҹжһҒеҸҚеә”дёәпјҡ CпјҺжҜҸз”ҹжҲҗ1 mol Al2(C2O4)3пјҢжңү6 molз”өеӯҗжөҒиҝҮиҚүй…ёзӣҗжә¶ж¶І DпјҺжӯЈжһҒжҜҸж¶ҲиҖ—4.48Lзҡ„CO2пјҢеҲҷз”ҹжҲҗ0.1molC2O42пјҚ
|
|
| 9. | иҜҰз»ҶдҝЎжҒҜ |
|
з”ЁзҹіеўЁз”өжһҒз”өи§ЈзЎ«й…ёй“ңжә¶ж¶ІпјҢз”өи§ЈдёҖж®өж—¶й—ҙеҗҺиӢҘйҳҙгҖҒйҳіжһҒеқҮдә§з”ҹж ҮеҶөдёӢ2.24Lж°”дҪ“пјҢиҰҒе°Ҷз”өи§ЈиҙЁжә¶ж¶ІжҒўеӨҚеҲ°з”өи§ЈеүҚпјҢйңҖеҠ е…ҘдёҖе®ҡйҮҸзҡ„ AпјҺCu(OH)2В В В В В В В В BпјҺH2SO4В В В В В В В CпјҺCuOВ В В В В В В В DпјҺH2O
|
|
| 10. | иҜҰз»ҶдҝЎжҒҜ |
|
жө“еәҰеқҮдёә0.1mol/Lзҡ„NH4ClгҖҒ(NH4)2SO4гҖҒNH4HSO4гҖҒ(NH4)2Fe(SO4)2еӣӣз§Қжә¶ж¶ІдёӯпјҢи®ҫNH4+зҰ»еӯҗжө“еәҰеҲҶеҲ«дёә a mol/LгҖҒb mol/Lе’Ңc mol/LпјҢd mol/LеҲҷaгҖҒbгҖҒcгҖҒdе…ізі»дёә AпјҺb=d>a=bВ В В В В В В BпјҺc<a<c<d В В В В В CпјҺa<c<b=dВ В В В В В В В DпјҺa<c<b<d
|
|
| 11. | иҜҰз»ҶдҝЎжҒҜ |
|
еҺҹз”өжұ зҡ„з”өжһҒеҗҚз§°дёҚд»…дёҺз”өжһҒжқҗж–ҷзҡ„жҖ§иҙЁжңүе…іпјҢд№ҹдёҺз”өи§ЈиҙЁжә¶ж¶Іжңүе…ігҖӮдёӢеҲ—иҜҙжі•дёӯдёҚжӯЈзЎ®зҡ„жҳҜ AпјҺз”ұAlгҖҒCuгҖҒзЁҖH2SO4з»„жҲҗеҺҹз”өжұ пјҢе…¶иҙҹжһҒеҸҚеә”ејҸдёәпјҡAlвҲ’3eвҲ’=== Al3+ BпјҺз”ұFeгҖҒCuгҖҒFeCl3жә¶ж¶Із»„жҲҗеҺҹз”өжұ пјҢе…¶иҙҹжһҒеҸҚеә”ејҸдёәпјҡCu вҖ“ 2eпјҚ=== Cu2+ CпјҺз”ұMgгҖҒAlгҖҒNaOHжә¶ж¶Із»„жҲҗеҺҹз”өжұ пјҢе…¶иҙҹжһҒеҸҚеә”ејҸдёәпјҡAl + 4OHпјҚвҲ’ 3eвҲ’ === AlO2пјҚВ + 2H2O DпјҺз”ұAlгҖҒCuгҖҒжө“зЎқй…ёз»„жҲҗеҺҹз”өжұ пјҢе…¶иҙҹжһҒеҸҚеә”ејҸдёәпјҡCu вҖ“ 2eпјҚ=== Cu2+
|
|
| 12. | иҜҰз»ҶдҝЎжҒҜ |
|
дёӢеҲ—е…ізі»зҡ„иЎЁиҝ°дёӯпјҢжӯЈзЎ®зҡ„жҳҜ AпјҺ0.1molвҲҷLп№Ј1NaHSO4жә¶ж¶Ідёӯпјҡc(NaпјӢ)+c(HпјӢ)=c(SO BпјҺ0.1molвҲҷLп№Ј1NaHCO3жә¶ж¶Ідёӯпјҡc(Na+)>c(HCO CпјҺдёӯе’Ңжө“еәҰе’ҢдҪ“з§ҜйғҪзӣёеҗҢзҡ„зӣҗй…ёе’ҢйҶӢй…ёпјҢж¶ҲиҖ—еҗҢжө“еәҰзҡ„NaOHжә¶ж¶Ізҡ„дҪ“з§Ҝд№ӢжҜ”дёә1пјҡ1 DпјҺpH=3зҡ„зӣҗй…ёе’ҢpH=3зҡ„FeCl3жә¶ж¶ІдёӯпјҢз”ұж°ҙз”өзҰ»еҮәзҡ„c(H+)зӣёзӯү
|
|
| 13. | иҜҰз»ҶдҝЎжҒҜ |
|
й…ҚеҲ¶FeCl3жә¶ж¶Іж—¶пјҢе°ҶFeCl3еӣәдҪ“жә¶и§ЈеңЁиҫғжө“зҡ„зӣҗй…ёдёӯпјҢеҶҚеҠ ж°ҙзЁҖйҮҠгҖӮдёӢеҲ—иҜҙжі•й”ҷиҜҜзҡ„жҳҜ AпјҺиҫғжө“зӣҗй…ёеҸҜжңүж•ҲжҠ‘еҲ¶Fe3пјӢж°ҙи§Ј BпјҺзЁҖйҮҠиҝҮзЁӢдёӯFeCl3ж°ҙи§ЈзЁӢеәҰеўһеӨ§пјҢc(HпјӢ)еўһеӨ§ CпјҺFeCl3жә¶ж¶ІдёӯеҠ е…ҘNaHCO3жә¶ж¶Іжңүж°”дҪ“е’ҢзәўиӨҗиүІжІүж·Җдә§з”ҹ DпјҺFeCl3жә¶ж¶Ідёӯж»ҙеҠ KSCNжә¶ж¶ІпјҢжә¶ж¶ІеҮәзҺ°иЎҖзәўиүІ
|
|
| 14. | иҜҰз»ҶдҝЎжҒҜ |
|
иЎЁзӨәдёӢеҲ—еҸҳеҢ–зҡ„еҢ–еӯҰз”ЁиҜӯжӯЈзЎ®зҡ„жҳҜ AпјҺNaHCO3жә¶ж¶ІжҳҫзўұжҖ§пјҡHCO3пјҚ+H2O BпјҺйҶӢй…ёжә¶ж¶Іжҳҫй…ёжҖ§пјҡCH3COOH=CH3COOпјҚ+H+ CпјҺж°Ёж°ҙжҳҫзўұжҖ§пјҡNH3В·H2O DпјҺй“ҒеңЁжҪ®ж№ҝз©әж°”дёӯиў«и…җиҡҖзҡ„иҙҹжһҒеҸҚеә”пјҡFeпјҚ3eпјҚ =Fe3+
|
|
| 15. | иҜҰз»ҶдҝЎжҒҜ |
|
дёӢеҲ—жә¶ж¶Іи’ёе№ІеҗҺиғҪеҫ—еҲ°еҺҹжә¶иҙЁзҡ„жҳҜпјҡ AпјҺNaHCO3В В В В В В В BпјҺNa2SO3В В В В В В В В В CпјҺ(NH4)2SO4В В В В В В DпјҺMgCl2
|
|
| 16. | иҜҰз»ҶдҝЎжҒҜ |
|
жҹҗеҺҹз”өжұ еҸҚеә”зҡ„зҰ»еӯҗж–№зЁӢејҸдёәFe+ 2H+ AпјҺеҸҜз”ЁзЁҖHNO3дҪңз”өи§ЈиҙЁжә¶ж¶І В В В В В В В В В BпјҺжә¶ж¶ІдёӯH+移еҗ‘иҙҹжһҒ CпјҺз”өжұ ж”ҫз”өиҝҮзЁӢдёӯз”өи§ЈиҙЁжә¶ж¶ІpHеҖјеҮҸе°ҸВ В В В DпјҺз”Ёй“ҒдҪңиҙҹжһҒпјҢй“ҒиҙЁйҮҸдёҚж–ӯеҮҸе°‘
|
|
| 17. | иҜҰз»ҶдҝЎжҒҜ |
|
е®Өжё©дёӢпјҢеҗ‘йҘұе’ҢзЎ«й…ёй“ңжә¶ж¶ІдёӯеҠ е…Ҙе°‘йҮҸзҷҪиүІзҡ„CuSO4зІүжң«жҒўеӨҚиҮіе®Өжё©пјҢеҸҚеә”жүҖеҫ—жә¶ж¶Ідёӯ AпјҺc(Cu2+)еўһеӨ§гҖҒc(SO CпјҺn(Cu2+)еҮҸе°ҸгҖҒn(SO
|
|
| 18. | иҜҰз»ҶдҝЎжҒҜ |
|
еңЁзӣҗзұ»еҸ‘з”ҹж°ҙи§Јзҡ„иҝҮзЁӢдёӯпјҢдёӢеҲ—иҜҙжі•дёӯжӯЈзЎ®зҡ„жҳҜ AпјҺзӣҗзҡ„ж°ҙи§ЈдёҚеұһдәҺзҰ»еӯҗеҸҚеә”В В В В В В В В В BпјҺжә¶ж¶Ізҡ„pHеҸҜиғҪдёҚеҸҳ CпјҺжІЎжңүдёӯе’ҢеҸҚеә”еҸ‘з”ҹВ В В В В В В В В В В В В DпјҺж°ҙзҡ„з”өзҰ»зЁӢеәҰдёҚеҸҳ
|
|
| 19. | иҜҰз»ҶдҝЎжҒҜ |
|
дёӢеҲ—дәӢе®һдёҚиғҪз”Ёйҡҫжә¶з”өи§ЈиҙЁзҡ„жә¶и§Је№іиЎЎеҺҹзҗҶжқҘи§ЈйҮҠзҡ„жҳҜ AпјҺзўій…ёй’ЎдёҚиғҪз”ЁдҪңвҖңй’ЎйӨҗвҖқиҖҢзЎ«й…ёй’ЎеҲҷиғҪгҖҖВ В В BпјҺй“қзІүжә¶дәҺж°ўж°§еҢ–й’ жә¶ж¶І CпјҺз”ЁFeSйҷӨеҺ»еәҹж°ҙдёӯеҗ«жңүзҡ„Cu2+гҖҖ В В В В В В DпјҺж°ўж°§еҢ–й“ңжӮ¬жөҠж¶ІдёӯеҠ е…Ҙжө“ж°Ёж°ҙжә¶ж¶ІеҸҳжҫ„жё…
|
|
| 20. | иҜҰз»ҶдҝЎжҒҜ |
|
еҲҶеӯҗејҸдёәC4H8O2зҡ„жңүжңәзү©пјҢеұһдәҺй…Ҝзҡ„еҗҢеҲҶејӮжһ„дҪ“ж•°зӣ®жңү AпјҺ2з§ҚВ В В В В В В BпјҺ3з§ҚВ В В В В В В CпјҺ4з§Қ В В В В DпјҺ5з§Қ
|
|
| 21. | иҜҰз»ҶдҝЎжҒҜ |
|
дёӢеҲ—жңүе…іжңүжңәзү©зҡ„иҜҙжі•дёӯжӯЈзЎ®зҡ„жҳҜ AпјҺеҮЎжҳҜеҗ«зўіе…ғзҙ зҡ„еҢ–еҗҲзү©йғҪеұһдәҺжңүжңәзү© BпјҺжңүжңәзү©дёҖе®ҡеҗ«жңүCгҖҒHдёӨз§Қе…ғзҙ пјҢеҸҜиғҪеҗ«жңүе…¶е®ғе…ғзҙ CпјҺжңүжңәзү©зҶ”жІёзӮ№дёҖиҲ¬иҫғдҪҺ DпјҺжңүжңәзү©йғҪдёҚжә¶дәҺж°ҙ
|
|
| 22. | иҜҰз»ҶдҝЎжҒҜ |
|
гҖҠзӨји®°В·еҶ…еҲҷгҖӢи®°иҪҪпјҡвҖңеҶ еёҰеһўпјҢе’ҢзҒ°жё…жјұпјӣиЎЈиЈіеһўпјҢе’ҢзҒ°жё…жөЈгҖӮвҖқеҸӨдәәжҙ—ж¶ӨиЎЈиЈіеҶ еёҰпјҢжүҖз”Ёзҡ„е°ұжҳҜиҚүжңЁзҒ°жөёжіЎзҡ„жә¶ж¶ІгҖӮдёӢеҲ—иҜҙжі•й”ҷиҜҜзҡ„жҳҜ AпјҺиҚүжңЁзҒ°зҡ„дё»иҰҒжҲҗеҲҶжҳҜзәҜзўұВ В В В В В В BпјҺжҙ—ж¶ӨеҲ©з”ЁдәҶиҚүжңЁзҒ°жә¶ж¶Ізҡ„зўұжҖ§ CпјҺжҙ—ж¶Өж—¶еҠ зғӯеҸҜеўһејәеҺ»жІ№жұЎиғҪеҠӣВ В В DпјҺиҚүжңЁзҒ°еҒҡиӮҘж–ҷж—¶дёҚеҸҜдёҺй“өжҖҒж°®иӮҘж··еҗҲж–Ҫз”Ё
|
|
- й«ҳдәҢдёӢжңҹжңҹжң«жЈҖжөӢеҢ–еӯҰдё“йўҳи®ӯз»ғпјҲ2019-2020е№ҙеӣӣе·қзңҒеҮүеұұе·һпјү
- жұҹиҘҝеёҲиҢғеӨ§еӯҰйҷ„еұһдёӯеӯҰ2020-2021е№ҙй«ҳдёҖдёҠеӯҰжңҹ12жңҲиҖғиҜ•еҢ–еӯҰж— зәёиҜ•еҚ·е®Ңж•ҙзүҲ
- 2018иҮі2019е№ҙй«ҳдёҖдёӢеҶҢжңҹжң«иҖғиҜ•еҢ–еӯҰпјҲеҶ…и’ҷеҸӨејҖжқҘдёӯеӯҰпјү
- 2018иҮі2019е№ҙй«ҳдёҖдёӢеҚҠжңҹжңҹдёӯиҖғиҜ•еҢ–еӯҰе…Қиҙ№иҜ•еҚ·пјҲе®үеҫҪзңҒж»Ғе·һеёӮжҳҺе…үдёӯеӯҰпјү
- еӣӣе·қзңҒжҲҗйғҪеёӮеӣӣе·қеӨ§еӯҰйҷ„еұһдёӯеӯҰж–°еҹҺеҲҶж Ў2021еұҠй«ҳдёүдёҠеӯҰжңҹдёҖиҜҠзғӯиә«иҖғиҜ•зҗҶ科综еҗҲиғҪеҠӣжөӢиҜ•еҢ–еӯҰйўҳеёҰеҸӮиҖғзӯ”жЎҲ
- жҙӣйҳіеёӮй«ҳдәҢеҢ–еӯҰдёҠеҶҢжңҹжң«иҖғиҜ•е…Қиҙ№иҜ•еҚ·е®Ңж•ҙзүҲ
- жұҹиӢҸзңҒеҚ—дә¬еёӮ第еҚҒдәҢдёӯеӯҰ2020-2021е№ҙй«ҳдёҖдёҠеҚҠжңҹжңҹдёӯиҖғиҜ•еҢ–еӯҰйўҳе…Қиҙ№еңЁзәҝжЈҖжөӢ
- 2019еұҠй«ҳдёү第д№қж¬ЎжЁЎжӢҹиҖғиҜ•зҗҶ科综еҗҲеҢ–еӯҰиҖғиҜ•пјҲиҫҪе®ҒзңҒе…ҙеҹҺеёӮпјү