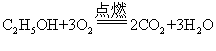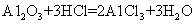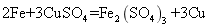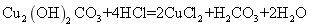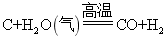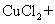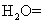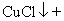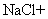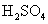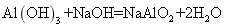2021年黑龙江省大庆市化学中考试题含详解
| 1. | 详细信息 |
|
随着新冠疫情的迅速爆发,人类越来越认识到自然环境的重要性、人类与自然是生命的共同体,人类的生存离不开自然环境。下列叙述错误的是 A . 在工业生产中,采用低碳技术,降低能耗,能体现 “绿色发展”的理念 B . 新冠疫情期间,人们可以用食醋杀死新冠病毒 C . 开发使用可降解塑料,能有效解决 “白色污染”问题 D . 使用无铅汽油可以减少汽车尾气污染 |
|
| 2. | 详细信息 |
|
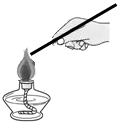
下列图示实验操作正确的是 A . 点燃镁条 C . 加入锌粒 |
|
| 3. | 详细信息 |
|
下列叙述属于化学变化的是 A . 浓硫酸稀释 B . 水力发电 C . 食物的腐烂 D . 碘的升华 |
|
| 4. | 详细信息 |
|
下列表述完全正确的是 A . 钛合金与人体 “相容性”好,可用于制造人造骨 B . 质子数相同的粒子,一定是同种元素的原子 C . 稀有气体化学性质比较稳定,它们的原子最外层都有 8 个电子 D . 有一瓶未知体积的 NaCl 溶液,若使用量筒测量其体积,仰视读数会导致测量结果偏大 |
|
| 5. | 详细信息 | ||||||||||||||||||||||||||||||
|
分类法是学习化学的重要方法之一,某同学对所学的部分化学物质进行分类。其中完全正确的是
A . A B . B C . C D . D |
|||||||||||||||||||||||||||||||
| 6. | 详细信息 |
|
下列化学方程式与事实相符且正确的是 A . 乙醇在空气中完全燃烧: B . 铝土矿溶于盐酸: C . 将洁净的铁丝浸入硫酸铜溶液中: D . 孔雀石溶于稀盐酸: |
|
| 7. | 详细信息 | ||||||||||||||||||||
|
下列除杂所用试剂和主要实验操作均正确的是
A . A B . B C . C D . D |
|||||||||||||||||||||
| 8. | 详细信息 |
|
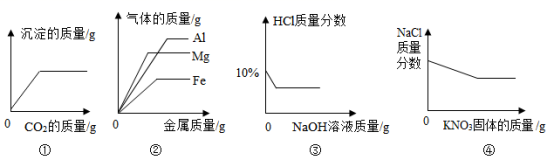
下图所示的图像能正确反映对应变化关系的是 A . ①向 Ca ( OH ) 2 溶液通入 CO 2 至过量 B . ②向等质量、质量分数的一份稀盐酸中分别加入不同的金属 C . ③向一定量 10% 的盐酸中逐滴加入 NaOH 溶液 D . ④ 20 ° C 时,向一定质量分数的 NaCl 溶液中加入 KNO 3 固体 |
|
| 9. | 详细信息 |
|
a 、 b 、 c 三种固体物质的溶解度曲线如图所示。下列说法正确的是 A . t 1 ℃时, a 物质的溶解度是 30g B . t 1 ℃时, b 的饱和溶液中溶质的质量分数为 50% C . t 3 ℃时,各取 15ga 、 b 、 c 三种物质分别加入到 50g 水中充分溶解,能得到饱和溶液的是 c D . t 2 ℃和 t 3 ℃时的两份 b 溶液,所含溶质的质量不可能相等 |
|
| 10. | 详细信息 |
|
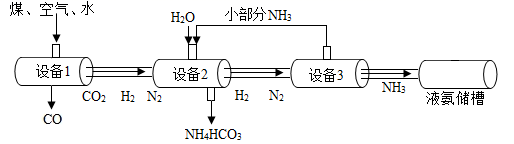
某化肥厂以煤、空气、水为原料合成氨,生产流程如图所示。下列说法错误的是 A . 氨气转变为液氨是放热过程 B . 设备 1 中此反应 C . 设备 2 中发生的反应,属于基本反应类型中的化合反应 D . 设备 3 中参加反应的 N 2 和 H 2 的质量比为 14 : 1 |
|
| 11. | 详细信息 |
|
已知 Mg 能在 CO 2 中燃烧,根据金属活动性顺序表, Na 的金属活动性比 Mg 强,说明 Na 也能在 CO 2 中燃烧。为了验证,实验小组进行了以下实验探究: (查阅资料) ①金属钠性质活泼,常温下,金属钠极易与氧气反应,生成白色固体氧化钠,氧化钠溶于水生成氢氧化钠。全属钠还可以与水剧烈反应,放出氢气。 ② Na 2 CO 3 溶液显碱性; CaCl 2 溶液显中性。 (实验探究一) 步骤 1 :打开活塞,让 A 装置中产生的气体依次通过 B 、 C ,收集一瓶纯净的 CO 2 气体。 步骤 2 :将燃烧的钠迅速伸入集气瓶中,观察到钠在 CO 2 中继续燃烧,发光放热,冷却后观察到瓶内附着黑色颗粒,并粘附着白色物质。 (问题讨论) ( 1 )为获得纯净的 CO 2 ,可利用装置 B 除去 CO 2 中混有的 ______ ;装置 C 中盛放的试剂是 ______ 。 ( 2 )步骤 2 中生成的黑色固体成分是 ______ 。 (初步结论) Na 能在 CO 2 中燃烧。 (提出问题)白色物质是什么? (猜想与假设)猜想一:氧化钠 猜想二:碳酸钠; 猜想三:氧化钠和碳酸钠的混合物; 猜想四:氢氧化钠。 ( 3 )大家讨论后一致认为猜想四是错误的,理由是 ______ 。 (实验探究二)对白色物质是什么进行实验探究,方案设计如下: 方案 1 :取该样品少量于试管中,加入适量的水。振荡,过滤,向滤液中加入无色酚酞试液,观察到溶液变成红色。结论:白色物质中一定有氧化钠。 方案 2 :取该样品少量于试管中,滴加足量盐酸,溶液中有气泡冒出: 结论:白色物质中一定有 ______ 。 方案 3 :取该样品少量于试管中,加入适量的水,振荡,过滤,向滤液中加入过量的氯化钙溶液,出现白色沉淀,过滤,再向滤液中滴加无色酚酞溶液,无明显现象。 (反思与评价) ( 4 )甲同学思考后提出方案 1 得出的结论不正确,其理由是 ______ 。 ( 5 )请将方案 2 结论补充完整: ______ 。(填化学式) ( 6 )方案 3 中加入过量 CaCl 2 溶液的目的是 ______ 。写出此反应的化学方程式 ______ 。 (实验结论) ( 7 )综上所述,你认为猜想 ______ 成立。 ( 8 )请写出 Na 在 CO 2 中燃烧的化学方程式 ______ 。 |
|
| 12. | 详细信息 |
|
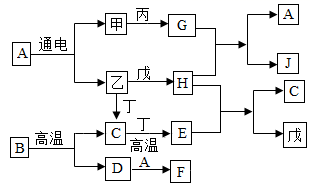
图中的物质均为初中化学常见的物质。其中甲、乙、丙、丁、戊均为单质,丙是一种黄绿色有毒气体,是由 17 号元素组成的双原子分子,丁是黑色固体,戊是紫红色金属;常温下 A 是液态,农业上常用 F 改良酸性土壤(图中部分反应条件已省略)回答下列问题: ( 1 )甲为 ______ ; B 为 ______ 。(填化学式) ( 2 )在电解 A 实验中,与电源 ______ 极相连的一端产生物质乙。 ( 3 )工业上常用丙和 F 制漂白粉( CaCl 2 和 Ca ( C1O ) 2 )。同时生成 A .请写出该反应的化学方程式 ______ 。 ( 4 ) D 和 A 反应 ______ 热量。(填 “吸收”或“放出”) |
|
| 13. | 详细信息 |
|
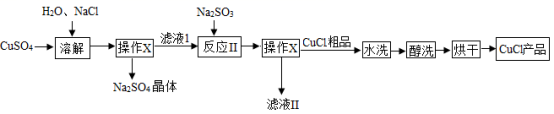
氯化亚铜 CuCl 是一种难溶于水和乙醇且在潮湿空气中易变质的物质,广泛应用于冶金、电镀、医药等行业、 CuCl 的制备流程如下: ( 1 ) “操作 Y ”名称是 ______ 。 ( 2 ) CuCl 中铜元素的化合价为 ______ 。 ( 3 )请配平 “反应Ⅱ”的化学方程式: ______ ( 4 )在 “滤液Ⅱ”中可以循环利用的物质(水除外)是 ______ 。(填化学式) ( 5 ) “醇洗”的目的是 ______ ,防止后续过程中氯化亚铜变质。 |
|
| 14. | 详细信息 |
|
( 1 )墙内开花墙外香,说明 ______ 在不停地运动。 ( 2 )画出钾离子的结构示意图: ______ 。 ( 3 ) “ 冰毒 ” 的化学式是 C 10 H 15 N ,其中碳、氢元素的质量比为 ______ 。 ( 4 )羊毛、蚕丝的主要成分都是 ______ 。(填 “ 蛋白质 ” 或 “ 纤维素 ” ) ( 5 )过磷酸钙是 Ca ( H 2 PO 4 ) 2 和 ______ 的混合物。(填化学式) ( 6 )我们需要清新洁净的空气,为减少雾霾的吸入,人们出行经常戴口罩,是利用口罩中填充物(活性炭)的 ______ 性。 |
|
| 15. | 详细信息 |
|
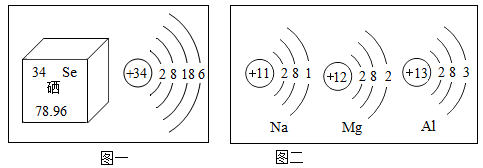
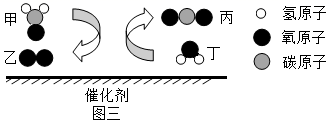
1 、建立 “ 宏观 · 微观 ” 之间的联系,是化学学习的重要方法。根据图示回答下列问题: ( 1 )硒元素被科学家称为 “ 抗癌之王 "” ,科学界研究发现血硒水平的高低与癌的发生息息相关。图一是硒元素的相关信息:硒原子在化学变化中易 ______ 电子(填 “ 得到 ” 或 “ 失去 ” )。硒元素的相对原子质量是 ______ 。 ( 2 )由图二可知:在元素周期表中,钠、镁、铝元素位于同一周期,是因为它们具有相同的 ______ 。 ( 3 )科学家发现,利用催化剂可有效消除室内装修材料释放的有害气体甲醛( HCHO )。请根据图三写出反应的化学方程式 ______ 。 Ⅱ、人们在实验研究中总结出常见金属的活动性顺序: ( 4 )请在表中 ( 5 ) Mg 、 Sn 、 Pb 、 Cu 、 Ag 五种金属,能与稀盐酸(或稀硫酸)发生置换反应的金属有 ______ 种。 |
|
| 16. | 详细信息 |
|
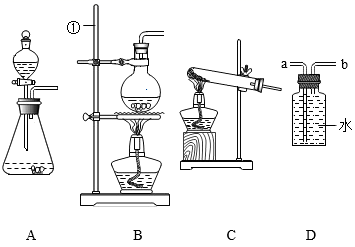
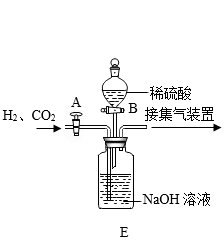
根据下列装置,回答问题: ( 1 )写出图中标号 ①仪器的名称: ______ 。 ( 2 )实验室里常用 H 2 O 2 和 MnO 2 来制取 O 2 ,应选用的发生装置为图中的 ______ 。(填字母) ( 3 )实验室若用装置 D 收集 H 2 ,则气体应从导管 ______ (填 “ a ”或“ b ”)端进入。 ( 4 )工业常需分离 H 2 、 CO 2 的混合气体。某同学采用装置 E 也能达到分离该混合气体的目的。操作步如下: 步骤 1 :关闭活塞 B ,打开活塞 A ,通入混合气体,可收集到 ______ 。 步骤 2 ;然后, ______ (填操作),又可收集到另一种气体。 |
|
| 17. | 详细信息 |
|
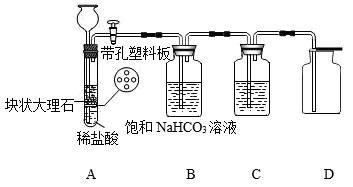
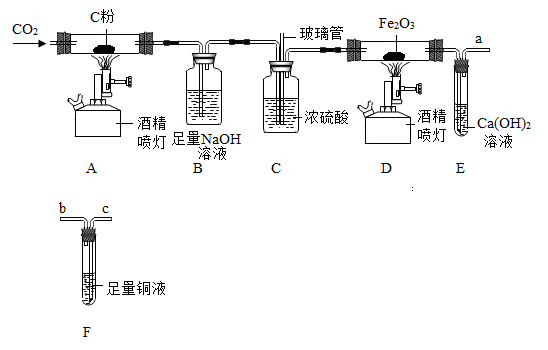
某兴趣小组的同学们利用如图所示的装置对 CO 还原 Fe 2 O 3 粉末的实验进行探究(固定装置略)。 (查阅资料) CO 能溶于铜液(醋酸二氨合铜( Ⅰ)和氨水的混合液) ( 1 )按上图连接装置 A-E ,在装入试剂前,先 ______ 。 ( 2 )写出装置 B 中反应的化学方程式 ______ 。 ( 3 )通入 CO 2 一段时间后,先点燃 ______ 处酒精喷灯(填 “A” 或 “D” )。 ( 4 )装置 C 中玻璃管的作用: ______ 。 ( 5 )反应一段时间后,能证明 CO 与 Fe 2 O 3 反应的实验现象: ______ ; ______ 。写出装置 D 中反应的化学方程式 ______ 。 ( 6 )某同学认为该裝置有缺陷,需在装置 E 后再连接装置 F ,其目的是 ______ 。装置 E . F 的接口连接顺序: a 连接 ______ (填 “b” 或 “c” )。 |
|
| 18. | 详细信息 |
|
将 50.0g 盐酸、氯化镁和氯化铝的混合溶液置于烧杯中,逐滴加入质量分数为 20.0% 的氢氧化钠溶液,生成氢氧化铝沉淀的最大质量为 7.8g 。加入氢氧化钠溶液质量和生成沉淀质量的关系如图所示。请根据题意回答问题: 已知: ( 1 ) B 点溶液中所含溶质是 ______ (填化学式)。 ( 2 )求图中 A 点的坐标: ______ 。 ( 3 )原混合溶液中 MgCl 2 的质量分数是多少?(写出计算过程,计算结果精确到 0.1% ) |
|