2016дә‘еҚ—д№қе№ҙзә§дёӢеӯҰжңҹдәәж•ҷзүҲеҲқдёӯеҢ–еӯҰжңҹдёӯиҖғиҜ•
| 1. | иҜҰз»ҶдҝЎжҒҜ |
|
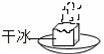
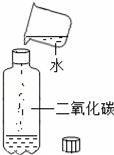
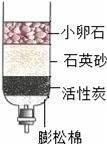
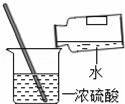
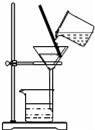
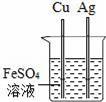
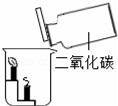
дёӢеӣҫжүҖзӨәзҡ„е®һйӘҢдёӯпјҢеҸ‘з”ҹдәҶеҢ–еӯҰеҸҳеҢ–зҡ„жҳҜпјҲгҖҖгҖҖпјү AпјҺ е№ІеҶ°еҚҮеҚҺВ В В BпјҺ CO2жә¶дәҺж°ҙ CпјҺ е®һйӘҢCO2зҡ„еҜҶеәҰВ В DпјҺ иҮӘеҲ¶иҝҮж»ӨеҷЁиҝҮж»Өж¶ІдҪ“
|
|
| 2. | иҜҰз»ҶдҝЎжҒҜ |
|
з”ұдёӢеҲ—дәӢе®һжҲ–зҺ°иұЎжҺЁеҮәзҡ„з»“и®әдёӯпјҢжӯЈзЎ®зҡ„жҳҜпјҲгҖҖгҖҖпјү AпјҺеёёжё©дёӢжөӢеҫ—жҹҗжә¶ж¶Ізҡ„pH=0пјҢеҲҷиҜҘжә¶ж¶ІдёҖе®ҡжҳҫй…ёжҖ§ BпјҺжҫ„жё…йҖҸжҳҺзҡ„жІіж°ҙдёҖе®ҡжҳҜиҪҜж°ҙ CпјҺиғҪеӨҹдёҺзўұеҸ‘з”ҹеҸҚеә”зҡ„зү©иҙЁдёҖе®ҡжҳҜй…ё DпјҺж»ҙеҠ й…ҡй…һиҜ•ж¶ІжҳҫзәўиүІзҡ„жә¶ж¶ІдёҖе®ҡжҳҜзўұзҡ„жә¶ж¶І
|
|
| 3. | иҜҰз»ҶдҝЎжҒҜ |
|
дёӢеҲ—еӣҫзӨәзҡ„е®һйӘҢж“ҚдҪңпјҢжӯЈзЎ®зҡ„жҳҜпјҲгҖҖгҖҖпјү AпјҺ зЁҖйҮҠжө“зЎ«й…ёВ BпјҺ й…ҚеҲ¶NaClжә¶ж¶ІВ В CпјҺ жөӢе®ҡжә¶ж¶Ізҡ„pHВ В В DпјҺ иҝҮж»Ө
|
|
| 4. | иҜҰз»ҶдҝЎжҒҜ |
|
дёӢеҲ—е®һйӘҢиҝӣиЎҢдёӯзҡ„зҺ°иұЎжҲ–е®һйӘҢеҺҹзҗҶжӯЈзЎ®зҡ„жҳҜпјҲгҖҖгҖҖпјү AпјҺ зҷҪзЈ·е§Ӣз»ҲдёҚзҮғзғ§ BпјҺ е°Ҹж°”зҗғеҸҳзҳӘ CпјҺ UеһӢз®ЎеҶ…ж¶Ійқўе·Ұй«ҳеҸідҪҺ DпјҺ йӘҢиҜҒFeгҖҒCuгҖҒAgзҡ„йҮ‘еұһжҙ»еҠЁжҖ§ејәејұ
|
|
| 5. | иҜҰз»ҶдҝЎжҒҜ | ||||||||||||||||||||
|
дёӢеҲ—е®һйӘҢз»“и®әй”ҷиҜҜзҡ„жҳҜпјҲгҖҖгҖҖпјү
AпјҺAВ В В BпјҺBВ В В CпјҺCВ В В DпјҺD
|
|||||||||||||||||||||
| 6. | иҜҰз»ҶдҝЎжҒҜ |
|
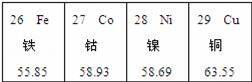
дёӢеӣҫдёәе…ғзҙ е‘Ёжңҹ表第4е‘Ёжңҹзҡ„дёҖйғЁеҲҶпјҺжҚ®жӯӨеҲӨж–ӯд»ҘдёӢиҜҙжі•дёӯй”ҷиҜҜзҡ„жҳҜпјҲгҖҖгҖҖпјү AпјҺй’ҙе…ғзҙ зҡ„з¬ҰеҸ·дёәCO BпјҺй“ңе…ғзҙ зҡ„зӣёеҜ№еҺҹеӯҗиҙЁйҮҸжҳҜ63.55 CпјҺд»Һе·ҰеҲ°еҸіеҗ„е…ғзҙ зҡ„еҺҹеӯҗеәҸж•°дҫқж¬ЎеўһеӨ§ DпјҺеҗ„е…ғзҙ йғҪеұһдәҺйҮ‘еұһе…ғзҙ
|
|
| 7. | иҜҰз»ҶдҝЎжҒҜ |
|
зү©иҙЁXеҸҜеҸ‘з”ҹвҖңв‘ X+зўұвҶ’зӣҗ+H2OвҖқпјҢв‘ЎX+йҮ‘еұһж°§еҢ–зү©вҶ’зӣҗ+H2Oзҡ„еҸҚеә”пјҢеҲҷXеҸҜиғҪжҳҜпјҲгҖҖгҖҖпјү AпјҺNa2CO3В В В BпјҺCO2В CпјҺNaOH DпјҺH2SO4
|
|
| 8. | иҜҰз»ҶдҝЎжҒҜ |
|
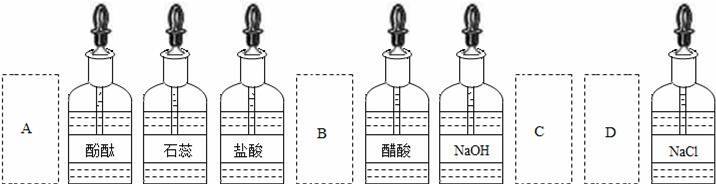
еҢ–еӯҰе®һйӘҢе®Өдёӯзҡ„иҚҜе“ҒжҢүзү©иҙЁзұ»еҲ«еҲҶзұ»ж”ҫзҪ®пјҺеҰӮеӣҫжҳҜеҒҡвҖңй…ёзҡ„жҖ§иҙЁвҖқе®һйӘҢж—¶пјҢе®һйӘҢжЎҢдёҠйғЁеҲҶиҚҜе“Ғзҡ„ж‘Ҷж”ҫжғ…еҶөпјҺе°Ҹжһ—еҸ–з”ЁдәҶзЎ«й…ёд»ҘеҗҺпјҢеә”иҜҘжҠҠе®ғж”ҫеӣһзҡ„дҪҚзҪ®жҳҜпјҲгҖҖгҖҖпјү
AпјҺAВ В В BпјҺBВ В В CпјҺCВ В В DпјҺD
|
|
| 9. | иҜҰз»ҶдҝЎжҒҜ | |||||||||||||||
|
дёӢеҲ—еҢ–еӯҰж–№зЁӢејҸдёҺеҜ№еә”еҸҚеә”зұ»еһӢеқҮжӯЈзЎ®зҡ„жҳҜпјҲгҖҖгҖҖпјү
AпјҺAВ В В BпјҺBВ В В CпјҺCВ В В DпјҺD
|
||||||||||||||||
| 10. | иҜҰз»ҶдҝЎжҒҜ | |||||||||||||||
|
дёӢеҲ—йүҙеҲ«дёӨз§ҚдёҚеҗҢзү©иҙЁзҡ„ж–№жі•пјҢдёҚжӯЈзЎ®зҡ„жҳҜпјҲгҖҖгҖҖпјү
AпјҺAВ В В BпјҺBВ В В CпјҺCВ В В DпјҺD
|
||||||||||||||||
| 11. | иҜҰз»ҶдҝЎжҒҜ |
|
пјҺиҝ‘еҮ е№ҙзҡ„йӣӘзҒҫеҜ№жҲ‘еӣҪеҚ—ж–№зҡ„з”өеҠӣгҖҒдәӨйҖҡйҖ жҲҗеҫҲеӨ§зҡ„еҚұе®іпјҢжңүдёҖз§ҚиһҚйӣӘеүӮеҗ«жңүNa2SiO3пјҢNa2SiO3дёӯSiе…ғзҙ зҡ„еҢ–еҗҲд»·дёәпјҲгҖҖгҖҖпјү AпјҺ+4д»· BпјҺ+3д»· CпјҺ+2д»· DпјҺ+1д»·
|
|
| 12. | иҜҰз»ҶдҝЎжҒҜ |
|
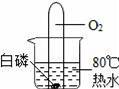
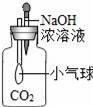
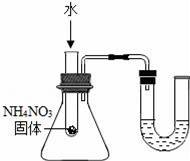
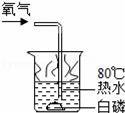
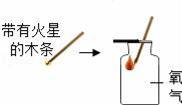
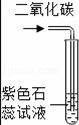
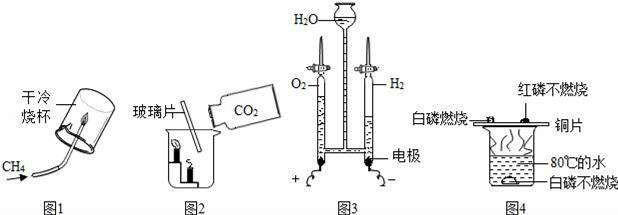
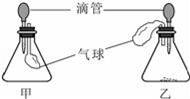
йҖҡиҝҮдёӢеҲ—еӣҫзӨәе®һйӘҢеҫ—еҮәзҡ„з»“и®әдёӯжӯЈзЎ®зҡ„жҳҜпјҲгҖҖгҖҖпјү
AпјҺеӣҫ1жүҖзӨәе®һйӘҢж—ўиҜҙжҳҺз”Ізғ·е…·жңүеҸҜзҮғжҖ§пјҢеҸҲиҜҙжҳҺз”Ізғ·дёӯеҗ«жңүзўігҖҒж°ўдёӨз§Қе…ғзҙ BпјҺеӣҫ2жүҖзӨәе®һйӘҢж—ўиҜҙжҳҺдәҢж°§еҢ–зўіеҜҶеәҰжҜ”з©әж°”еӨ§пјҢеҸҲиҜҙжҳҺдәҢж°§еҢ–зўідёҚиғҪзҮғзғ§д№ҹдёҚж”ҜжҢҒзҮғзғ§ CпјҺеӣҫ3жүҖзӨәе®һйӘҢж—ўиҜҙжҳҺз”өи§Јж°ҙз”ҹжҲҗж°ўж°”е’Ңж°§ж°”пјҢеҸҲиҜҙжҳҺж°ҙжҳҜз”ұж°ўж°”е’Ңж°§ж°”з»„жҲҗзҡ„ DпјҺеӣҫ4жүҖзӨәе®һйӘҢж—ўеҸҜжҺўз©¶еҸҜзҮғзү©зҡ„зҮғзғ§жқЎд»¶пјҢеҸҲиҜҙжҳҺзәўзЈ·дёҚжҳҜеҸҜзҮғзү©
|
|
| 13. | иҜҰз»ҶдҝЎжҒҜ |
|
зү©иҙЁзҡ„дҝ—еҗҚдёҺеҢ–еӯҰејҸзӣёеҜ№еә”жӯЈзЎ®зҡ„жҳҜпјҲгҖҖгҖҖпјү AпјҺеӨ©з„¶ж°”пјҡCOВ В BпјҺзғ§зўұпјҡNa2CO3В CпјҺзҶҹзҹізҒ°пјҡCaпјҲOHпјү2 DпјҺзәҜзўұпјҡNaOH
|
|
| 14. | иҜҰз»ҶдҝЎжҒҜ |
|
жңүXгҖҒYгҖҒZдёүз§ҚйҮ‘еұһпјҢеҸҜд»ҘеҸ‘з”ҹеҰӮдёӢеҸҚеә”пјҡ в‘ X+ZпјҲNO3пјү2=XпјҲNO3пјү2+ZВ в‘ЎX+YSO4=XSO4+YВ в‘ўZ+YSO4=ZSO4+Y еҲҷиҝҷдёүз§ҚйҮ‘еұһзҡ„жҙ»еҠЁжҖ§з”ұејәеҲ°ејұзҡ„йЎәеәҸжҳҜпјҲгҖҖгҖҖпјү AпјҺXпјһZпјһYВ BпјҺZпјһYпјһXВ CпјҺXпјһYпјһZВ DпјҺYпјһZпјһX
|
|
| 15. | иҜҰз»ҶдҝЎжҒҜ |
|
зұ»жҺЁжҳҜеӯҰд№ дёӯеёёз”Ёзҡ„жҖқз»ҙж–№жі•пјҢпјҺзҺ°жңүд»ҘдёӢзұ»жҺЁз»“жһңпјҢе…¶дёӯй”ҷиҜҜзҡ„жҳҜпјҲгҖҖгҖҖпјү в‘ зўұзҡ„ж°ҙжә¶ж¶ІйҖҡеёёе‘ҲзўұжҖ§пјҢжүҖд»ҘзўұжҖ§жә¶ж¶ІдёҖе®ҡжҳҜзўұзҡ„жә¶ж¶І в‘Ўж°§еҢ–зү©дёӯеҗ«жңүж°§е…ғзҙ пјҢжүҖд»Ҙеҗ«жңүж°§е…ғзҙ зҡ„еҢ–еҗҲзү©дёҖе®ҡжҳҜж°§еҢ–зү©пјӣ в‘ўй…ёзўұеҸ‘з”ҹдёӯе’ҢеҸҚеә”з”ҹжҲҗзӣҗе’Ңж°ҙпјҢжүҖд»Ҙз”ҹжҲҗж°ҙзҡ„еҸҚеә”дёҖе®ҡжҳҜдёӯе’ҢеҸҚеә”пјҺ AпјҺеҸӘжңүв‘ В В BпјҺв‘ в‘Ў CпјҺв‘ в‘ў DпјҺв‘ в‘Ўв‘ў
|
|
| 16. | иҜҰз»ҶдҝЎжҒҜ |
|
жҹҗеҗҢеӯҰе°Ҷй”ҢзІ’ж”ҫе…ҘCuSO4жә¶ж¶ІдёӯпјҢеҸ‘зҺ°й”ҢзІ’иЎЁйқўжңүзәўиүІзү©иҙЁжһҗеҮәпјҢеҗҢж—¶иҝҳжңүе°‘йҮҸзү©иүІж— е‘іж°”жіЎдә§з”ҹпјҢеҜ№дә§з”ҹж°”жіЎзҡ„вҖңејӮеёёзҺ°иұЎвҖқпјҢдёӢеҲ—зҢңжғіж— 科еӯҰйҒ“зҗҶзҡ„жҳҜпјҲгҖҖгҖҖпјү AпјҺдә§з”ҹзҡ„ж°”дҪ“еҸҜиғҪжҳҜCO2 BпјҺдә§з”ҹзҡ„ж°”дҪ“еҸҜиғҪжҳҜH2 CпјҺCuSO4жә¶ж¶ІдёӯеҸҜиғҪеҗ«жңүе°‘йҮҸй…ё DпјҺCuSO4жә¶ж¶Ізҡ„pHеҸҜиғҪе°ҸдәҺ7
|
|
| 17. | иҜҰз»ҶдҝЎжҒҜ |
|
з”ІгҖҒд№ҷдёӨз§ҚеӣәдҪ“зҡ„жә¶и§ЈеәҰжӣІзәҝеҰӮеӣҫжүҖзӨәпјҺдёӢеҲ—иҜҙжі•дёӯпјҢжӯЈзЎ®зҡ„жҳҜпјҲгҖҖгҖҖпјү
AпјҺ20в„ғж—¶пјҢз”Іжә¶ж¶Ідёӯжә¶иҙЁзҡ„иҙЁйҮҸеҲҶж•°дёҖе®ҡеӨ§дәҺд№ҷжә¶ж¶І BпјҺ40в„ғж—¶пјҢеҲҶеҲ«еңЁ100 gж°ҙдёӯеҠ е…Ҙ50 g з”ІгҖҒд№ҷпјҢжүҖеҫ—жә¶ж¶Іжә¶иҙЁзҡ„иҙЁйҮҸеҲҶж•°зӣёзӯү CпјҺ40в„ғж—¶пјҢеҲҶеҲ«еңЁ100 gж°ҙдёӯеҠ е…Ҙ30 g з”ІгҖҒд№ҷпјҢеҗҢж—¶йҷҚжё©иҮі20в„ғпјҢз”ІгҖҒд№ҷжә¶ж¶ІеқҮдёәйҘұе’Ңжә¶ж¶І DпјҺ20в„ғж—¶пјҢеҲҶеҲ«еңЁ100 gж°ҙдёӯеҠ е…Ҙ40 g з”ІгҖҒд№ҷпјҢеҠ зғӯеҲ°40в„ғпјҢз”ІгҖҒд№ҷжә¶ж¶ІеқҮдёәйҘұе’Ңжә¶ж¶І
|
|
| 18. | иҜҰз»ҶдҝЎжҒҜ |
|
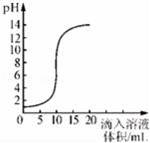
е®Өжё©ж—¶пјҢе°Ҷж°ўж°§еҢ–й’ жә¶ж¶ІдёҺзӣҗй…ёз”Ёж»ҙеҠ ж–№ејҸеҸҚеә”ж—¶пјҢжә¶ж¶Ізҡ„pHйҡҸж»ҙе…Ҙжә¶ж¶ІдҪ“з§ҜеҸҳеҢ–еҰӮеӣҫжүҖзӨәпјҺдёӢеҲ—жңүе…іиҜҙжі•дёҚжӯЈзЎ®зҡ„жҳҜпјҲгҖҖгҖҖпјү
AпјҺиҜҘеӣҫиұЎиЎЁзӨәзҡ„жҳҜе°Ҷж°ўж°§еҢ–й’ жә¶ж¶Іж»ҙе…Ҙзӣҗй…ёдёӯ BпјҺж°ўж°§еҢ–й’ жә¶ж¶Іе’Ңзӣҗй…ёжҒ°еҘҪе®Ңе…ЁеҸҚеә”ж—¶пјҺжә¶ж¶Ізҡ„pHзӯүдәҺ7 CпјҺж»ҙе…Ҙжә¶ж¶ІдҪ“з§Ҝдёә15mLж—¶пјҢеҶҚеҠ еҮ ж»ҙзҙ«иүІзҹіи•ҠиҜ•ж¶Іжә¶ж¶Іе‘Ҳи“қиүІ DпјҺеҪ“ж»ҙе…Ҙжә¶ж¶Ізҡ„дҪ“з§Ҝдёә5mLж—¶пјҢжүҖеҫ—жә¶ж¶Ідёӯзҡ„жә¶иҙЁеҸӘжңүNaCl
|
|
| 19. | иҜҰз»ҶдҝЎжҒҜ |
|
дёӢеҲ—зҰ»еӯҗиғҪеңЁpH=11зҡ„жә¶ж¶ІдёӯеӨ§йҮҸе…ұеӯҳзҡ„жҳҜпјҲгҖҖгҖҖпјү AпјҺK+гҖҒNO3п№ЈгҖҒNa+гҖҒOHп№Ј BпјҺCO32п№ЈгҖҒK+гҖҒClп№ЈгҖҒCa2+ CпјҺH+гҖҒBa2+гҖҒClп№ЈгҖҒSO42п№ЈВ В DпјҺK+гҖҒOHп№ЈгҖҒSO42п№ЈгҖҒCu2+
|
|
| 20. | иҜҰз»ҶдҝЎжҒҜ |
|
еҲқдёӯеҢ–еӯҰзҡ„еҫҲеӨҡеҸҚеә”еҸҜд»ҘиЎЁзӨәдёәпјҡз”І+д№ҷ=дёҷ+дёҒпјҢе…¶дёӯз”ІгҖҒд№ҷгҖҒдёҷгҖҒдёҒж—ўеҸҜиғҪжҳҜеҚ•иҙЁд№ҹеҸҜиғҪжҳҜеҢ–еҗҲзү©пјҺдёӢеҲ—иҜҙжі•дёӯпјҢжӯЈзЎ®зҡ„жҳҜпјҲгҖҖгҖҖпјү AпјҺиӢҘз”ІгҖҒд№ҷгҖҒдёҷгҖҒдёҒеқҮжҳҜеҢ–еҗҲзү©пјҢеҲҷиҜҘеҸҚеә”дёҖе®ҡжҳҜеӨҚеҲҶи§ЈеҸҚеә” BпјҺиӢҘз”ІгҖҒд№ҷгҖҒдёҷеҲҶеҲ«жҳҜй…ёгҖҒзўұгҖҒзӣҗпјҢеҲҷдёҒдёҖе®ҡжҳҜж°ҙ CпјҺиӢҘз”ІжҳҜдёҖж°§еҢ–зўіпјҢд№ҷжҳҜйҮ‘еұһж°§еҢ–зү©пјҢеҲҷдёҷдёҖе®ҡжҳҜдәҢж°§еҢ–зўі DпјҺиӢҘз”ІжҳҜй”ҢпјҢдёҷжҳҜж°ўж°”пјҢеҲҷд№ҷдёҖе®ҡжҳҜзЁҖзЎ«й…ё
|
|
| 21. | иҜҰз»ҶдҝЎжҒҜ |
|
з”ЁеҢ–еӯҰз”ЁиҜӯеЎ«з©ә пјҲ1пјүж ҮеҮәиҝҮж°§еҢ–ж°ўдёӯж°§е…ғзҙ зҡ„еҢ–еҗҲд»·гҖҖ пјҲ2пјүзўҳй…’еңЁеҢ»з–—дёҠеёёз”ЁжқҘж¶ҲзӮҺпјҢе…¶жә¶еүӮжҳҜгҖҖгҖҖ пјҲ3пјүең°еЈідёӯеҗ«йҮҸжңҖеӨҡзҡ„йҮ‘еұһе…ғзҙ е’ҢжңҖеӨҡзҡ„йқһйҮ‘еұһе…ғзҙ з»„жҲҗзҡ„зү©иҙЁгҖҖгҖҖ пјҲ4пјүеҶҷеҮәз¬ҰеҸ·дёӯвҖң2вҖқзҡ„еҗ«д№үпјҡCa2+гҖҖгҖҖ пјҲ5пјүж°ҜеҢ–й“Ғдёӯзҡ„йҳізҰ»еӯҗгҖҖгҖҖпјҺ
|
|
| 22. | иҜҰз»ҶдҝЎжҒҜ |
|
з”ҹжҙ»дёӯи•ҙеҢ–еӯҰпјҢз•ҷеҝғеӨ„зҡҶеӯҰй—®пјҺиҜ·з”ЁдёӢеҲ—еәҸеҸ·еЎ«з©әпјҺ в‘ Na2CO3 в‘ЎCaпјҲOHпјү2 в‘ўHCl в‘ЈNaCl в‘ӨNaOH в‘ҘCaOВ в‘ҰCO ⑧NaHCO3 пјҲ1пјүз”ҹжҙ»дёӯзҡ„и°ғе‘іе“ҒгҖҖгҖҖпјӣпјҲ2пјүз”ЁдәҺж”№иүҜй…ёжҖ§еңҹеЈӨгҖҖгҖҖпјӣ пјҲ3пјүиғғй…ёзҡ„дё»иҰҒжҲҗеҲҶгҖҖгҖҖпјӣпјҲ4пјүдҫҜж°ҸиҒ”еҗҲеҲ¶зўұжі•зҡ„дё»иҰҒдә§е“ҒгҖҖпјҺ пјҲ5пјүе…·жңүиҝҳеҺҹжҖ§зҡ„жңүжҜ’ж°”дҪ“гҖҖгҖҖпјҲ6пјүеҸҜд»ҘжІ»з–—иғғй…ёиҝҮеӨҡз—Үзҡ„зү©иҙЁжҳҜгҖҖгҖҖпјӣ пјҲ7пјүеҸҜдҪңйЈҹе“Ғе№ІзҮҘеүӮзҡ„зү©иҙЁжҳҜгҖҖгҖҖпјӣпјҲ8пјүзӮүе…·жё…жҙҒеүӮдёӯеҗ«жңүзҡ„зү©иҙЁгҖҖгҖҖпјҺ
|
|
| 23. | иҜҰз»ҶдҝЎжҒҜ |
|
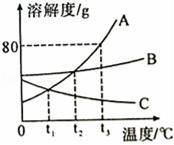
еҰӮеӣҫжҳҜAгҖҒBгҖҒCдёүз§ҚеӣәдҪ“зү©иҙЁзҡ„жә¶и§ЈеәҰжӣІзәҝеӣҫпјҢиҜ·з»“еҗҲеӣҫзӨәеӣһзӯ”дёӢеҲ—й—®йўҳпјҡ пјҲ1пјүt2в„ғж—¶пјҢAгҖҒBгҖҒCдёүз§Қзү©иҙЁзҡ„жә¶и§ЈеәҰеӨ§е°Ҹе…ізі»жҳҜгҖҖгҖҖпјҺ пјҲ2пјүt3в„ғж—¶пјҢе°Ҷ30gAзү©иҙЁеҠ е…ҘеҲ°50gж°ҙдёӯпјҢе……еҲҶжә¶и§ЈеҗҺпјҢжүҖеҫ—жә¶ж¶ІжҳҜгҖҖгҖҖ пјҲеЎ«вҖңйҘұе’ҢвҖқжҲ–вҖңдёҚйҘұе’ҢвҖқпјүжә¶ж¶ІпјҺжүҖеҫ—жә¶ж¶Іжә¶иҙЁиҙЁйҮҸеҲҶж•°дёәгҖҖгҖҖ пјҲ3пјүе®Өжё©дёӢпјҢе°ҶзӣӣжңүAзҡ„йҘұе’Ңжә¶ж¶Ізҡ„иҜ•з®Ўж”ҫе…Ҙзӣӣж°ҙзҡ„зғ§жқҜдёӯпјҢеҶҚеҗ‘зғ§жқҜеҶ…зҡ„ж°ҙдёӯеҠ е…ҘдёҖе®ҡйҮҸзҡ„并NH4NO3并жҗ…жӢҢпјҢиҜ•з®ЎеҶ…еҸҜд»Ҙи§ӮеҜҹеҲ°зҡ„зҺ°иұЎжҳҜгҖҖгҖҖпјҺ пјҲ4пјүе°Ҷt2в„ғж—¶AгҖҒBгҖҒCдёүз§ҚйҘұе’Ңжә¶ж¶ІеҗҢж—¶йҷҚжё©иҮіt1в„ғж—¶пјҢжүҖеҫ—жә¶ж¶Ідёӯжә¶иҙЁзҡ„иҙЁйҮҸеҲҶж•°зҡ„еӨ§е°Ҹе…ізі»жҳҜгҖҖгҖҖпјҺ
|
|
| 24. | иҜҰз»ҶдҝЎжҒҜ | ||||||||||||||||
|
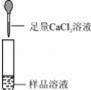
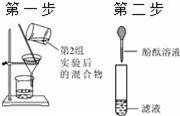
жҹҗеҗҢеӯҰеҸ‘зҺ°пјҢдёҠдёӘжңҲеҒҡе®һйӘҢз”Ёзҡ„NaOHжә¶ж¶Іеҝҳи®°дәҶзӣ–瓶зӣ–пјҺеҜ№дәҺиҜҘжә¶ж¶ІжҳҜеҗҰеҸҳиҙЁпјҢеҗҢеӯҰ们ејҖе§Ӣе®һйӘҢжҺўз©¶е№¶и®ҫи®ЎеҰӮдёӢе®һйӘҢпјҺиҜ·дҪ е°Ҷе®һйӘҢи®ҫи®ЎиЎҘе……е®Ңж•ҙпјҺ гҖҗзҢңжғіеҒҮи®ҫгҖ‘ зҢңжғіпјҲ1пјүпјҡиҜҘжә¶ж¶ІжІЎжңүеҸҳиҙЁпјҢдёәNaOHжә¶ж¶ІпјҺ зҢңжғіпјҲ2пјүпјҡиҜҘжә¶ж¶Іе…ЁйғЁеҸҳиҙЁпјҢдёәгҖҖжә¶ж¶ІпјҺ зҢңжғіпјҲ3пјүпјҡиҜҘжә¶ж¶ІйғЁеҲҶеҸҳиҙЁпјҢдёәNaOHе’ҢNa2CO3зҡ„ж··еҗҲжә¶ж¶ІпјҺ гҖҗжҹҘйҳ…иө„ж–ҷгҖ‘Na2CO3жә¶ж¶Іе‘ҲзўұжҖ§пјҢж°ҜеҢ–й’ҷжә¶ж¶Іе‘ҲдёӯжҖ§пјҺ гҖҗи®ҫи®Ўж–№жЎҲгҖ‘иҜ·дҪ е®Ңе–„дёӢиЎЁеҮ з»„еҗҢеӯҰжҺўи®Ёзҡ„и®ҫи®Ўж–№жЎҲ
гҖҗжҺўз©¶е®һйӘҢгҖ‘з»јеҗҲеҗ„е°Ҹз»„зҡ„ж–№жЎҲеҗҺпјҢеҠЁжүӢе®һйӘҢпјҺ гҖҗз»“и®әдёҺеҸҚжҖқгҖ‘NaOHжә¶ж¶Іжҳ“дёҺз©әж°”дёӯCO2еҸҚеә”иҖҢеҸҳиҙЁпјҢжүҖд»ҘиҰҒеҜҶе°ҒдҝқеӯҳпјҺ гҖҗжӢ“еұ•е»¶дјёгҖ‘еҗҢеӯҰ们и®ҫи®ЎдәҶдёӢеҲ—дёӨеҘ—иЈ…зҪ®иҝӣиЎҢе®һйӘҢпјҡ
з”Ёиғ¶еӨҙж»ҙз®ЎеҗёеҸ–жҹҗз§Қж¶ІдҪ“пјҢй”ҘеҪўз“¶дёӯе……е…ҘдёҖз§Қж°”дҪ“жҲ–ж”ҫе…ҘдёҖз§ҚеӣәдҪ“зү©иҙЁпјҢжҢӨеҺӢиғ¶еӨҙж»ҙз®ЎпјҺдёҖж®өж—¶й—ҙеҗҺпјҢдёӨиЈ…зҪ®дёӯж°”зҗғжҳҺжҳҫиғҖеӨ§пјҺ пјҲ1пјүз”ІиЈ…зҪ®дёӯеҸҜиғҪеҸ‘з”ҹеҸҚеә”зҡ„ж–№зЁӢејҸжҳҜгҖҖпјҲ2пјүиӢҘд№ҷиЈ…зҪ®дёӯиғ¶еӨҙж»ҙз®ЎеҗёеҸ–зҡ„жҳҜзЁҖзӣҗй…ёпјҢеҲҷй”ҘеҪўз“¶дёӯж”ҫе…Ҙзҡ„еӣәдҪ“еҸҜиғҪжҳҜгҖҖгҖҖпјҺ
|
|||||||||||||||||
| 25. | иҜҰз»ҶдҝЎжҒҜ |
|
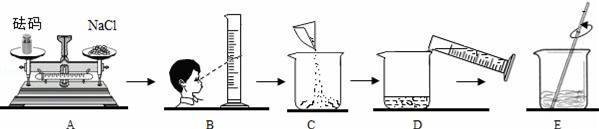
еҗҢеӯҰиҰҒеңЁе®һйӘҢе®Өй…ҚеҲ¶15%зҡ„ж°ҜеҢ–й’ жә¶ж¶І50gпјҺиҜҘеҗҢеӯҰжҢүдёӢеӣҫжүҖзӨәжӯҘйӘӨдҫқж¬Ўж“ҚдҪңпјҡиҜ·еӣһзӯ”дёӢеҲ—й—®йўҳпјҡ
пјҲ1пјүиӢҘз”Ёж°ҜеҢ–й’ еӣәдҪ“й…ҚеҲ¶пјҢйңҖз§°еҸ–ж°ҜеҢ–й’ гҖҖгҖҖgпјҺ пјҲ2пјүе…¶дёӯж“ҚдҪңй”ҷиҜҜзҡ„жӯҘйӘӨжҳҜгҖҖгҖҖпјҲеЎ«еӯ—жҜҚпјүпјӣ пјҲ3пјүEдёӯзҺ»з’ғжЈ’зҡ„дҪңз”ЁжҳҜгҖҖ пјҲ4пјүиӢҘдёҠеӣҫAдёӯз қз Ғзҡ„иҙЁйҮҸдёә5gпјҢжёёз Ғдёә2.5gпјҢеҲҷе°ҸжҳҺз§°еҫ—зҡ„ж°ҜеҢ–й’ иҙЁйҮҸе®һйҷ…дёәгҖҖg пјҲ5пјүиӢҘдёҠеӣҫдёӯAжӯҘйӘӨж“ҚдҪңжӯЈзЎ®пјҢжүҖз§°ж°ҜеҢ–й’ иҙЁйҮҸеҮҶзЎ®пјҢиҖҢж“ҚдҪңBдјҡеҜјиҮҙжүҖеҫ—жә¶ж¶Іжә¶иҙЁиҙЁйҮҸеҲҶж•°гҖҖгҖҖ15%пјҲеЎ«вҖңеӨ§дәҺвҖқвҖңе°ҸдәҺвҖқжҲ–вҖңзӯүдәҺвҖқпјү пјҲ6пјүиӢҘз”Ё30%зҡ„ж°ҜеҢ–й’ жә¶ж¶Ій…ҚеҲ¶пјҢйңҖ30%зҡ„ж°ҜеҢ–й’ жә¶ж¶ІгҖҖгҖҖgпјӣи’ёйҰҸж°ҙгҖҖгҖҖgпјҺ
|
|
| 26. | иҜҰз»ҶдҝЎжҒҜ |
|
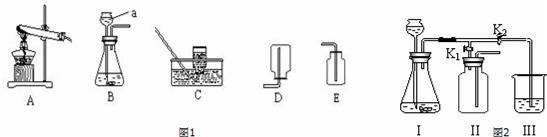
жҹҗж ЎеҢ–еӯҰз ”з©¶жҖ§еӯҰд№ е°Ҹз»„е…ұеҗҢжҺўз©¶еҲ¶еҸ–ж°”дҪ“зҡ„еҺҹзҗҶгҖҒж–№жі•еҸҠжҖ§иҙЁзҡ„жңүе…іе®һйӘҢпјҺ пјҲ1пјүз”ІеҗҢеӯҰе°ҶжүҖеӯҰж°”дҪ“еҲ¶еҸ–зҡ„зҹҘиҜҶж•ҙзҗҶеҰӮдёӢпјҢиҜ·дҪ её®еҠ©д»–е®ҢжҲҗзӣёе…іеҶ…е®№пјҺ
в‘ еҶҷеҮәеӣҫдёӯжңүж ҮеҸ·д»ӘеҷЁзҡ„еҗҚaгҖҖгҖҖпјҺ в‘Ўз”ЁеҸҢж°§ж°ҙе’ҢдәҢж°§еҢ–й”°жқҘеҲ¶еҸ–ж°§ж°”ж—¶пјҢеҸҜйҖүз”Ёзҡ„еҸ‘з”ҹиЈ…зҪ®жҳҜгҖҖгҖҖ пјҲеЎ«еәҸеҸ·пјҢдёӢеҗҢпјүпјҺ в‘ўеҸҚеә”з»“жқҹеҗҺпјҢж¬Іе°ҶдәҢж°§еҢ–й”°еӣһ收еҶҚеҲ©з”Ёеә”иҝӣиЎҢзҡ„дё»иҰҒж“ҚдҪңжҳҜгҖҖгҖҖпјҺ в‘Је®һйӘҢе®Өеёёз”Ёж°ҜеҢ–й“өеӣәдҪ“дёҺзўұзҹізҒ°еӣәдҪ“е…ұзғӯжқҘеҲ¶еҸ–ж°Ёж°”пјҲNH3пјүпјҢеә”йҖүжӢ©зҡ„еҸ‘з”ҹиЈ…зҪ®жҳҜгҖҖгҖҖпјҺ пјҲ2пјүд№ҷеҗҢеӯҰи®ҫи®Ўзҡ„е®һйӘҢиЈ…зҪ®пјҲеҰӮеӣҫ2пјүпјҢж—ўеҸҜз”ЁдәҺеҲ¶еҸ–ж°”дҪ“пјҢеҸҲеҸҜз”ЁдәҺжҺўз©¶зү©иҙЁжҖ§иҙЁпјҺ в‘ еҪ“жү“ејҖK1гҖҒе…ій—ӯK2ж—¶пјҢеҲ©з”ЁIгҖҒв…ЎиЈ…зҪ®еҸҜиҝӣиЎҢзҡ„е®һйӘҢжҳҜгҖҖгҖҖ пјҲеЎ«еәҸеҸ·пјүпјҺ aпјҺеӨ§зҗҶзҹідёҺзЁҖзӣҗй…ёеҸҚеә”еҲ¶еҸ–дәҢж°§еҢ–зўіbпјҺй”ҢдёҺзЁҖзЎ«й…ёеҸҚеә”еҲ¶еҸ–ж°ўж°” в‘ЎеҪ“жү“ејҖK2гҖҒе…ій—ӯK1пјҢеҲ©з”ЁIгҖҒв…ўиЈ…зҪ®еҸҜд»ҘжЈҖйӘҢз”ҹжҲҗзҡ„дәҢж°§еҢ–зўіпјҢеҲҷиЈ…зҪ®IдёӯеҸ‘з”ҹеҸҚеә”зҡ„еҢ–еӯҰж–№зЁӢејҸдёәгҖҖгҖҖпјӣиӢҘиҰҒиҜҒжҳҺдәҢж°§еҢ–зўідёҺж°ҙеҸ‘з”ҹеҸҚеә”пјҢзғ§жқҜдёӯеә”ж”ҫе…Ҙзҡ„иҜ•еүӮжҳҜгҖҖгҖҖпјҺ
|
|
| 27. | иҜҰз»ҶдҝЎжҒҜ |
|
AдёҺBжңүеҰӮдёӢзҡ„еҸҚеә”пјҡA+BвҶ’C+DпјҺ пјҲ1пјүиӢҘCдёәеҺЁжҲҝеҶ…еёёз”Ёзҡ„и°ғе‘іе“ҒпјӣеңЁAжә¶ж¶ІдёӯеҠ е…Ҙй“ҒзІүиғҪдә§з”ҹж°ўж°”пјҢеҲҷAжҳҜгҖҖгҖҖпјҺиӢҘAгҖҒBдёӨжә¶ж¶ІжҒ°еҘҪеҸҚеә”е®Ңе…ЁпјҢеҲҷеҸҚеә”еҗҺжә¶ж¶Ізҡ„pHгҖҖгҖҖ7пјҲеЎ«вҖңпјңвҖқгҖҒвҖңпјһвҖқжҲ–вҖң=вҖқпјүпјӣеҶҷеҮәAгҖҒBдёӨжә¶ж¶ІеҸҚеә”зҡ„еҢ–еӯҰж–№зЁӢејҸгҖҖпјҺ пјҲ2пјүиӢҘBеёёз”ЁжқҘж”№иүҜй…ёжҖ§еңҹеЈӨпјҢDжҳҜйҮҚиҰҒзҡ„еҢ–е·ҘеҺҹж–ҷдё”дёҺBзҡ„зұ»еҲ«зӣёеҗҢпјӣBдёҺCO2еҸҚеә”д№ҹиғҪз”ҹжҲҗCпјӣеҲҷAдёәгҖҖгҖҖпјҢCдёәгҖҖгҖҖпјҺеҶҷеҮәBзү©иҙЁзҡ„жә¶ж¶ІдёҺCO2еҸҚеә”зҡ„еҢ–еӯҰж–№зЁӢејҸгҖҖпјҺ
|
|
| 28. | иҜҰз»ҶдҝЎжҒҜ |
|
100gжҹҗзЎ«й…ёжҒ°еҘҪдёҺ13gй”Ңе®Ңе…Ёиө·еҸҚеә”пјҢиҜ•и®Ўз®—пјҡ пјҲ1пјүз”ҹжҲҗж°ўж°”зҡ„иҙЁйҮҸпјӣ пјҲ2пјүиҜҘзЎ«й…ёдёӯжә¶иҙЁзҡ„иҙЁйҮҸеҲҶж•°пјӣ пјҲ3пјүеҸҚеә”еҗҺжүҖеҫ—жә¶ж¶Ідёӯжә¶иҙЁзҡ„иҙЁйҮҸеҲҶж•°пјҲдҝқз•ҷеҲ°0.1%пјүпјҺ
|
|
- ж·ұеңіеёӮд№қе№ҙзә§еҢ–еӯҰжңҲиҖғжөӢйӘҢпјҲ2018е№ҙеүҚеҚҠжңҹпјүзҪ‘з»ңиҖғиҜ•иҜ•еҚ·
- йҷ•иҘҝзңҒжёӯеҚ—еёӮйҹ©еҹҺеёӮ2020-2021е№ҙеҲқдёүдёҠеҶҢжңҹжң«еҢ–еӯҰдё“йўҳи®ӯз»ғ
- 2018-2019е№ҙеҲқдёүдёҠеӯҰжңҹ12жңҲи°ғз ”еҢ–еӯҰиҖғйўҳпјҲеұұиҘҝзңҒеӨӘеҺҹеёӮеҝ—иҫҫдёӯеӯҰпјү
- 2017е№ҙ6жңҲе№ҝдёңзңҒдёӯиҖғдёҖжЁЎеҢ–еӯҰиҖғйўҳеҗҢжӯҘи®ӯз»ғ
- д№қе№ҙзә§еҢ–еӯҰпјҲ2020е№ҙдёӢеӯҰжңҹпјүе®Ңж•ҙиҜ•еҚ·
- еҚ—е……еёӮ2017е№ҙд№қе№ҙзә§еҢ–еӯҰдёҠеҶҢжңҲиҖғжөӢйӘҢиҜ•еҚ·е®Ңж•ҙзүҲ
- еҲқдёүдёӢеҶҢж•ҲжһңжөӢиҜ•дә”еҢ–еӯҰе…Қиҙ№иҜ•йўҳеёҰзӯ”жЎҲе’Ңи§ЈжһҗпјҲ2019-2020е№ҙжұҹиӢҸзңҒж— й”ЎеёӮеүҚжҙІдёӯеӯҰпјү
- дёӯиҖғйўҳеҺҹеҲӣпјҡжһңжһңе®ўдёІвҖңе°Ҹе°ҸеҢ–еӯҰ家вҖқ