河北省实验中学2020-2021学年高三上学期化学期中考试试卷
河北省实验中学2020-2021学年高三上学期化学期中考试试卷
教材版本:化学
试卷分类:化学高三上学期
试卷大小:1.0 MB
文件类型:.doc 或 .pdf 或 .zip
发布时间:2024-05-01
授权方式:免费下载
下载地址:点此下载
教材版本:化学
试卷分类:化学高三上学期
试卷大小:1.0 MB
文件类型:.doc 或 .pdf 或 .zip
发布时间:2024-05-01
授权方式:免费下载
下载地址:点此下载
以下为试卷部分试题预览
| 1. 单选题 | |
|
用下列装置完成相关实验,合理的是( )
A . 图①:验证H2CO3的酸性强于H2SiO3
B . 图②:收集CO2或NH3
C . 图③:分离Na2CO3溶液与CH3COOC2H5
D . 图④:分离CH3CH2OH与CH3COOC2H5
|
|
| 2. 单选题 | |||||||||||||
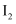 在KI溶液中存在平衡 在KI溶液中存在平衡  ,测得不同温度下该反应的平衡常数如表所示: ,测得不同温度下该反应的平衡常数如表所示:
下列说法正确的是( )
A . 反应
 的 的  B . 利用该反应可以除去硫粉中少量的碘单质
C . 在上述体系中加入苯,平衡不移动
D . 25℃时,向溶液中加入少量KI固体,平衡常数K小于680
B . 利用该反应可以除去硫粉中少量的碘单质
C . 在上述体系中加入苯,平衡不移动
D . 25℃时,向溶液中加入少量KI固体,平衡常数K小于680
|
|||||||||||||
| 3. 单选题 | |
|
宋代张杲《医说》引《集验方》载:每每外出,用雄黄桐子大,在火中烧烟薰脚绷、草履、领袖间,以消毒灭菌,防止疫菌通过衣物的接触而传染。雄黄的结构如图所示,下列说法错误的是( )。
A . 雄黄中硫的价态为-2价
B . 古代熏蒸的消毒原理与H2O2、酒精相同
C . 佩戴药剂香囊是中医独特的防疫措施
D . 生活中也可使用火、盐水消毒器具
|
|
| 4. 单选题 | |
|
根据vt图分析外界条件改变对可逆反应A(g)+3B(g)
可见在t1、t3、t5、t7时反应都达到平衡,如果t2、t4、t6、t8时都只改变了一个反应条件,则下列对t2、t4、t6、t8时改变条件的判断正确的是( )
A . 使用了催化剂、增大压强、减小反应物浓度、降低温度
B . 升高温度、减小压强、减小反应物浓度、使用了催化剂
C . 增大反应物浓度、使用了催化剂、减小压强、升高温度
D . 升高温度、减小压强、增大反应物浓度、使用了催化剂
|
|
| 5. 单选题 | ||||||||||||||||
|
为增强铝的耐腐蚀性,现以铅蓄电池为外电源,以Al作阳极、Pb作阴极,电解稀硫酸,使铝表面的氧化膜增厚。其反应原理如下:
电池:Pb(s) + PbO2(s) + 2H2SO4(aq) = 2PbSO4(s) + 2H2O(l) 电解池:2Al + 3H2O = Al2O3 + 3H2↑ 对该电解过程,以下判断正确的是( )
A . A
B . B
C . C
D . D
|
||||||||||||||||
| 6. 单选题 | |
|
利用太阳能电解水制H2是解决能源危机的重要方向。采用固体氧化还原调节剂作为离子交换体系,实现H2、O2分离。下列分析正确的是( )
A . 左侧电解池应选用酸性溶液,a极反应式为:2H+ + 2e-=H2↑
B . b极反应式:NiOOH + H2O + e-=Ni(OH)2 + OH-
C . c为阳极,发生氧化反应
D . 电解一段时间后,可将b、c对调,循环利用物质
|
|
| 7. 单选题 | |
|
短周期主族元素X、Y、Z、W、Q原子序数依次增大,Y元素最外层电子数是其电子层数的3倍,Q与Y同主族,X与Y构成的化合物可引起光化学烟雾,Z、W、Q的最高价氧化物的水化物两两之间均能发生反应。下列说法正确的是( )
A . 简单氢化物的沸点:Y < Q
B . 气态氢化物的稳定性:Y < X
C . 简单离子半径最大的为Z
D . W的氧化物可作耐高温材料
|
|
| 8. 单选题 | ||||||||||||||||
|
下列实验方案不能达到相应实验目的的是( )
A . A
B . B
C . C
D . D
|
||||||||||||||||
| 9. 单选题 | |
|
Na2CO3(aq)与盐酸反应过程中的能量变化示意图如图,下列选项正确的是( )
A . H2CO3(aq)=CO2(g)+H2O(l)为放热反应
B . CO
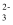 (aq)+H+(aq)=HCO (aq)+H+(aq)=HCO  (aq)∆H=a kJ·mol-1
C . HCO (aq)∆H=a kJ·mol-1
C . HCO  (aq)+H+(aq)=CO2(g)+H2O (l)∆H=(c-b) kJ·mol-1
D . CO (aq)+H+(aq)=CO2(g)+H2O (l)∆H=(c-b) kJ·mol-1
D . CO 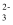 (aq)+2H+(aq)=CO2(g)+H2O(l)∆H=(a+b-c) kJ·mol-1 (aq)+2H+(aq)=CO2(g)+H2O(l)∆H=(a+b-c) kJ·mol-1
|
|
| 10. 单选题 | |
|
用如图装置探究Cl2和NO2在NaOH溶液中的反应。通入适当比例的Cl2和NO2 , 发生的化学反应为Cl2+2NO2+4NaOH=2NaNO3+2NaCl+2H2O。下列叙述正确的是( )
A . 实验室中可用Cu与1mol·L-1的硝酸制备二氧化氮气体
B . 装置II中的玻璃管起到平衡气压作用,可将多余气体直接排出
C . 由该反应可知氧化性顺序:NO2>NaNO3
D . 通过观察装置I、III中的气泡的快慢控制Cl2和NO2的通入量
|
|
最近更新









