2017年高考化学备考复习专题十一:水溶液中的离子平衡
教材版本:化学
试卷分类:化学高考
试卷大小:1.0 MB
文件类型:.doc 或 .pdf 或 .zip
发布时间:2024-05-01
授权方式:免费下载
下载地址:点此下载
以下为试卷部分试题预览
| 1. 单选题 | |
|
室温下向10mL0.1 mol·L-1NaOH溶液中加入0.1 mol·L-1的一元酸HA溶液pH的变化曲线如图所示。下列说法正确的是( )
A . a点所示溶液中c(Na+)>c(A-)>c(H+)>c(HA)
B . a、b两点所示溶液中水的电离程度相同
C . pH=7时,c(Na+)= c(A-)+ c(HA
D . b点所示溶液中c(A-)> c(HA)
|
|
| 2. 单选题 | |
|
25℃时,向纯水中加入NaOH,使溶液的pH为11,则由NaOH电离出的OH﹣离子浓度为( )mol•L﹣1 .
A . 10﹣3
B . 10﹣11
C . 10﹣14
D . 无法确定
|
|
| 3. 填空题 | |
|
25℃时,0.1mol•L﹣1的HA溶液中c(H+)/c(OH﹣)=1010 . 请回答下列问题:
①HA是 (填“强电解质”或“弱电解质”); ②在加水稀释HA溶液的过程中,随着水量的增加而减小的是 (填字母). A.c(H+)/c(HA) B.c(HA)/(A﹣) C.c(H+)与c(OH﹣)的乘积 D.c(OH﹣) ③若M溶液是由上述HA溶液V1mL与pH=12的NaOH溶液V2mL混合充分反应而得,则下列说法中正确的是 A.若溶液M呈中性,则溶液M中c(H+)+c(OH﹣)=2.0×10﹣7 mol•L﹣1 B.若V1=V2 , 则溶液M的pH一定等于7 C.若溶液M呈酸性,V1一定大于V2 D.若溶液M呈碱性,V1一定小于V2 . |
|
| 4. 填空题 | |
|
25℃,将0.4mol/L CH3COOH 溶液和 0.2mol/L NaOH 溶液各 100mL 混合后,pH=5,(设混合后溶液总体积为两溶液体积之和)
(1)混合溶液中离子浓度由大到小的顺序是 (2)①c(CH3COO﹣)+c(CH3COOH)= mol/L②c(CH3COO﹣)﹣c(CH3COOH)= mol/L. |
|
| 5. 单选题 | |
|
苯甲酸钠(
A . 相比于未充CO2的饮料,碳酸饮料的抑菌能力较低
B . 提高CO2充气压力,饮料中c(A﹣)不变
C . 当pH为5.0时,饮料中
 =0.16
D . 碳酸饮料中各种粒子的浓度关系为:c(H+)=c(HCO3﹣)+c(CO32﹣)+c(OH﹣)﹣c(HA) =0.16
D . 碳酸饮料中各种粒子的浓度关系为:c(H+)=c(HCO3﹣)+c(CO32﹣)+c(OH﹣)﹣c(HA)
|
|
| 6. 单选题 | |
|
在两份相同的Ba(OH)2溶液中,分别滴入物质的量浓度相等的H2SO4、NaHSO4溶液,其导电能力随滴入溶液体积变化的曲线如图所示.下列分析不正确的是( )
A . ①代表滴加H2SO4溶液的变化曲线
B . b点,溶液中大量存在的离子是Na+、OH﹣
C . c点,两溶液中含有相同量的OH﹣
D . a、d两点对应的溶液均显中性
|
|
| 7. 单选题 | |
|
下列有关电解质溶液的说法正确的是( )
A . 向0.1mol•L﹣1 CH3COOH溶液中加入少量水,溶液中
 减小
B . 将CH3COONa溶液从20℃升温至30℃,溶液中 减小
B . 将CH3COONa溶液从20℃升温至30℃,溶液中  增大
C . 向盐酸中加入氨水至中性,溶液中 增大
C . 向盐酸中加入氨水至中性,溶液中  >1
D . 向AgCl、AgBr的饱和溶液中加入少量AgNO3 , 溶液中 >1
D . 向AgCl、AgBr的饱和溶液中加入少量AgNO3 , 溶液中  不变 不变
|
|
| 8. 单选题 | |
|
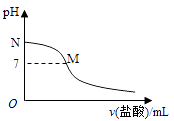
298K时,在20.0mL 0.10mol•L﹣1氨水中滴入0.10mol•L﹣1的盐酸,溶液的pH与所加盐酸的体积关系如图所示.已知0.10mol•L﹣1氨水的电离度为1.32%,下列有关叙述正确的是( )
A . 该滴定过程应该选择酚酞作为指示剂
B . M点对应的盐酸体积为20.0mL
C . M点处的溶液中c(NH4+)=c(Cl﹣)=c(H+)=c(OH﹣)
D . N点处的溶液中pH<12
|
|
| 9. 单选题 | |
|
下列图示与对应的叙述不相符合的是( )
A . 图甲表示燃料燃烧反应的能量变化
B . 图乙表示酶催化反应的反应速率随反应温度的变化
C . 图丙表示弱电解质在水中建立电离平衡的过程
D . 图丁表示强碱滴定强酸的滴定曲线
|
|
| 10. 综合题 | ||||||||||||||||||||||||
|
随着科学技术的发展和环保要求的不断提高,CO2的捕集利用技术成为研究的重点.
完成下列填空:
|
||||||||||||||||||||||||
- 吉林省白山市2020-2021学年高一下学期期末考试化学试题
- 河南省南阳市2020-2021学年高三上学期化学期中考试试卷
- 陕西省渭南市富平县2020-2021学年高一下学期期末考试化学试题
- 江苏省苏州市吴江区2020-2021学年高二上学期化学期中考试试卷
- 福建省泉州市2021-2022学年高三上学期化学开学考试试卷
- 广西梧州市2021年高考理综-化学3月模拟试卷
- 陕西省汉中市2021-2022学年高一下学期期中考试化学试题
- 上海市黄浦区2021年高考化学二模试卷
- 冲刺2021高考化学押题训练(七)电化学及其应用
- 黑龙江省西北部八校2021-2022学年高一下学期期中联考化学试题
- 广西柳州市2021年高考化学三模试卷
- 天津市南开区2022届高三模拟考试(二模)化学试题

 ,缩写为NaA)可用作饮料的防腐剂,研究表明苯甲酸(HA)的抑菌能力显著高于A﹣ , 已知25℃时,HA的Ka=6.25×10﹣5 , H2CO3的Ka1=4.17×10﹣7 , Ka2=4.90×10﹣11 , 在生产碳酸饮料的过程中,除了添加NaA外,还需加压冲入CO2气体,下列说法正确的是(温度为25℃,不考虑饮料中其他成分)( )
,缩写为NaA)可用作饮料的防腐剂,研究表明苯甲酸(HA)的抑菌能力显著高于A﹣ , 已知25℃时,HA的Ka=6.25×10﹣5 , H2CO3的Ka1=4.17×10﹣7 , Ka2=4.90×10﹣11 , 在生产碳酸饮料的过程中,除了添加NaA外,还需加压冲入CO2气体,下列说法正确的是(温度为25℃,不考虑饮料中其他成分)( )