人教版化学高二选修4第四章第三节电解池同步练习
人教版化学高二选修4第四章第三节电解池同步练习
教材版本:化学
试卷分类:化学高二上学期
试卷大小:1.0 MB
文件类型:.doc 或 .pdf 或 .zip
发布时间:2024-05-01
授权方式:免费下载
下载地址:点此下载
教材版本:化学
试卷分类:化学高二上学期
试卷大小:1.0 MB
文件类型:.doc 或 .pdf 或 .zip
发布时间:2024-05-01
授权方式:免费下载
下载地址:点此下载
以下为试卷部分试题预览
| 1. 单选题 | |
|
银制器皿日久表面会逐渐变黑,这是生成了Ag2S的缘所以.根据电化学原理可进行如下处理:在铝质容器中加入食盐溶液,再将变黑的银器浸入该溶液中,一段时间后发现黑色会褪去.下列说法正确的是( )
A . 处理过程中银器一直保持恒重
B . 银器为正极,Ag2S被还原生成单质银
C . 该过程中总反应为2Al+3Ag2S═6Ag+Al2S3
D . 黑色褪去的原因是黑色Ag2S转化为白色AgCl
|
|
| 2. 单选题 | |
|
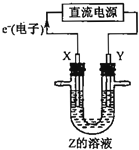
利用如图所示装置,当X、Y选用不同材料时,可将电解原理广泛应用于工业生产.下列说法中正确的是( )
A . 氯碱工业,若X、Y均为石墨,Y附近能得到氯气
B . 铜的精炼中,X是纯铜,Y是粗铜,Z是CuSO4
C . 外加电流的阴极保护法中,Y是待保护金属
D . 电镀工业中,X是待镀金属,Y是镀层金属
|
|
| 3. 单选题 | |
|
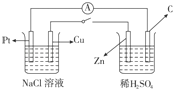
如图,将两烧杯用导线相连,Pt、Cu、Zn、C分别为四个电极,当闭合开关后,以下叙述正确的是( )
A . Cu极附近OH﹣浓度增大
B . Cu极为原电池负极
C . 电子流向是由C极流向Pt极
D . 当C极上有4mol电子转移时,Pt极上有1mol O2生成
|
|
| 4. 单选题 | |
|
下列关于电解池的叙述中不正确的是( )
A . 与电源正极相连的是电解池的阴极
B . 与电源负极相连的是电解池的阴极
C . 在电解池的阳极发生氧化反应
D . 电子从电源的负极沿导线流入电解池的阴极
|
|
| 5. 单选题 | |
|
下列过程需要通电才能进行的是( )
①电离 ②电解 ③电镀 ④电化学腐蚀.
A . ①②
B . ②③
C . ②④
D . 全部
|
|
| 6. 单选题 | |
|
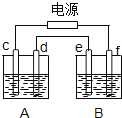
如图,A池用石墨电极电解NaOH溶液,B池精炼粗铜,一段时间后停止通电,A池中d极产生具有氧化性的气体在标准状况下为2.24L.下列说法正确的是( )
A . A池为电解池,B池为原电池
B . d、e两极都发生氧化反应
C . e极应为粗铜板材料
D . B池中e极质量增加12.8g
|
|
| 7. 单选题 | |
|
下列叙述中,正确的是( )
①电解池是将化学能转变成电能的装置 ②原电池是将电能转变成化学能的装置 ③金属和石墨导电均为物理变化,电解质溶液导电是化学变化 ④不能自发进行的氧化还原反应,通过电解的原理有可能实现 ⑤电镀过程相当于金属的“迁移”,可视为物理变化.
A . ①②③④
B . ③④
C . ③④⑤
D . ④
|
|
| 8. 单选题 | |
|
下列关于铜电极的叙述正确的是( )
A . 铜一锌原电池中,铜是负极
B . 用电解法精炼粗铜时,粗铜作阴极
C . 在镀件上电镀铜时,用金属铜作阳极
D . 电解稀硫酸制H2、O2时,铜作阳极
|
|
| 9. 单选题 | |
|
如图所示,按如图甲装置进行实验,若图乙的x轴表示流入电极的电子的量,则y轴不可能表示的是( )
A . c(Ag+)
B . c(NO3﹣)
C . 溶液的pH
D . 铁片质量
|
|
| 10. 单选题 | |
|
某同学按如图所示的装置进行电解实验.下列说法不正确的是( )
A . 电解过程中,铜电极上有H2产生
B . 电解初期,总反应方程式为 Cu+H2SO4
 CuSO4+H2↑
C . 电解一定时间后,石墨电极上有铜析出
D . 整个电解过程中,H+的浓度不断减小 CuSO4+H2↑
C . 电解一定时间后,石墨电极上有铜析出
D . 整个电解过程中,H+的浓度不断减小
|
|
高中化学 试卷推荐
- 2016-2017学年海南省国科园实验学校高一上学期期中化学试卷
- 2016-2017学年湖南省株洲市茶陵三中高二上学期开学化学试卷
- 云南省保山市2018-2019学年高考理综-化学检测考试试卷
- 天津市耀华中学2019-2020学年高三下学期化2月月考试卷
- 山西省运城市芮城县2019-2020学年高二下学期化学期末考试试卷
- 吉林省四平市双辽市第二中学2019-2020学年高二上学期化学期末考试试卷
- 江西省宜春市2018-2019学年高三上学期化学期末考试试卷
- 浙江省名校协作体(G12)2018-2019学年高二下学期化学期末考试试卷
- 四川成都田家炳中学2018-2019学年高一上学期化学12月月考试卷
- 2017年高考理综真题试卷(化学部分)(北京卷)(正式版)
- 2019年高考理综化学真题试卷(北京卷)
- 山东省临沂市2016-2017学年高一上学期化学期末考试试卷
最近更新