高中化学人教版(2019)选择性必修1第三章第二节水的电离和溶液pH
高中化学人教版(2019)选择性必修1第三章第二节水的电离和溶液pH
教材版本:化学
试卷分类:化学高二上学期
试卷大小:1.0 MB
文件类型:.doc 或 .pdf 或 .zip
发布时间:2024-05-01
授权方式:免费下载
下载地址:点此下载
教材版本:化学
试卷分类:化学高二上学期
试卷大小:1.0 MB
文件类型:.doc 或 .pdf 或 .zip
发布时间:2024-05-01
授权方式:免费下载
下载地址:点此下载
以下为试卷部分试题预览
| 1. 填空题 | |
|
现有下列物质:①100 ℃纯水;②25 ℃ 0.1 mol·L-1HCl溶液;③25 ℃ 0.1 mol·L-1KOH溶液;④25 ℃ 0.1 mol·L-1Ba(OH)2溶液。
|
|
| 2. 填空题 | |
|
18℃时,H2A(酸):K1=4.3×10-7 , K2=2.1×10-12;H2B(酸):K1=1.0×10-7 , K2=6.3×10-13;在浓度相同的两种溶液中,用“>”、“<”或“=”填空。
|
|
| 3. 多选题 | |
|
一定温度下,水存在如下电离:H2O
A . 向水中滴入少量稀盐酸,平衡逆向移动,Kw减小
B . 将水加热,Kw增大,pH减小
C . 向水中加入少量固体NH4Cl,平衡逆向移动,c(H+)降低
D . 向水中加入少量固体硫酸钠,c(H+)=10-7mol/L,Kw不变
|
|
| 4. 多选题 | |
|
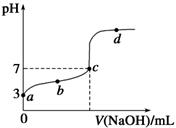
已知某温度时CH3COOH 的电离平衡常数为K , 该温度下向 20mL 0.1mol·L-1 CH3COOH 溶液中逐滴加入0.1mol·L-1NaOH 溶液,其pH变化曲线如图所示(忽略温度变化)。下列说法中错误的是( )
A . a 点表示溶液中c(CH3COO-)=10-3 mol·L-1
B . b 点表示的溶液中c(CH3COO-)>c(Na+)
C . c点表示CH3COOH和NaOH恰好反应完全
D . b、d 点表示的溶液中
 均等于K 均等于K
|
|
| 5. 填空题 | |
|
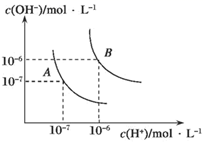
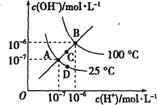
水的电离平衡曲线如图所示,若A点表示25℃时水的电离达平衡时的离子浓度,B点表示100℃时水的电离达平衡时的离子浓度。则100℃时0.001 mol/L的NaOH溶液中,由水电离出的c(H+)=mol·L-1 , Kw(25℃)Kw(100℃)(填“>”、“<”或“=”)。25℃时,向水的电离平衡体系中加入少量NH4HCO3固体,对水的电离平衡的影响是(填“促进”、“抑制”或“不影响”)。
|
|
| 6. 综合题 | |
|
设水的电离平衡线如图所示。
|
|
| 7. 多选题 | |
|
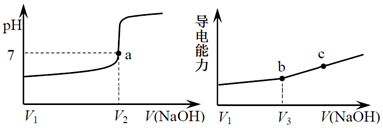
用一定浓度NaOH溶液滴定某一元酸HA溶液。滴定终点附近溶液pH和导电能力的变化分别如图所示。下列说法正确的是( )
A . HA为一元弱酸
B . b点对应的溶液中:c(A-)>c(Na+)
C . 根据溶液pH和导电能力的变化可判断V2<V3
D . a、b、c三点对应的溶液中水的电离程度依次减小
|
|
| 8. 单选题 | |
|
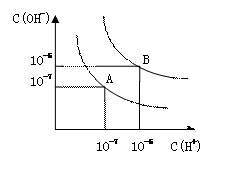
水的电离平衡曲线如图所示,下列说法错误的是( )
A . 图中四点Kw间的关系:A=D<C<B
B . 若从A点到D点,可采用:温度不变在水中加入少量酸
C . 若从A点到C点,可采用:温度不变在水中加入少量NH4Cl固体
D . 若从A点到D点,可采用:温度不变在水中加入少量NH4Cl固体
|
|
| 9. 单选题 | |
|
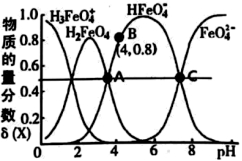
高铁酸钾(K2FeO4)是一种高效多功能的新型非氯绿色消毒剂,主要用于饮水处理。常温下,调节其水溶液pH时,含铁粒子的物质的量分数δ(X)随pH的变化如图所示[已知
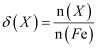 ]。 ]。 下列说法正确的是( )
A . 25℃,B点水的电离出的c(H+)=1×10−4
B . NaHFeO4溶液显碱性
C . 常温下,H2FeO4(aq)+H+(aq)
 H3FeO H3FeO  (aq)的平衡常数K<100
D . K2FeO4起杀菌消毒作用是因为其遇水生成了Fe(OH)3胶体 (aq)的平衡常数K<100
D . K2FeO4起杀菌消毒作用是因为其遇水生成了Fe(OH)3胶体
|
|
| 10. 单选题 | |
|
短周期主族元素W、X、Y、Z的原子序数依次增大,四种元元素组成的一种分子簇的球棍模型如图所示。W与X不在同周期,X原子的最外层电子数与核外电子总数之比为3:4,Z的周期数等于族序数。下列说法错误的是( )
A . 该分子簇的化学式为Y2Z2X6W2
B . 工业上常用电解熔融YX制备Y单质
C . 简单离子的半径:X>Y>Z
D . Y、Z的简单离子均可促进水的电离
|
|
高中化学 试卷推荐
- 专题04:氧化还原反应
- 山西省晋中市2020年高考化学三模试卷
- 吉林省五地六市联盟2018-2019学年高二下学期化学期末考试试卷A卷
- 2016-2017学年黑龙江省双鸭山市友谊县红兴隆管理局一中高三上学期期中化学试卷
- 高中化学鲁科版(2019)选择性必修2 第1章第1节 原子结构模型
- 北京市房山区2020年高考化学一模试卷
- 北京市海淀区2016-2017学年高三上学期化学期末考试试卷
- 人教版化学高二选修1第四章第一节改善大气质量同步练习
- 2016-2017学年浙江省湖州市高二下学期期中化学试卷
- 2016-2017学年湖北省天门、仙桃联考高一上学期期末化学试卷
- 江苏省宿迁市2018-2019学年高一上学期化学期末考试试卷
- 2017-2018学年人教版化学选修五 第一章 第三节 有机化合物的命名
最近更新