江西省景德镇市2021-2022学年高一下学期期末质量检测化学试题
江西省景德镇市2021-2022学年高一下学期期末质量检测化学试题
教材版本:化学
试卷分类:化学高一下学期
试卷大小:1.0 MB
文件类型:.doc 或 .pdf 或 .zip
发布时间:2024-05-01
授权方式:免费下载
下载地址:点此下载
教材版本:化学
试卷分类:化学高一下学期
试卷大小:1.0 MB
文件类型:.doc 或 .pdf 或 .zip
发布时间:2024-05-01
授权方式:免费下载
下载地址:点此下载
以下为试卷部分试题预览
| 1. 单选题 | ||||||||||||||||||||||||||
|
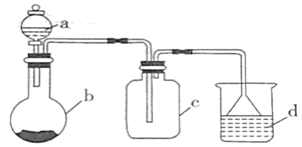
实验室中某些气体的制取、收集及尾气处理装置如图所示(省略夹持和净化装置)。仅用此装置中提供的物质完成相关实验,最合理的选项是( )
A . A
B . B
C . C
D . D
|
||||||||||||||||||||||||||
| 2. 单选题 | |
|
下列说法正确的是( )
A . 工业上镁、铝都是用电解其熔融氯化物制得
B . 可利用铝热反应冶炼铁、铬、锰、钴等高熔点金属
C . 蛋白质、油脂、糖类均能发生水解反应
D . 煤的干馏指将煤在空气中加强热使之分解的过程,工业上也叫做煤的焦化
|
|
| 3. 单选题 | |
|
绿色化学的核心是反应过程的绿色化,即要求原料物质中的所有原子完全被利用且全部转入期望的产品中,下列过程不符合这一思想的是( )
A . 乙烯合成聚乙烯
B . 甲烷与氯气反应制氯仿
C . 盐酸的制备:
 D . 甲烷、CO合成乙酸乙酯:
D . 甲烷、CO合成乙酸乙酯:
|
|
| 4. 单选题 | |
|
利用下列原电池,既能实现有效消除氮氧化物的排放,减轻环境污染,又能充分利用化学能,装置如图所示,下列有关说法错误的是( )
A . 电极A为负极,发生氧化反应
B . 电流从电极B经导线流向电极A,再经电解质溶液回到电极B
C . 为使电池持续放电,离子交换膜需选用阴离子交换膜
D . 当有4.48L
 (标准状况)被处理时,转移电子物质的量为0.6mol (标准状况)被处理时,转移电子物质的量为0.6mol
|
|
| 5. 单选题 | |
|
下列关于阿伏加德罗常数的计算正确的是( )
A . 1mol—OH和1molOH﹣的电子数均为10
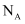 B . 标准状况下44.8L
B . 标准状况下44.8L 与足量氧气充分反应生成的 与足量氧气充分反应生成的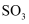 的分子数为2 的分子数为2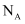 C . 42g聚乙烯和聚丙烯的混合物含有的碳原子数为3
C . 42g聚乙烯和聚丙烯的混合物含有的碳原子数为3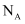 D . 44g
D . 44g 含有的共价键数目为9 含有的共价键数目为9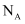
|
|
| 6. 单选题 | |
|
1mol某链状烷烃在氧气中充分燃烧,需要消耗氧气246.4L(标准状况下)。它在光照的条件下与氯气反应能生成四种不同的一氯取代物,该烃的结构简式是( )
A .
 B .
B .  C .
C .  D .
D . 
|
|
| 7. 单选题 | |
|
下列有关有机物的结构和性质的说法错误的是( )
A .
 只有一种结构说明了甲烷是空间四面体结构
B . 乙烯和聚乙烯都能使溴的四氯化碳溶液褪色
C . 只有一种结构说明了甲烷是空间四面体结构
B . 乙烯和聚乙烯都能使溴的四氯化碳溶液褪色
C .  中所有原子可能处于同一平面
D . 1mol乙醇与足量钠反应生成 中所有原子可能处于同一平面
D . 1mol乙醇与足量钠反应生成 证明了乙醇的结构为 证明了乙醇的结构为 , 而不是 , 而不是
|
|
| 8. 单选题 | |
|
下列说法能说明反应
 已达到平衡状态的是( ) 已达到平衡状态的是( )①单位时间内生成n mol ②一个H—H键断裂的同时有两个H—I键断裂 ③c(HI)=c( ④反应速率 ⑤ ⑥温度和体积一定时,某一生成物浓度不再变化 ⑦温度和体积一定时,容器内压强不再变化 ⑧条件一定,混合气体的平均相对分子质量不再变化 ⑨温度和体积一定时,混合气体的颜色不再发生变化 ⑩温度和压强一定时,混合气体的密度不再发生变化
A . ①②⑤⑨⑩
B . ②⑥⑨
C . ②⑥⑨⑩
D . 全部
|
|
| 9. 单选题 | |
|
下列关于反应热的叙述正确的是( )
A . 任何化学反应的反应热均可通过实验直接测定
B . Sn(s,灰锡)
 (Sn(s,白锡) (Sn(s,白锡)  (灰锡为粉末状,白锡为块状),则锡制品在炎热的夏天更容易损坏
C . (灰锡为粉末状,白锡为块状),则锡制品在炎热的夏天更容易损坏
C .  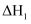 ; ;  则 则 D . P4(s,白磷)=4P(s,红磷)
D . P4(s,白磷)=4P(s,红磷)  , 常温下白磷比红磷更稳定 , 常温下白磷比红磷更稳定
|
|
| 10. 单选题 | |
|
室温下,用50mL 0.50mol/L盐酸和50mL0.55mo/L NaOH溶液在如图所示装置中进行中和反应,并通过测定反应过程中放出的热量计算中和反应的反应热。下列说法正确的是( )
A . 若用相同形状的细铜丝代替仪器a进行相应的实验操作,所测中和热
 将偏小
B . HCl和NaOH反应的中和热 将偏小
B . HCl和NaOH反应的中和热 , 则 , 则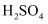 和 和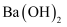 反应的中和热 反应的中和热 C . 该实验最少需要测定并记录温度的次数是3次
D . 若实验测得的反应前后温度差平均值
C . 该实验最少需要测定并记录温度的次数是3次
D . 若实验测得的反应前后温度差平均值 , 中和后生成溶液的比热容 , 中和后生成溶液的比热容 (若近似认为0.55mol/L NaOH溶液和0.50mol/L盐酸的密度都是 (若近似认为0.55mol/L NaOH溶液和0.50mol/L盐酸的密度都是 )。则生成1mol )。则生成1mol (l)时的反应热 (l)时的反应热
|
|
高中化学 试卷推荐
- 广西玉林、柳州市2020年高考理综-化学二模试卷
- 江苏省苏北四市2018届高三化学一模考试试卷
- 2016-2017学年河南省郑州市新密市英华中学高二上学期开学化学试卷
- 2015年广东省湛江市高考化学模拟试卷
- 2015-2016学年宁夏银川市育才中学勤行校区高二上学期月考化学试卷(12月份)
- 2016-2017学年河北省邯郸市四县联考高二下学期期中化学试卷
- 2016-2017学年湖北省部分重点中学高一上学期期中化学试卷
- 高中化学人教版(2019)必修第二册第五章 第二节 氮及其化合物
- 河南省周口市2016-2017学年高一下学期化学期末考试试卷
- 广西壮族自治区北海市2019-2020学年高一下学期化学期末考试试卷
- 2019年高考化学真题分类汇编专题10:物质结构与性质
- 2015-2016学年山东省菏泽市高一上学期期末化学试卷
最近更新

 的同时生成n molHI
的同时生成n molHI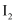 )
)





