河南省南阳市2021-2022学年高二上学期期中考试化学试题
河南省南阳市2021-2022学年高二上学期期中考试化学试题
教材版本:化学
试卷分类:化学高二上学期
试卷大小:1.0 MB
文件类型:.doc 或 .pdf 或 .zip
发布时间:2024-05-01
授权方式:免费下载
下载地址:点此下载
教材版本:化学
试卷分类:化学高二上学期
试卷大小:1.0 MB
文件类型:.doc 或 .pdf 或 .zip
发布时间:2024-05-01
授权方式:免费下载
下载地址:点此下载
以下为试卷部分试题预览
| 1. 单选题 | |
|
我国提出争取在2030年前实现碳达峰,2060 年实现碳中和,这对于改善环境,实现绿色发展至关重要。下列措施中叙述错误的是( )
A . 消费端的减碳:研发能够高效利用CO2的新型电池
B . 消费端的减碳:推动新能源汽车的开发和充电桩基础实施的安装
C . 发电端的减碳:鼓励光伏、风电、水电、核电、煤电等能源的发展
D . 配套措施之一碳捕捉:使用溶剂对CO2进行吸收,最后吹出CO2气体并压缩再利用
|
|
| 2. 单选题 | |
|
下列事实不能用勒夏特列原理解释的是( )
A . 用排饱和食盐水法收集Cl2
B . 对于2HI(g)
 H2(g)+I2(g),达平衡后,缩小容器体积可使体系颜色变深
C . 开启可乐瓶后,瓶中马上泛起大量泡沫
D . 工业制硫酸的过程中使用过量的空气以提高二氧化硫的转化率,从而降低生产成本 H2(g)+I2(g),达平衡后,缩小容器体积可使体系颜色变深
C . 开启可乐瓶后,瓶中马上泛起大量泡沫
D . 工业制硫酸的过程中使用过量的空气以提高二氧化硫的转化率,从而降低生产成本
|
|
| 3. 单选题 | |
|
下列与金属腐蚀有关的说法正确的是 ( )
A . 图a插入海水中的铁棒(含碳量为10.8%)越靠近烧杯底部发生电化学腐蚀就越严重
B . 图b开关由N改置于M时,金属铁的腐蚀速率减小
C . 图c为牺牲阳极的阴极保护法,钢闸门应与外接电源的负极相连
D . 图d在反应过程中能产生氢气
|
|
| 4. 单选题 | |||||||||||||||||||||
|
下列对化学反应的预测正确的是( )
A . A
B . B
C . C
D . D
|
|||||||||||||||||||||
| 5. 单选题 | |
|
下列说法正确的是( )
A . 已知C(s)+O2(g)=CO2(g) △H =akJ·mol-1 , C(s)+
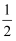 O2(g)=CO(g) △H=bkJ·mol-1 ,则a>b
B . 恒温条件下,反应NH2COONH4(s)⇌2NH3(g)+CO2(g)达平衡后,向密闭容器中加入NH2COONH4 , 平衡正向移动
C . 恒温恒容条件下, N2(g)+3H2(g)⇌2NH3(g)达平衡后, 通入稀有气体使压强增大,平衡正向移动
D . 测定中和热实验过程中,用温度计测量NaOH溶液的温度后,不能直接测定盐酸的温度 O2(g)=CO(g) △H=bkJ·mol-1 ,则a>b
B . 恒温条件下,反应NH2COONH4(s)⇌2NH3(g)+CO2(g)达平衡后,向密闭容器中加入NH2COONH4 , 平衡正向移动
C . 恒温恒容条件下, N2(g)+3H2(g)⇌2NH3(g)达平衡后, 通入稀有气体使压强增大,平衡正向移动
D . 测定中和热实验过程中,用温度计测量NaOH溶液的温度后,不能直接测定盐酸的温度
|
|
| 6. 单选题 | |
|
用惰性电极电解下列各组中的三种溶液,电解过程中,溶液中pH依次为减小、不变、增大的是( )
A . HCl、HNO3、K2SO4
B . AgNO3、CuCl2、 Cu(NO3)2
C . CaCl2、 KOH、NaNO3
D . CuSO4、Na2SO4、KCl
|
|
| 7. 单选题 | |
|
100℃时, 将0.1 mol N2O4置于1 L密闭的烧瓶中,然后将烧瓶放入100℃的恒温槽中,烧瓶内的气体逐渐变为红棕色: N2O4(g)
 2NO2(g)。 下列结论不能说明上述反应在该条件下已经达到反应限度的是( ) 2NO2(g)。 下列结论不能说明上述反应在该条件下已经达到反应限度的是( )①N2O4的消耗速率与NO2的生成速率之比为1:2 ②烧瓶内气体的颜色不再加深 ③烧瓶内气体的压强不再变化 ④烧瓶内气体的质量不再变化 ⑤NO2的物质的量浓度不再改变 ⑥烧瓶内气体的密度不再变化 ⑦烧瓶内气体的平均相对分子质量不再变化
A . ①④⑥
B . 只有①④
C . ②③⑥⑦
D . 只有⑥⑦
|
|
| 8. 单选题 | |
|
甲、乙均为1L的恒容密闭容器,向甲中充入1molCH4和1molCO2 , 乙中充入1molCH4和n molCO2 , 在催化剂存在下发生反应: CH4(g)+CO2(g)
 2CO(g)+2H2(g),测得CH4的平衡转化率随温度的变化如图所示。下列说法正确的是( ) 2CO(g)+2H2(g),测得CH4的平衡转化率随温度的变化如图所示。下列说法正确的是( )
A . H2 的体积分数:φ(b)<φ(c)
B . 773K 时,该反应的平衡常数大于12.96
C . 该反应的正反应是放热反应
D . 873K 时,向甲的平衡体系中再充入CO2、CH4各0.4mol,CO、H2各1.2 mol,平衡不发生移动
|
|
| 9. 单选题 | |
|
氢能是一种极具发展潜力的清洁能源。以太阳能为热源,热化学硫碘循环分解水是一种高效、环保的制氢方法,其流程如图所示。
相关反应的热化学方程式为: 反应I: SO2(g)+I2(g)+ 2H2O(1)= 2HI(aq)+H2SO4(aq) △H1 = -213kJ·mol-1 反应II: H2SO4(aq)= SO2(g)+H2O(1)+ 反应III: 2HI(aq)=H2(g)+I2(g) △H3 = +172 kJ· mol-1 下列说法错误的是( )
A . 该过程实现了太阳能到化学能的转化
B . 总反应的热化学方程式为2H2O(1)=2H2(g)+O2(g) △H = +286 kJ· mol-1
C . 升高温度可使反应II、III的化学平衡常数均增大
D . 该制氢方法生成1molH2(g)的反应热与直接电解水生成1 molH2(g)的反应热相等
|
|
| 10. 单选题 | |
|
在恒容密闭容器中充入一定量的CO2和H2 , 在不同温度下发生反应CO2(g)+3H2(g)⇌CH3OH(g)+H2O(g) △H <0。 CH3OH 的体积分数与起始时H2与CO2的投料比值
 的关系如图甲所示,投料比值 一定时,CH3OH的浓度与温度的关系如图乙所示。 的关系如图甲所示,投料比值 一定时,CH3OH的浓度与温度的关系如图乙所示。
下列推断正确的是( )
A . 图甲中,T1>T2
B . 图甲中,CO2的转化率: b>a>c
C . 图乙中,T1之前随着温度的升高,平衡正向移动
D . 图乙中,CO2的转化率: e>d>f
|
|
高中化学 试卷推荐
- 天津市河西区2022届二模化学试题
- 吉林省长春市农安县五校联考2020-2021学年高一上学期化学期末考试试卷
- 黑龙江省哈尔滨市依兰县高中2020-2021学年高一下学期化学5月月考试卷
- 广东省梅州市2020-2021学年高二上学期化学期末考试试卷
- 四川省德阳市2021年高考化学三模试卷
- 北京市东城区2020-2021学年高一上学期期末考试化学试题
- 广东省惠州市惠城区2021-2022学年高三上学期化学开学考试试卷
- 陕西省宝鸡市金台区2020-2021学年高一下学期期末考试化学试题
- 内蒙古包头市2022届高三第二次模拟考试理综试卷化学试题
- 黑龙江省牡丹江市海林市朝鲜族中学2020-2021学年高一下学期化学4月月考试卷
- 辽宁省大连市2021-2022学年高二上学期期末联考化学试题
- 安徽省合肥市2022届高三第二次教学质量检测理综化学试题
最近更新







