4 二氧化碳 知识点题库
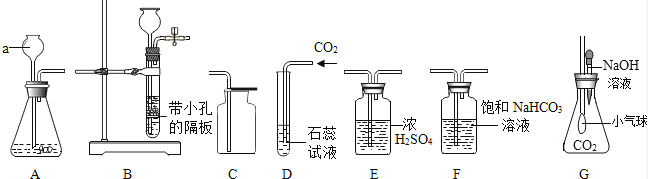
某化学小组Ⅰ探究用大理石和盐酸反应制取二氧化碳气体,并进行性质实验.如图是有关实验的部分装置,请根据要求回答问题:
-
(1) a仪器的名称为;甲同学用A和C组合制取二氧化碳,乙同学用B和C组合制取二氧化碳,你认为哪个组合更便于控制反应(填写甲或乙).
-
(2) 甲同学利用装置D进行性质实验时,观察到紫色石蕊试液变红色,将红色液体充分加热未能重新变为紫色,你认为可能的原因是;为使上述红色液体加热后能重新变为紫色,在气体通入装置D之前可接入如图装置 (填字母序号),在该装置中发生的主要化学反应方程式为 .
-
(3) 乙同学将CO2通入到氢氧化钠溶液中,无明显现象,经过思考讨论后,设计了如图G装置,使该反应有了明显现象,则装置G中的现象为 .
实验室现有氯酸钾、稀盐酸、二氧化锰、大理石、火柴、药匙、镊子及以下仪器:

(1)若补充仪器和(填名称),并利用上述部分仪器和药品可制取一种气体,则发生反应的化学方程式为 .制取该气体时,需先检查装置的气密性;连接好仪器,将导管一端浸入水中,用手紧握容器外壁,使容器内湿度 , 压强变 , 观察到水中导管口有时,说明装置不漏气.
(2)若要制备并检验二氧化碳,需补充一种溶液,该溶液中溶质的俗称有 .
①请连接A、B,并将装置图2补充完整 ;
②B中可观察到的实验现象是 .

【査阅资料】①Na2S4受热时,会与空气中的水蒸气反应,生成少量有毒气体硫化氢
②硫代硫酸钠(Na2S2O3)可溶于水,常温下与NaOH溶液不反应。
③NaOH溶液可吸收硫化氢和二氧化碳。
【实验过程】

①取0.5g碳酸钠、0.2g硫粉混合后置于试管中,加入(如图①所示,夹持装置已略去),制得Na2S4 , 反应为:4Na2CO3+12S+X 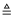 2Na2S4+2Na2S2O3+4CO2 , X的化学式为。
2Na2S4+2Na2S2O3+4CO2 , X的化学式为。
②冷却后,取下棉花,放置一段时间,再向该试管中加入10mL水,迅速塞紧橡胶塞,充分振荡。测量液面至橡胶塞下沿的距离,记录数据h1(如图②所示);
③将该试管插入水中(如图③所示),拔下橡胶塞,观察到,塞紧橡胶塞。将试管取出,倒转过来,测量液面至橡胶塞下沿的距离h2 , 记录数据h2。理论上h2:h1= ;
④按照①~③再重复实验2次。3次实验数据如下表所示。
| 第1次 | 第2次 | 第3次 | |
| h1/cm | 11.0 | 11.4 | 11.6 |
| h2/cm | 8.7 | 9.1 | 9.2 |
【解释与结论】根据第1次实验数据,计算空气中氧气的体积分数为%(结果精确到0.1%);
【反思与评价】实验过程①中浓NaOH溶液的作用是;若实验过程②中,取下棉花后,未放置一段时间即进行后续操作,测定结果(填“偏大”、“偏小”或“无影响”),理由是:。

实验一:如图,将一支充满二氧化碳试管倒扣在盛有氢氧化钠溶液的烧杯中,观察管中的液面情况。
实验二:如图乙,向两个装满二氧化碳的同样规格的瓶中分别注入等量的氢氧化钠溶液和蒸馏水,振荡后放在水平桌面上,观察U型管(装有红墨水)两端液面的变化情况。请问:
-
(1) 实验二中若观察到U型管左端的液面(填“升高”或“降低”),则证明溶液中的氢氧化钠与二氧化碳反应。
-
(2) 与实验一相比,同学们认为实验二更合理,因为它能排除对实验的干扰。

-
(1) 该兴趣小组同学设计的木炭还原CuO实验装置有何不足之处?
-
(2) 为验证产生的气体是CO2和CO的混合物,将混合气体进行如下操作:

实验中观察到现象则证明是CO2和CO的混合气体。
-
(3) 探究红色固体中是否有Cu2O。设计一个简便的实验方案,如下表所示。
实验步骤
向剩余固体中加入稀盐酸反应后,静置
实验现象与结论
现象;结论:红色固体中有Cu2O
化学反应方程式


-
(1) 把A装置与E装置连接,如果E装置中出现溶液变浑浊的现象,则证明二氧化碳气体中混有;
-
(2) 将除去杂质的二氧化碳气体通入C装置中,发现澄清石灰水变浑浊,写出发生反应的化学方程式;
-
(3) 若要制取一瓶纯净、干燥的二氧化碳气体,请从上述各装置中选择适当的装置进行连接,连接顺序是。

资料一:17世纪,海尔蒙特发现木炭燃烧之后除了产生灰烬外还产生一些看不见、摸不着,却能使烛火自然熄灭的气体,他称之为“森林之精”,后来被证实是CO2气体。
资料二:1766年,卡文迪许通过实验测得,室温下1体积水大约能溶解1体积CO2气体。
资料三:1828年德国化学家德里希维勒首次使用氨气(NH3)与CO2在高温高压下反应生成尿素[CO(NH2)2]和水。
-
(1) 根提海尔蒙特的发现,可推测二氧化碳的化学性质: 。
-
(2) 如图,在室温下将容积为300毫升的广口瓶注满蒸馏水,通过导管a缓慢通入500毫升CO2 , 如果卡文迪许的结论是正确的,则在量筒中收集到的水约为毫升。

-
(3) 写出德里希维勒实验中的化学方程式: 。
①它们的物理性质不同
②它们的化学性质不同
③它们是不同的两种物质

①不能燃烧
②不能支持燃烧
③不能供给呼吸
④同体积的质量比空气大
⑤同体积的质量比空气小
|
实验次序 |
实验一 |
实验二 |
实验三 |
实验四 |
|
鸡蛋壳的质量/g |
10 |
10 |
10 |
10 |
|
加入盐酸的质量/g |
10 |
20 |
30 |
40 |
|
反应后溶液总质量/g |
18.9 |
m |
36.7 |
46.7 |
请计算:
-
(1) 表格中m的数值为。
-
(2) 40g鸡蛋壳与足量的盐酸溶液反应,最多生成气体质量为g。
-
(3) 该鸡蛋壳中CaCO3的质量分数是多少?

-
(1) 步骤①中发生反应的化学方程式为:。
-
(2) 滤液II是30℃时氯化钡的饱和溶液,请说明原因:。
-
(3) 关于上述实验方案的相关内容,下列说法正确的是 (填字母)。A . 氯化钡是一种有毒的物质,使用时应注意安全 B . 该实验流程中得到的副产品二氧化碳是重要的化工原料 C . 可用重晶石(主要成分是硫酸锁)代替该实验流程中的毒重石制备氟化钡晶体 D . 步骤②将滤渣进行水洗,既能提高氯化钡晶体的产率,又能减少Ba2+对环境的污染



