第4章 认识化学变化 知识点题库
硫酸钡是一种不溶于水,也不和酸反应的固体,医疗上常用硫酸钡作透视肠胃的内
服造影剂,俗称“钡餐”。若“钡餐”中含有碳酸钡,就会致人中毒。为测定某硫酸钡样品中碳酸钡的 含量,取100g样品,向其中逐渐加入一定质量分数的稀硝酸至恰好完全反应,发生反应的化学方
程式为:BaCO3+2HNO3═Ba(NO3)2+H2O+CO2↑,测得共用去稀硝酸245.7g,反应后称得烧杯中物质的总质量为341.3 g.请计算:
-
(1) 反应生成的二氧化碳为g。
-
(2) 所用的稀硝酸的溶质质量分数是多少?原样品中硫酸钡的质量分数是多少?(计算结果保留% 前一位小数)
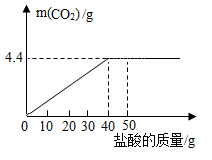
钙是人体中的常量元素,缺钙时可通过食用保健药剂来增加摄人量,现将20片该药剂制成粉末(主要成分为碳酸钙,每片1g,其他成分不与盐酸反应且不含钙元素),并与50g盐酸混合,充分反应后得到如下图像,请根据有关信息回答问题。
-
(1) 反应结束共生成二氧化碳的质量为g。
-
(2) 计算每片药剂中所含碳酸钙的质量分数?
-
(3) 反应结束后,溶液中的阳离子主要为(写离子符号)
某氧化钙样品中混有碳酸钙杂质,现取样品
6.6g,经高温灼烧至碳酸钙完全分解,冷却至室温,称得残留固体的质量为 6.16g。(碳酸钙高温分解生成氧化钙和二氧化碳  )求:
)求:
 )求:
)求:
-
(1) 生成二氧化碳的质量。
-
(2) 样品中氧化钙的质量。
-
(3) 样品中钙元素的质量分数。(保留到 0.1%)
对下列化学知识的认识正确的是( )
A . 化学变化的过程常会伴随着能量变化
B . 化合物是含有不同元素的纯净物,所以纯净物一定含有不同元素
C . 控制化学反应的条件,可使化学反应向着人们需要的方向转化
D . 可燃物燃烧时需要与氧气接触,所以可燃物只要与氧气接触,就一定能燃烧
下列做法符合安全要求的是( )
A . 电器着火,马上用水浇灭
B . 给不超过试管容积1/3的液体加热
C . 室内失火,立即打开门窗排除浓烟
D . 氢氧化钠溶液沾到皮肤上,先用水冲洗,再涂上稀硫酸
能源、环境与人类的生活和社会发展密切相关
-
(1) 三大化石燃料包括:煤、、天然气。 天然气的主要成分为甲烷,请写出 甲烷充分燃烧的化学方程式。
-
(2) 在汽油中加入适量的乙醇作为汽车燃料(车用乙醇汽油),不但可以适当节约石 油资源,还具有的优点是(答一点即可)。
-
(3) 做饭时,当燃气灶的火焰呈现黄色,锅底出现黑色,说明燃气没有充分燃烧,此时应该调 (填“大”或“小”)灶具的进风口。
下列4个坐标图分别表示实验过程中某些量的变化,其中正确的是( )
A . 在密闭装置内点燃红磷  B . 向盛有MnO2的烧杯中加入H2O2溶液
B . 向盛有MnO2的烧杯中加入H2O2溶液  C . 向一定量石灰石中滴加稀盐酸
C . 向一定量石灰石中滴加稀盐酸  D . 向两份完全相同的稀盐酸中分别加入足量锌粉、镁粉
D . 向两份完全相同的稀盐酸中分别加入足量锌粉、镁粉 
 B . 向盛有MnO2的烧杯中加入H2O2溶液
B . 向盛有MnO2的烧杯中加入H2O2溶液  C . 向一定量石灰石中滴加稀盐酸
C . 向一定量石灰石中滴加稀盐酸  D . 向两份完全相同的稀盐酸中分别加入足量锌粉、镁粉
D . 向两份完全相同的稀盐酸中分别加入足量锌粉、镁粉 
塑料的回收再利用意义重大。下列属于回收标志的是( )
A .  B .
B .  C .
C .  D .
D . 
 B .
B .  C .
C .  D .
D . 
电石渣是电石制取乙炔气体后的废渣,电石渣主要成分是
Ca(OH)2 , 另有少量 SiO2、FeO、Al2O3、MgO
等物质。电石渣可用于生产建材、化工产品,治理大气及废水污染处理等。某化工厂用电石渣湿法脱硫,除去烟气中的 SO2.回答问题:

-
(1) 化工厂烟气中的 SO2排放到空气中,降雨时会造成酸雨,SO2和 H2O反应的化学方程式为。
-
(2) 学习小组研究了不同 pH 条件下的脱硫效率,发现 pH 为 6.5 时,脱硫效率较好,测定 pH 时,应用测定。
-
(3) 上图是湿法脱硫工艺中的喷淋塔局部示意图,SO2入口为(填“a”或“b”)。
-
(4) 常用石灰石进行烟气脱硫,反应的原理是
 。电石渣湿法脱硫过程中,Ca(OH)2与 SO2、O2、H2O 发生反应,生成 CaSO4·2H2O,反应的化学方程式为。湿法脱硫相比石灰石脱硫效率更 高的原因可能是,此外,电石渣湿法脱硫的优点除了以废治废,降低成本,还有。
。电石渣湿法脱硫过程中,Ca(OH)2与 SO2、O2、H2O 发生反应,生成 CaSO4·2H2O,反应的化学方程式为。湿法脱硫相比石灰石脱硫效率更 高的原因可能是,此外,电石渣湿法脱硫的优点除了以废治废,降低成本,还有。
-
(5) 已知:
 ,某pH条件下,若SO2入口浓度为2000mg/m3 , 出口浓度为 30mg/m3 , 则此工艺条件下 SO2的脱除效率为 。
,某pH条件下,若SO2入口浓度为2000mg/m3 , 出口浓度为 30mg/m3 , 则此工艺条件下 SO2的脱除效率为 。
下列图标中,表示“禁止燃放鞭炮”的是( )
A .  B .
B .  C .
C .  D .
D . 
 B .
B .  C .
C .  D .
D . 
下列化学方程式书写正确的是( )
A .  B .
B .  C .
C .  D .
D . 
 B .
B .  C .
C .  D .
D . 
下列关于燃烧与灭火的说法中,正确的是( )

A . 由图 b 的现象可知,金属镁引起的火灾不能用二氧化碳扑灭
B . 将大块煤粉碎后再燃烧,其目的是延迟煤燃烧的时间
C . 灭火蜡烛用嘴一吹即灭,是因为吹出的气体主要是二氧化碳
D . 如图 a,火柴头斜向下时更容易燃烧,是因为降低了火柴梗的着火
可燃物燃烧条件的验证实验如图所示。已知白磷的着火点为40℃,请你根据实验回答下列问题。

-
(1) 三个实验中,白磷会燃烧的是(选填序号)。
-
(2) 通过A、C实验对比,证明可燃物燃烧的条件之一是。
-
(3) 通过B、C实验对比,证明可燃物燃烧的条件之一是。
根据如图所示的实验回答相关问题。
A.测定空气中氧气含量  B.燃烧条件探究
B.燃烧条件探究 
C.量取水的体积  D.蜡烛燃烧前后质量的测定
D.蜡烛燃烧前后质量的测定 
-
(1) A实验红磷需过量的目的是。
-
(2) B实验观察到Y形管中白磷燃烧,红磷不燃烧,可得出的燃烧条件是;Y形管中白磷燃烧,热水中的白磷不燃烧,又可得出的燃烧条件是。
-
(3) C操作会导致量取水的体积(填“偏大”“偏小”或“不变”)。
-
(4) D实验(填“能”或“不能”)用于验证质量守恒定律。
下列实验设计不能达到其对应实验目的是( )
A .  读出液体的体积
B .
读出液体的体积
B .  检查装置的气密性
C .
检查装置的气密性
C .  验证质量守恒定律
D .
验证质量守恒定律
D .  闻气体的味
闻气体的味
 读出液体的体积
B .
读出液体的体积
B .  检查装置的气密性
C .
检查装置的气密性
C .  验证质量守恒定律
D .
验证质量守恒定律
D .  闻气体的味
闻气体的味
书写化学方程式:
-
(1) 硫燃烧的化学方程式为。
-
(2) 氢气燃烧的化学方程式为。
-
(3) 铁丝在氧气中燃烧的化学方程式为。
-
(4) 天然气的主要成分是甲烷。甲烷燃烧的化学方程式为。
-
(5) 酒精燃烧的化学方程式为。
化学是一门以实验为基础的科学,下面是初中化学中几组重要的对比实验。


-
(1) 实验1中,观察到A烧杯中的现象是,由此可验证分子的性质。
-
(2) 实验2中,观察到铜片上的白磷燃烧而红磷不燃烧,可得出可燃物燃烧的一个条件为。根据此条件,举一例相关的灭火事例。
-
(3) 实验3中,实验过程中布条能变红色的试剂瓶是,C烧杯发生反应的化学方程式为。
酸碱盐种类繁多,与人类日常生活和工农业生产关系十分密切。
-
(1) 酸具有相似的性质,因为不同的酸在水溶液中都能解离出(填化学符号)测定溶液的pH时,不能将pH试纸直接浸入待测液中的原因;盐酸可用于金属表面除锈,请写出盐酸除铁锈的化学方程式。
-
(2) 下列各组物质在强酸性和强碱性溶液中都能大量共存的是_______。(填序号)A . NaCl、MgSO4 B . (NH4)2CO3、K2SO4 C . KNO3、BaCl2 D . Ba(NO3)2、CuCl2
-
(3) 下列试剂能将稀盐酸、氯化钠溶液、澄清石灰水三种溶液一次鉴别出来的是____(填字母序号)。A . 稀硫酸 B . 碳酸钠溶液 C . 酚酞溶液
-
(4) 实验室有一瓶久置的氢氧化钠样品,为探究其是否完全变质,某同学设计了以下实验方案:取少量样品溶解,滴加适量饱和石灰水,再在上层清液中滴加酚酞溶液,溶液变为红色。你认为上述实验方案都能达到目的吗,为什么?。
-
(5) 老师建议将(4)中该同学方案
 进行定量化处理:取10g样品溶于足量的水,向其中滴加过量饱和石灰水,过滤,将沉淀洗涤烘干,称其质量为2g,请通过计算说明氢氧化钠是否完全变质。
进行定量化处理:取10g样品溶于足量的水,向其中滴加过量饱和石灰水,过滤,将沉淀洗涤烘干,称其质量为2g,请通过计算说明氢氧化钠是否完全变质。
我国最近已研究出新型水处理剂ClO2的新制法,其反应的微观过程如图所示。下列说法错误的是( )

A . 乙中氯元素的化合价为+3价
B . 该反应前后分子的个数不变
C . 该反应的本质是原子的重新组合
D . 丙属于氧化物
有关下列图像的描述,正确的是( )
A .  表示向硫酸铜溶液中不断滴入氢氧化钡溶液
B .
表示向硫酸铜溶液中不断滴入氢氧化钡溶液
B .  表示将两份质量相等的固体物质分别加热制取氧气
C .
表示将两份质量相等的固体物质分别加热制取氧气
C .  表示向一定温度下氢氧化钙的饱和溶液中加入少量氧化钙固体
D .
表示向一定温度下氢氧化钙的饱和溶液中加入少量氧化钙固体
D .  表示向等质量的镁条和铝条中分别加入足量的溶质质量分数相同的稀硫酸
表示向等质量的镁条和铝条中分别加入足量的溶质质量分数相同的稀硫酸
 表示向硫酸铜溶液中不断滴入氢氧化钡溶液
B .
表示向硫酸铜溶液中不断滴入氢氧化钡溶液
B .  表示将两份质量相等的固体物质分别加热制取氧气
C .
表示将两份质量相等的固体物质分别加热制取氧气
C .  表示向一定温度下氢氧化钙的饱和溶液中加入少量氧化钙固体
D .
表示向一定温度下氢氧化钙的饱和溶液中加入少量氧化钙固体
D .  表示向等质量的镁条和铝条中分别加入足量的溶质质量分数相同的稀硫酸
表示向等质量的镁条和铝条中分别加入足量的溶质质量分数相同的稀硫酸
最近更新



