基础实验4 常见金属的性质 知识点题库
如图所示,玻璃瓶中都装满冷开水,并加入碳酸氢钠(一种二氧化碳释放剂).将装置置于光照条件下,一段时间后,判断甲、乙两瓶中哪枚铁钉先出现锈迹,并说明理由.

控制变量法是实验探究的重要方法.利用如图所示实验不能实现的探究目的是( )

①在铁制品表面镀锌 ②在铁制品表面涂油脂 ③在铁制品表面覆盖搪瓷 ④在铁器表面刷油漆
⑤自行车脏了用清水冲洗 ⑥用废酸液冲洗铁制污水管道 ⑦切完咸菜后,尽快将菜刀洗净擦干
⑧保留铁件表面的铁锈作保护层.

 ,铁的相对原子质量为55.85
D . Fe在空气中燃烧生成Fe2O3
,铁的相对原子质量为55.85
D . Fe在空气中燃烧生成Fe2O3
选项 | 待提纯的物质(括号内为杂质) | 所加试剂 | 操作方法 |
A | CuSO4(铁粉) | 足量水 | 溶解、过滤 |
B | FeCl3溶液(CuCl2) | 过量铁粉 | 过滤 |
C | CaO(石灰石) | 无 | 高温 |
D | Cu(Zn) | 足量稀盐酸 | 过滤、洗涤、干燥 |
|
选 项 |
物 质 |
杂 质 |
试剂 |
方法 |
|
A |
CO2 |
CO |
O2 |
点燃 |
|
B |
NaOH溶液 |
NaCl |
适量稀盐酸 |
蒸发 |
|
C |
CaO |
CaCO3 |
H2O |
过滤 |
|
D |
Cu |
Fe |
过量稀硫酸 |
过滤 |

| | | | |
| A.向一定量的稀盐酸中加入过量的镁粉 | B.向一定量的稀盐 酸中加入足量的水稀释 | C.向两份完全相同的稀盐酸中分别加入锌粉、镁粉 | D.向一定量氢氧化钠溶液中滴加稀盐酸 |
-
(1) I 化学兴趣小组的同学对“影响铁钉锈蚀快慢的因素”展开了如下探究:
(提出问题)溶液的酸碱性对铁钉生锈的快慢是否有影响?溶液中的阴离子种类对铁钉锈蚀的快慢是否有影响?
(设计实验)按图1装置进行实验,测得装置中氯化铵、硫酸铵溶液上方氧气浓度变化曲线如图2。


上述实验中,氧气浓度下降先陡后缓的原因为。
-
(2) 将规格、材质相同的打磨过的铁钉放入下列不同溶液中,测得有关数据如下表:
溶液中的溶质
氯化铵
硫酸铵
氯化钠
硫酸钠
氢氧化钠
0 min时氧气浓度/%
20.8
20.8
20.8
20.8
20.8
500 min时氧气浓度/%
15.8
17.0
18.6
19.0
19.8
实验前溶液pH
5.31
5.53
7.0
7.0
13.6
实验后溶液pH
7.37
7.99
10.5
10.4
13.8
铁钉锈蚀情况
大量
铁锈
大量
铁锈
少量
铁锈
少量
铁锈
几乎
无锈
(结论与拓展)①实验中溶液上方氧气浓度变化越大,证明铁钉锈蚀速率。
②根据表中数据可知,铁钉在(填“酸”、“碱”或“中”)性溶液中更易锈蚀,其中铁钉在含有(填“氯离子”或“硫酸根离子”)的溶液中锈蚀更快。
-
(3) (拓展应用)化学是把双刃剑,铁制品在使用过程中常常会出现不同程度的锈蚀,会造成资源浪费,但将铁生锈的原理用于食品脱氧时,要求铁能快速生锈从而达到脱氧的目的,因此食品脱氧剂中除了加入铁粉、炭粉外,还可加入。
-
(4) II某实验小组同学欲通过实验探究金属的性质。
(实验目的)证明金属活动性强弱:Al > Cu
(设计并实施实验)小组内的3位同学分别做了下述实验:
实验
现象
甲
将铝片直接放入到稀CuCl2溶液中
一段时间后才出现了预期的实验现象
乙
将用砂纸打磨过的铝片放入稀CuCl2溶液(与甲实验浓度相同)中
十几秒内即观察到明显现象。
丙
将用砂纸打磨过的铝片放入稀CuSO4溶液中
在与乙相同的时间内没有观察到明显现象
对比甲、乙同学的实验,推测甲同学开始时没有观察到明显实验现象的原因是。
-
(5) (提出问题)为什么打磨过的铝片放入到CuCl2溶液和CuSO4溶液中观察到的现象不同呢?
(微观探析)查阅资料可知两个反应的微观示意图如下。
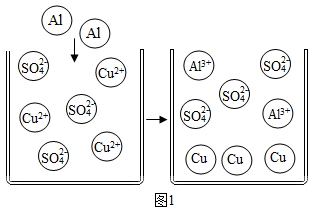

图1反应的化学方程式为;Al和CuCl2溶液、CuSO4溶液反应的微观本质是Al和Cu2+反应生成 Al3+和。
-
(6) (提出猜想)根据上述图示,小组同学提出了如下猜想。
猜想1:产生现象不同的原因是CuCl2溶液比CuSO4溶液中含有的Cu2+浓度大。
猜想2:溶液中Cl-对Al和Cu2+反应有促进作用。
猜想3:溶液中
 对Al和Cu2+反应有阻碍作用。
对Al和Cu2+反应有阻碍作用。(设计并实施实验)
序号
实验方案及操作
现象
结论
①
乙、丙两位同学取Cu2+浓度相同的CuCl2溶液和CuSO4溶液重复实验。
与上述乙、丙同学实验现象相同
猜想1(填“成立”或“不成立”)
②

在同一时间内,③最快产生现象,②次之,①无明显现象
猜想2成立
-
(7) 甲同学认为通过实验2得到的结论证据不充足,理由是溶液中的微粒对实验可能有干扰。
-
(8) 丙同学通过查阅资料排除了上述干扰,并模仿实验2又设计了一组3支试管的实验,证明了猜想3也成立。请在下列方框中画出实验设计图示。

求:
-
(1) 生成氢气的质量为克。
-
(2) 黄铜中锌的质量分数。(要求写出计算过程)

-
(1) F的名称是。
-
(2) 写出B→C反应的化学方程式:。
-
(3) 写出A与E反应的化学方程式:。
-
(4) 写出G→J反应的化学方程式:。







