第四单元 我们周围的空气 知识点题库
-
(1) 在实验室里,利用大理石(含不溶于酸的杂质)和稀盐酸来制取二氧化碳。
①有关反应可用化学方程式表示为;
②要制取总质量为4.4g的二氧化碳,理论上需要g质量分数为10%的稀盐酸跟足量的大理石反应。
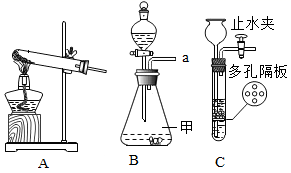
③组装一套制取装置时,可选用所给仅器中的a、b,d、g、h、j、n和;
④若从制取二氧化碳的废液中回收氯化钙,可行的操作步骤是。
-
(2) 实验室中若想利用上述制取二氧化碳的整套装置,还可以完成的实验是 。A . 高锰酸钾制氧气 B . 过氧化氢溶液和二氧化锰制氧气 C . 锌粒和稀硫酸制氢气
-
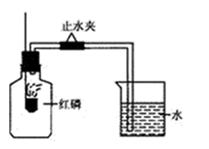
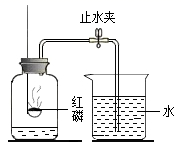
(1) 红磷燃烧的现象:红磷在集气瓶中发生反应的文字表达式为。该实验中红磷稍过量,目的是。
-
(2) 待燃烧停止,白烟消失并冷却后,打开止水夹,观察到烧杯中的水进入集气瓶,瓶内水量约是集气瓶中原空气体积的,瓶内剩余气体主要是,试写出该气体的一条性质。
-
(3) 若将红磷换成炭粉,该实验能否获得成功?,理由是 。
-
(1) 化学是在、层次上研究物质的性质、组成、结构以及变化规律的科学。
-
(2) 取用液体药品时,试剂瓶瓶盖应放在实验台上;试剂瓶标签;瓶口紧挨试管口;实验里要严格按照规定的用量取药,如果没有说明用量,就应该取用最少量,即:固体只要,液体用mL,取用块状固体时使用,取用粉末状固体时使用。
-
(3) 银白色的镁带在空气中燃烧时发出,在氧气中燃烧更加剧烈,放出大量的热,生成一种白色的粉末状固体是氧化镁。将二氧化锰粉末投入到过氧化氢溶液中,产生大量气泡,检验气泡是氧气的正确方法是;玻璃棒在粗盐提纯实验过程中的作用:溶解中的作用;蒸发中的作用。
-
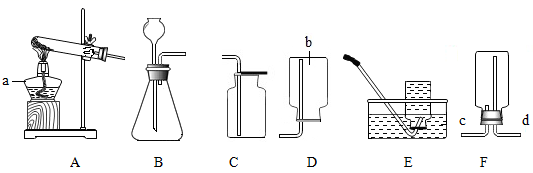
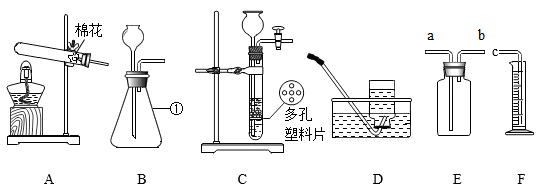
(1) 写出仪器a、b的名称:a,b。
-
(2) 实验室欲使用高锰酸钾制取氧气,反应的化学方程式为,应选择的发生装置和收集装置是(F除外)。若选择F装置收集氧气,气体应从端进入(填序号)。
-
(3) 若用C装置收集氧气,验满的方法是:将观察木条是否。
-
(4) 若用排水法收集氧气,停止加热时,应(填序号)。
①先熄灭酒精灯,再把导管移出水面
②先把导管移出水面,再熄灭酒精灯
-
(5) 实验室制取某气体,组装好实验装置,加入药品前必须进行的一项操作是。
-
(1) 红磷燃烧的文字表达式是,该实验中红磷稍过量,目的是;
-
(2) 冷却后打开止水夹后观察到的现象是;
-
(3) 若实验中进入集气瓶的水不足容积的五分之一,可能原因主要有:。
-
(4) 查阅资料:镁+氧气
 氧化镁;镁+氮气
氧化镁;镁+氮气  氮化镁;根据提供的资料回答下列的问题,请问镁条能否用来代替红磷测定空气中氧气的含量吗?(填“能”或“不能”)并说出原因是。
氮化镁;根据提供的资料回答下列的问题,请问镁条能否用来代替红磷测定空气中氧气的含量吗?(填“能”或“不能”)并说出原因是。
-
(1) 写出上图中仪器①的名称。
-
(2) 实验室用A和D装置制取并收集O2 , 反应的化学方程式是,实验操作如下:①加热;②检查装置气密性;③装药品及用品;④用排水法收集;⑤从水槽中取出导气管;⑥熄灭酒精灯;⑦连接仪器。正确的操作顺序是。
-
(3) 实验室制取CO2的化学方程式是,B和C装置都可用于制取CO2的发生装置,原因是。使用B装置制取气体时,长颈漏斗下端管口要伸入液面以下,其原因是。与B装置相比较,C装置的优点是。
-
(4) 上图中E装置有多种功能。若要检验CO2气体则瓶内装入的无色试剂的名称是,若用装置E、F组合来收集并测定O2的体积,应先在集气瓶中装满水,然后将导管(填“a”或“b”)端和导管c端连接。
|
发生装置 |
收集装置 |
洗气装置 |
|
| | |
-
(1) 写出B图中仪器甲的名称:。
-
(2) 某同学用加热高锰酸钾制取并收集较纯净的 O2应选用的发生装置和收集装置是(填字母序号),该反应的化学方程式是。若用过氧化氢溶液和MnO2制取氧气时,不能选C装置来控制反应的发生和停止的原因是。
-
(3) 实验小组同学取一定浓度的盐酸和石灰石反应制取CO2 , 反应的化学方程式为:。将生成的气体通入澄清石灰水中,未见变浑浊。为探究其原因,小组同学讨论作出如下探究:
-
(4) (提出猜想)A.石灰水完全变质;B.气体中有挥发出来的HCl气体。
(实验探究)小组同学设计并进行实验,请填写表中空格,完成实验报告。
实验步骤
实验现象
实验结论
I.用玻璃棒蘸取少量石灰水,,读出溶液pH
pH>7
石灰水未完全变质猜想A不成立
Ⅱ.将生成的气体通入硝酸酸化的硝酸银溶液中
产生白色沉淀
气体中有HCl猜想B成立
写出步骤Ⅱ中反应的化学方程式:。
-
(1) 氮气充入食品包装袋防腐,是因为。
-
(2) 宇航员太空行走时,需要“人造空气”供给呼吸。这种“人造空气”中含有体积分数为70%的氮气、20%以上的氧气、还有二氧化碳。“人造空气”中供给呼吸的物质是,“人造空气”中的氮气和空气中的氮气化学性质(填“相同”或“不同”)。
-
(3) 修建高铁过程中常用黑火药(含KNO3、S、C)进行工程爆破,黑火药爆炸时产生浓烟,推测该浓烟中含有K2S,从元素守恒角度说明理由。
-
(4) 最新研究表明,在光照条件下,利用Pt/TiO2为催化剂分解水可以得到过氧化氢和氢气,该反应的化学方程式为。
 B .
B .  C .
C . 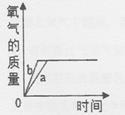 D .
D . 
-
(1) 炎热的夏天,街道上有雾炮车在向空中喷水,它比普通洒水车的降温、净化空气的效果更好,雾炮车净化空气主要针对的污染物是(填“有害气体”或“颗粒物”),请你写出两条减少大气污染的措施:,。

-
(2) 在污水处理中,生活污水中的难溶物可以通过的方法去除;
-
(3) 严禁乘客乘车携带易燃物,请举出生活中常见的一种易燃物,车用灭火器最好使用(填“泡沫”或“干粉”)灭火器。
| 选项 | 实验事实 | 结论 |
| A | 在常温常压下,硫在氧气中燃烧比在空气中燃烧更剧烈 | 该条件下,氧气的浓度越大,硫燃烧得越剧烈 |
| B | 在室温下,1L 水中大约可溶解 30mL 的氧气 | 室温下,氧气易溶于水 |
| C | 品红在静置的水中会扩散,且在热水中扩散得更快 | 分子在不停地运动,且温度越高,分子的运动速率越快 |
| D | 两块干燥的玻璃片,放在空气中的一块无明显变化,对着哈气的玻璃片上有无色液滴出现 | 呼出气体中水蒸气的含量比吸入空气中水蒸气的含量高 |
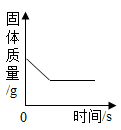 B .
B .  C .
C . 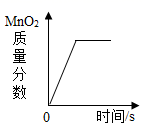 D .
D . 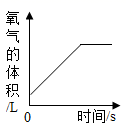
-
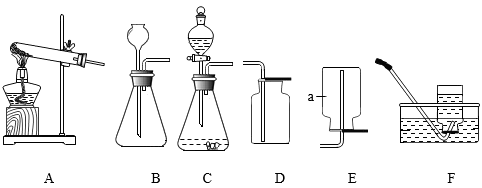
(1) 图中仪器a的名称是。
-
(2) 实验室用过氧化氢溶液制氧气的化学反应方程式为,若要收集较纯净的氧气,装置可选用(填字母)。
-
(3) 充分加热氯酸钾和1.5g二氧化锰制氧气,发生装置应选用(填字母)。将残留固体冷却至室温(20℃,该温度下,氯化钾的溶解度34g),称得其质量为4.6g,欲将其中的氯化钾全部溶解,至少应加入蒸馏水的体积约(填序号)。
a、10mL b、20mL c、30mL d、40mL
-
(4) 实验室制取CO2的化学反应方程式为,选用装置B时,长颈漏斗下管口应伸入液面以下,原因是:装置C与装置B相比,装置C的优点是。
-
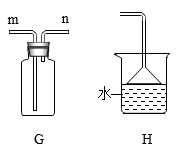
(5) 氨气是一种无色有刺激性气味的气体,密度小于空气,极易溶于水。实验室常用加热碱石灰与氯化铵混合物的方法制取氨气,发生装置可以选用,若选用G装置收集,应该从(填“m”或“n”)通入,还需在装置G后接装置H,H装置中倒置漏斗作用是。

-
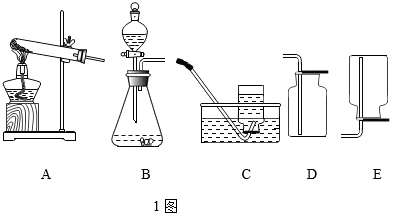
(1) 用A装置制取氧气,写出该反应的化学方程式。
-
(2) 用C装置制取二氧化碳比用B装置的突出优点是。
-
(3) 若用D装置检验二氧化碳,瓶内发生反应的化学方程式是。
-
(4) 实验室可用次氯酸钠固体粉末和浓盐酸在常温下反应制取氯气,氯气的密度比空气大、有毒,可与水反应生成酸。据此你认为实捡室制取较多量的氯气时,最好选用的发生装置是。
已知:乙炔(C2H2)是一种无色无味气体,极难溶于水,密度比空气略小。实验室里常用电石(CaC2)与水在常温下反应来制取。
-
(1) 实验室用氯酸钾制取一瓶较纯净的氧气,应选用的装置是(填序号,下同),反应的化学方程式为。
-
(2) 实验室用电石制取乙炔,选用的发生装置是,反应生成乙炔的同时会生成一种碱,反应的化学方程式是。
-
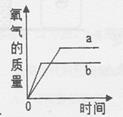
(3) 已知 CaCl2的水溶液呈中性。用2 图装置探究制取 CO2及其性质。实验开始时,向锥形瓶中加入一定量的盐酸。3 图表示实验过程中装置 G 和Ⅰ中溶液的 pH 变化曲线。
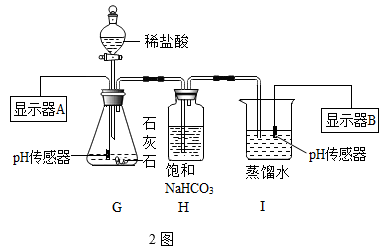

①装置 H 的作用为。
②t1时,锥形瓶中有固体残留,无气泡产生。根据显示器 A 的曲线判断盐酸(填“不足”、“过量”)。
③t1后,显示器 B 的曲线几乎无变化,其可能原因是。
A.二氧化碳的溶解已经达到饱和 B.t1时装置 G 中反应已停止,没有 CO2生成