学生实验 知识点题库
【提出问题】氯酸钾与二氧化锰混合加热后产生的气体成分是什么?
【查阅资料】
①氯酸钾与二氧化锰混合加热产生的气体只以单质形式存在;
②氯气 ![]() 是有刺激性气味的气体,能溶于水,能使湿润的淀粉碘化钾试纸变蓝。
是有刺激性气味的气体,能溶于水,能使湿润的淀粉碘化钾试纸变蓝。
【猜想假设】
猜想一:该气体为O2;猜想二:该气体为;猜想三:该气体为O2和Cl2的混合物。
【实验探究】
| 序号 | 操作 | 现象 | 结论 |
| 方案Ⅰ | 用排水集气法收集甲、乙两瓶气体,将带火星的木条伸入甲瓶,湿润的淀粉碘化钾试纸伸入乙瓶。 | 木条复燃,淀粉碘化钾试纸不变色 | 猜想成立 |
| 方案Ⅱ | 向上排空气法收集甲、乙两瓶气体,将带火星的木条伸入甲瓶,湿润的淀粉碘化钾试纸伸入乙瓶。 | 木条,淀粉碘化钾试纸为色 | 猜想三成立 |
【反思评价】
为什么两种方案得出的结论不一致?哪个是正确的?
①同学:方案Ⅰ结论不正确,其操作不合理,不合理之处是。
②老师:不需要进行实验,就能排除猜想一,理由是。
【拓展应用】
实验结束后,该组同学准备回收固体剩余物中的不溶物二氧化锰,实验的主要步骤为: ![]() 溶解、
溶解、 ![]() 、
、 ![]() 洗涤干燥。步骤
洗涤干燥。步骤 ![]() 中玻璃棒的作用是。
中玻璃棒的作用是。

-
(1) 甲同学利用上述仪器和药品可以制取二氧化碳,选择的仪器是(填序号), 反应的化学方程式是能用此法收集二氧化碳的原因是。
-
(2) 乙同学补充了一种仪器(填仪器名称),再利用上述仪器和药品制取氧气,选择的仪器是(填序号),反应的化学方程式是。
-
(3) 丙同学选用下图中装置⑨作为制取二氧化碳的发生装置,其中小试管的作用是 (写一点即可)。

-
(4) 丁同学选用下图中装置⑩制取氢气,此装置的优点是(写一点即可)。 添加稀硫酸时,液面最好添加到如图处(填字母“a”、“b"或“c”)。

 B .
B .  C .
C .  D .
D . 

-
(1) 溶解度随温度升高而减小的物质是。
-
(2) 10℃时A,B,C溶解度由大到小的顺序是。
-
(3) 将40℃时等质量的A,B,C的饱和溶液分别降温至30℃,溶质质量分数不变的是。
-
(4) 将30℃时65gA的饱和溶液升温至40℃,若要使溶液重新达到饱和,至少应加入gA。

-
(1) 写出仪器①的名称 。
-
(2) 若实验室制取氧气的发生装置选用B装置,反应的文字表达式为,若用向上排空气法收集氧气,验满的方法是。
-
(3) 小雪同学选用B装置并用排水法收集O2 , 下列操作正确的是(填字母)。
a 先检查装置气密性,再向大试管中加入固体
b 当导管口有连续气泡均匀冒出时,开始收集氧气
c 集气瓶中氧气收集满后,先用玻璃片在水下盖住集气瓶口,再将其移出水面
d 气体收集完毕后,先熄灭酒精灯,再将导管移出水面
-
(4) 实验室制取二氧化碳的文字表达式为,若用装置F收集二氧化碳,气体应从(填a或b)端进入。
-
(5) 当气体从a进入时,利用F装置还可以进行检验二氧化碳,则装置F中应该加入的试剂是。
-
(6) 实验室用二氧化锰和稀的双氧水制氧气,为达到控制反应速率的目的,发生装置A应该如何改进?请写出你的改进方案:。
(提出问题)淀粉能否作过氧化氢分解的催化剂?
(作出猜想)淀粉能作过氧化氢分解的催化剂。
-
(1) (实验验证)
实验步骤
实验现象
结论及解释
Ⅰ在盛有5mL 5%过氧化氢的试管中加入ag淀粉
产生大量能使带火星木条复燃的气体
产生的气体是
Ⅱ试管中重新加入的5mL 5%过氧化氢溶液,反应停止后过滤、洗涤、干燥、称量滤渣
①又产生大量使带火星木条复燃的气体
②滤渣质量为ag
①淀粉和在应前后均没有发生变化。
②淀粉能作过氧化氢分解的。
-
(2) 写出淀粉催化过氧化氢分解的文字表达式:。
-
(3) (拓展探究)探究小组想验证向上排空气法收集的氧气是否纯净,进行了几组实验,取几支集气瓶,分别装入其总体积不同含量的水用排水法收集氧气,恰好把几只集气瓶中的水排去。将带火星的木条依次插入集气瓶中,发现收集的氧气占容积的体积分数最低为35%时,木条复燃。
集气瓶中氧气的体积分数=收集的氧气占容积的体积分数+瓶中空气占容积的体积分数×%。
-
(4) 收集的氧气占容积的体积分数最低为35%时,可使带火星的木条复燃,这时集气瓶中氧气的体积分数是%(计算结果保留整数)。
 B . 过滤浑浊液体
B . 过滤浑浊液体  C . 点燃酒精灯
C . 点燃酒精灯  D . 给液体加热
D . 给液体加热 
-
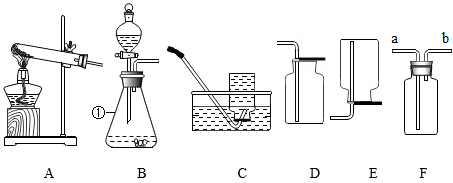
(1) 写出图中标有数字的仪器名称,①的名称是。
-
(2) 实验室用氯酸钾来制取氧气,选择的发生装置为(填序号),试管口稍向下倾斜的原因是,该反应的化学方程式为;为了收集较为纯净的氧气,最好选用的收集装置是(填序号);若改用高锰酸钾制取氧气,发生装置应作出的改进是:;实验结束时的正确操作顺序为:先,后;用向上排空气法收集氧气时的验满方法是。
-
(3) 实验室用石灰石和稀盐酸反应制取二氧化碳,选用的发生装置是(填序号), 该发生装置的优点是;若用装置F收集二氧化碳气体,气体应从(填a或b)端进入。
-
(4) 若用装置E收集某种气体,则该种气体应具备的性质。

-
(1) 8.9g不溶于水的物质是(填“纯净物”或“混合物”);D烧杯中所含溶质的化学式为。
-
(2) 列式计算,样品中硫酸铜的质量分数;配制上述实验所用的全部氢氧化钾溶液,需要质量分数为20%的氢氧化钾溶液的质量。
 B . 倾倒液体
B . 倾倒液体  C . 滴加液体
C . 滴加液体 

-
(1) 写出仪器名称:CF;
-
(2) 仪器A,B,C,E中能用仪器F直接加热的仪器(用字母序号填空,下同);
-
(3) 溶解、过滤、蒸发操作中都用到的仪器,在过滤操作中该仪器的作用是;
-
(4) 从用途上看,仪器C和E不同之处是。
-
(5) 某同学在使用仪器A给液体药品加热后发现其底部破裂,请你分析选出可能的原因有、(填两项)。
-
(1) 在实验桌上有如下几种气体发生装置和收集装置。请你参与实验并回答问题:

①实验室用石灰石与稀盐酸反应制取并收集二氧化碳,应选择的装置为 (填字母)。
②制取CO2的化学方程式为 ,组装气体发生装置后,应先检查装置的 ,再添加药品。
-
(2) 若用A,C装置制取并收集氧气,待收集满后要先 ;然后熄灭酒精灯。
-
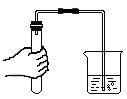
(3) 在探究Zn、Fe、Cu三种金属的有关性质时,进行了如图所示的实验,通过以上三个实验, (填“能”或“不能”)得出Zn、Fe、Cu三种金属的活动性顺序。

-
(4) 用粗木棍在涂有蜡的锌板上写“明”“和”两个字,露出下面的锌板。向“明”字上滴加CuSO4溶液,向“和”字上滴加稀硫酸。

①“明”字上的现象是 ;
②“和”字上产生气泡,用化学方程式解释 。
-
(5) 同学用某铁合金样品做了如下实验:称量11.4g样品,放入质量为40g的烧杯中,再往烧杯中加入200g稀硫酸,恰好完全反应(杂质不与酸反应,也不溶于水)。反应完毕后称量,烧杯及烧杯内物质总质量为251g。求所用稀硫酸的溶质质量分数 。
 B . 闻气味
B . 闻气味 C . 加入固体
C . 加入固体 D . 过滤
D . 过滤
 取用固体
B .
取用固体
B .  过滤浊液
C .
过滤浊液
C .  检查装置气密性
D .
检查装置气密性
D .  滴管清洗后放回原瓶
滴管清洗后放回原瓶


-
(1) 计算Na2CO3的质量为g,称量Na2CO3的仪器的名称是。
-
(2) 20℃时,Na2CO3的溶解度为21.5g,⑤中的溶液(填“是”或“不是”)该物质的饱和溶液。(忽略Na2CO3溶于水时溶液的温度变化)
-
(3) 将烧杯⑤中溶液倒入吸滤瓶的操作是,从橡胶管喷出大量液体的原因是。(用化学方程式表示)
-
(4) 酒精燃烧失火,可用干粉灭火器灭火。用干粉灭火器灭火的正确操作顺序是→→(填序号)。


-
(1) 注射器滴入液体后,写出A处玻璃管内发生反应的化学方程式。
-
(2) 一段时间后加热C处玻璃管,观察到B处玻璃管内红磷不燃烧而C处燃烧,由此可得到什么结论?



