第一节 金属的化学性质 知识点题库
两份铝片,第一份与足量盐酸反应,第二份与足量烧碱溶液反应.同温同压下放出相同体积的气体,则两份铝片的质量之比为( )
A . 1:1
B . 2:3
C . 3:2
D . 1:6
将铁粉放入由盐酸、MgCl2溶液、FeCl3溶液、CuCl2溶液组成的混合液中,充分反应后,铁粉有剩余,则溶液含有大量的阳离子是( )
A . Cu2+和Fe2+
B . H+和Cu2+
C . Fe3+和Fe2+
D . Fe2+和Mg2+
X、Y、Z、W有如图所示的转化关系,则X、W可能是( )
①C、O2 ②AlCl3、NaOH ③Fe、HNO3 ④CO2、NaOH.
![]()
A . ①②③
B . ①②
C . ③④
D . ①②③④
某同学研究铝及其化合物的性质时设计了如下两个实验方案:
方案①:2.7g Al  X溶液
X溶液  Al(OH)3沉淀
Al(OH)3沉淀
方案②:2.7g Al  Y溶液
Y溶液  Al(OH)3沉淀
Al(OH)3沉淀
NaOH溶液和盐酸的浓度均是3mol•L﹣1 , 如图所示,向X溶液和Y溶液中分别加入NaOH溶液和盐酸时产生沉淀的物质的量与加入盐酸和氢氧化钠溶液体积之间的关系,下列说法不正确的是( )

A . b曲线表示的是向X溶液中加入NaOH溶液
B . 在O点时两方案中所得溶液浓度相等
C . a、b曲线表示的反应都是非氧化还原反应
D . X溶液显酸性,Y溶液显碱性
将钠投入下列溶液中,反应的剧烈程度由强到弱的是( )
①水 ②乙醇 ③0.5mol•L﹣1盐酸 ④0.1mol•L﹣1 FeCl3溶液.
A . ④③②①
B . ④③①②
C . ③④①②
D . ①③④②
下列有关元素及其化台物的说法正确的是( )
A . 水蒸气通过灼热的铁粉生成四氧化三铁和氢气
B . FeCl3既能通过化台反应制得,也能通过金属与酸的置换反应制得
C . Na在空气中长期放置最终变为Na2CO3粉末
D . 向KClO3溶液中滴加AgNO3溶液得到白色AgCl沉淀
等物质的量的Na2CO3和NaHCO3分别与足量的同浓度盐酸充分反应,其中( )
A . Na2CO3放出的CO2多
B . NaHCO3放出的CO2多
C . Na2CO3放出CO2的速率快
D . NaHCO3放出CO2的速率快
金属能导电是因为它()
A . 表面富有光泽
B . 有可成键的电子
C . 有金属离子
D . 有自由运动的电子
有A、B、C、D四种常见的金属单质,A的焰色为黄色;B为红色固体,锈蚀时变为绿色;C在空气中加热熔化但不滴落;D在氧气中燃烧,火星四射,生成黑色固体。
根据以上信息回答下列问题:
-
(1) 写出对应化学式:A,B,C,D。
-
(2) 写出下列化学方程式:
①A在空气中燃烧;
②B与AgNO3 溶液:;
③C与氢氧化钠溶液:。
下列说法正确的是( )
A . Fe3+的水溶液呈红褐色,Fe2+的水溶液呈浅绿色
B . Fe3+具有氧化性,Fe2+具有还原性
C . Fe3+的溶液中滴入含KSCN的溶液,立即出现红色沉淀
D . 铁粉可以和水蒸气在高温下反应生成Fe2O3
取一块金属钠放在燃烧匙里加热,观察到下列现象:①金属先熔化;②在空气中燃烧,表面变暗;③燃烧后得到白色固体;④燃烧后火焰为黄色;⑤燃烧后生成浅黄色固体物质。描述正确的是( )
A . ①②
B . ①②③
C . ①④
D . ①④⑤
如图中横坐标为加入反应物的物质的量,纵坐标为产生沉淀的物质的量.下列选项编号对应的曲线编号错误的是( )

A . 向NaAlO2溶液中逐渐滴入HCl至过量
B . 向澄清石灰水中通入SO2至过量
C . 向含有盐酸的AlCl3溶液中滴入NaOH溶液至过量
D . 向含有等物质的量的Ca(OH)2、KOH的混合溶液中通入CO2至过量
在给定条件下,下列选项所示的物质间转化均能实现的是( )
A .  B .
B .  C .
C .  D .
D . 
 B .
B .  C .
C .  D .
D . 
下列物质中既能与稀H2SO4反应, 又能与NaOH溶液反应的是( )
①NaHCO3 ②Al2O3 ③Al(OH)3 ④Al ⑤Na2CO3
A . ①③④
B . ①②③④
C . ③④
D . 全部
下列说法错误的是( )
A .  使溴水褪色是因为
使溴水褪色是因为  具有氧化性
B . 钠与氧气反应的产物与反应条件有关
C . 还原铁粉与浓硫酸共热,生成能使品红溶液褪色的气体
D . 为除去
具有氧化性
B . 钠与氧气反应的产物与反应条件有关
C . 还原铁粉与浓硫酸共热,生成能使品红溶液褪色的气体
D . 为除去 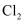 中的
中的 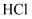 ,可将气体通入饱和食盐水
,可将气体通入饱和食盐水
 使溴水褪色是因为
使溴水褪色是因为  具有氧化性
B . 钠与氧气反应的产物与反应条件有关
C . 还原铁粉与浓硫酸共热,生成能使品红溶液褪色的气体
D . 为除去
具有氧化性
B . 钠与氧气反应的产物与反应条件有关
C . 还原铁粉与浓硫酸共热,生成能使品红溶液褪色的气体
D . 为除去 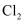 中的
中的 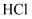 ,可将气体通入饱和食盐水
,可将气体通入饱和食盐水
下列“类比”合理的是( )
A . Fe与Cl2反应生成FeCl3 , 则Fe与I2反应生成FeI3
B . 钠在空气中加热生成Na2O2 , 则金属锂在空气中加热也生成Li2O2
C . NH3与HCl反应生成NH4Cl,则N2H4与HCl反应生成N2H6Cl2
D . Na2O2与CO2反应生成Na2CO3和O2 , 则Na2O2与SO2反应生成Na2SO3和O2
Na投入水中发生剧烈反应,并有H2生成;装运金属钠的包装箱应贴的图标是( )
A . 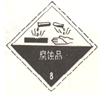 腐蚀品
B .
腐蚀品
B .  爆炸品
C .
爆炸品
C .  遇湿易燃品
D .
遇湿易燃品
D .  氧化剂
氧化剂
 腐蚀品
B .
腐蚀品
B .  爆炸品
C .
爆炸品
C .  遇湿易燃品
D .
遇湿易燃品
D .  氧化剂
氧化剂
下列有关钠及其化合物的说法错误的是( )
A . 侯氏制碱法制得的“碱”是碳酸钠
B . 钠与氧气反应的产物与反应条件有关
C . NaHCO3的热稳定性比Na2CO3强
D . 碳酸钠和碳酸氢钠可用作食用碱或工业用碱
某工厂的废金属屑中主要成分为Cu、Fe和Al,此外还含有少量Al2O3和Fe2O3 , 为探索工业废料的再利用,某化学兴趣小组设计了如下实验流程,用该工厂的合金废料制取氯化铝、绿矾晶体(FeSO4·7H2O)和胆矾晶体。

请回答:
-
(1) 写出步骤Ⅰ反应的离子方程式:、。
-
(2) 试剂X是,溶液D是。
-
(3) 在步骤Ⅱ时,用如图装置制取CO2并通入溶液A中。一段时间后,观察到烧杯中产生的白色沉淀会逐渐减少。为避免固体C减少,可采取的改进措施是。

-
(4) 由固体F制取硫酸铜溶液,通常有两种方案:
方案一:将固体F在加热条件下与浓硫酸反应;
方案二:将固体F投入热的稀硫酸中,然后不断鼓入空气。
方案一的缺点为:。
请写出方案二中发生反应的化学方程式:。
下列推理合理的是( )
A . NaCl固体与浓H2SO4 加热可制HCl, 则NaI固体与浓H2SO4 加热制HI
B . Na2O2 与CO2反应生成Na2CO3和O2 , 则Na2O2与SO2反应生成Na2SO3和O2
C . 实验室可利用AlCl3与足量氨水反应来制备Al(OH)3 , 则也可利用CuCl2与足量氨水反应生成Cu(OH)2
D . Fe与S反应生成FeS,则Cu与S反应生成Cu2S
最近更新



