第一节 元素周期表 知识点题库
下列微粒中:①13Al3+② ③F﹣ , ④
③F﹣ , ④ 其核外电子数相同的是( )
其核外电子数相同的是( )
A . ①②③
B . ②③④
C . ①②④
D . ①③④
同温同压下,等体积的两容器内分别充满由14N、13C、18O三种原子构成的一氧化氮和一氧化碳,两容器含有的( )
A . 分子数和气体质量均不同
B . 分子数和电子数均相同
C . 质子数和中子数均相同
D . 分子数、原子数和中子数均相同
下列说法不正确的是( )
①质子数相同的粒子一定属于同一种元素
②同一元素的核素种数由中子数决定
③同位素的化学性质几乎相同
④质子数相同、电子数也相同的两种粒子,不可能是一种分子和一种离子
⑤Cl2中35Cl与37Cl两种核素的个数之比与HCl中35Cl与37Cl的个数之比相等.
A . ③
B . ④
C . ②⑤
D . ①
下列有关碱金属的说法中,不正确的是( )
A . IA族元素都是碱金属元素
B . K的还原性强于Na
C . Na和Na+灼烧时都能使火焰呈黄色
D . Na在空气中燃烧时生成Na2O2
“8•12”天津港危化仓库爆炸,造成生命、财产的特大损失.据查危化仓库中存有大量的钠、钾,硝酸铵和氰化钠(NaCN).请回答下列问题:
-
(1) 钠、钾着火,下列可用来灭火的是A . 水 B . 泡沫灭火器 C . 干粉灭火器 D . 细沙盖灭
-
(2) 硝酸铵在常温下比较稳定,但在强热的条件下会发生爆炸.可以得到一种无色气体和另一种红棕色的气体等物质,请写出该反应的方程式;若标况下产生13mol的气体生成,则转移的电子的物质的量为.
-
(3) 硝酸铵和碱溶液反应生成的氨气,可以形成氨气﹣﹣空气燃料电池.其反应原理为NH3+O2→N2+H2O(未配平),则电解质溶液应显性(填“酸性”、“中性”或者“碱性”,负极的电极方程式为:.
-
(4) 以TiO2为催化剂,可以用NaClO将CN﹣离子氧化成CNO﹣ . 在酸性条件下,NaCNO继续与NaClO反应生成N2、CO2、NaCl等. 请写出NaCNO在酸性条件下被NaClO氧化的离子方程式.
下列微粒半径由大到小的排列是( )
A . Ca,Mg,Na
B . Cl﹣ , S2﹣ , O2﹣
C . P3﹣ , S2﹣ , Cl﹣
D . K+、Cl﹣ , S2﹣
下列判断正确的是( )
A . 核电荷数:Al<Na
B . 金属性:Na>Al
C . 原子序数:Na>Cl
D . 原子半径:Cl>Na
下列各组中属于同位素关系的是( )
A . 金刚石与石墨
B . T2O与H2O
C . 40K与39K
D . 16O与16O2-
已知短周期元素的离子aA2+、bB+、cC3-、dD-都具有相同的电子层结构,则下列叙述正确的是( )
A . 原子序数 d>c>b>a
B . 原子半径:r(A)>r(B)>r(D)>r(C)
C . 单质的还原性:A>B>D>C
D . 离子半径:r(C3-)> r(D-)> r(B+)> r(A2+)
下列各组中两种微粒所含电子数不相等的是( )
A . H3O+和OH-
B . CO和N2
C . NH3和 F-
D . CH4和NO
硒是人体必需的微量元素,右图是硒在周期表中的信息,关于硒元素的说法错误的是( )

A . 位于第四周期
B . 质量数为34
C . 原子最外层有6个电子
D . 相对原子质量为78.96
如图为周期表中短周期的一部分,若X原子最外层电子数比次外层电子数少3,则下列说法正确的是( )
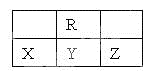
A . X的氢化物比R的氢化物稳定
B . 原子半径大小顺序是Z>Y>X
C . Y、R形成的化合物YR2能使KMnO4溶液褪色
D . X、Z可形成化合物XZ5 , 分子中各原子均满足最外层8电子结构
下图表示碱金属的某些性质与核电荷数的变化关系, 下列各性质中不符合图示关系的是( )

A . 还原性
B . 与水反应的剧烈程度
C . 阳离子的氧化性
D . 原子半径
科学家利用四种原子序数依次递增的短周期元素W、X、Y、Z“组合”成一种超分子,具有高效的催化性能,其分子结构示意图如图。W、X、Z分别位于不同周期,Z的原子半径在同周期元素中最大。(注:实线代表共价键,其他重复单元的W、X未标注)下列说法错误的是( )

A . Y单质的氧化性在同主族中最强
B . 离子半径:Z>Y
C . Z与Y可组成多种离子化合物
D . 氢化物的热稳定性:Y>X
我国成功研制的铯(133Cs)原子喷泉钟,使我国时间频率基准的精度从30万年不差1秒提高到600万年不差1秒。已知该铯原子的核外电子数为55,则该原子的中子数为( )
A . 23
B . 55
C . 78
D . 133
几种短周期元素的原子半径及某些化合价见下表。分析判断下列说法正确的是( )
| 元素代号 | A | B | D | E | X | Y | Z | W |
| 化合价 | -1 | -2 | +4、-4 | -1 | +5、-3 | +3 | +2 | +1 |
| 原子半径/nm | 0.071 | 0.074 | 0.077 | 0.099 | 0.110 | 0.143 | 0.160 | 0.186 |
A . A的单质能将E单质从YE3的溶液中置换出来
B . A,Y,W的离子半径由大到小顺序是A>W>Y
C . X元素的单质不存在同素异形体
D . Z在DB2中燃烧生成两种化合物
某种化合物(如图)由W、X、Y、Z四种短周期元素组成,其中W、Y、Z分别位于三个不同周期,Y核外最外层电子数是W核外最外层电子数的二倍;W的最高价氧化物对应的水化物具有两性,W、X、Y三种简单离子的核外电子排布相同。下列说法正确的是( )
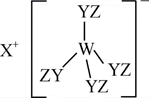
A . X与Y、Y与Z均可形成X2Y、Z2Y2型化合物
B . 离子半径:X>W>Y>Z
C . X、Y、Z组成的化合物中只含有离子键
D . 常温常压下熔点:X2Y<Z2Y
已知短周期元素的离子aW2+、b X+、cY2-、d Z- 具有相同的电子层结构,下列正确的是( )
A . 原子序数:a > b > c > d
B . 离子的还原性:Y2- > Z-
C . 氢化物的稳定性H2Y > HZ
D . 原子半径X < W
等物质的量的氢化锂(7LiH)、氘化锂(7LiD)、氚化锂(7LiT),肯定不同的是( )
A . 质子数
B . 中子数
C . 化学键类型
D . 化学性质
短周期主族元素W、X、Y、Z的原子序数依次增大,W、Z同主族,W、X、Y最外层电子数之和等于11,W、X、Y三种元素形成的化合物的水溶液可用作木材防火剂。下列说法错误的是( )
A . 离子半径: B . W与X形成的化合物中只含有离子键
C . Y的简单气态氢化物的稳定性比Z的弱
D . X、Z形成的化合物能破坏水的电离平衡
B . W与X形成的化合物中只含有离子键
C . Y的简单气态氢化物的稳定性比Z的弱
D . X、Z形成的化合物能破坏水的电离平衡
 B . W与X形成的化合物中只含有离子键
C . Y的简单气态氢化物的稳定性比Z的弱
D . X、Z形成的化合物能破坏水的电离平衡
B . W与X形成的化合物中只含有离子键
C . Y的简单气态氢化物的稳定性比Z的弱
D . X、Z形成的化合物能破坏水的电离平衡
最近更新



