第二单元 化学与资源开发利用 知识点题库
下列化学工业中,未涉及原料循环使用的是( )
A . 侯德榜制碱法
B . 索尔维制碱法
C . 工业电解饱和食盐水
D . 工业炼铁
下列有关实验的叙述,正确的是( )
A . 分馏石油时,温度计的水银球必须插入液面以下
B . 制备乙酸乙酯时,加料顺序为浓硫酸、乙醇、乙酸
C . 配制银氨溶液时,将稀氨水慢慢滴加到稀硝酸银溶液中,产生白色沉淀后继续滴加,直至沉淀刚好溶解为止
D . 实验室可用苯和溴水在Fe作催化剂的情况下制备溴苯
近些年来,我国的石油进口量逐渐增加.石油被称为“国民经济的血液”,它既是重要的战略资源和能源,也是十分重要的化工原料.请解答下列试题:
-
(1) 请将石油产品汽油、柴油、煤油、沥青、液化石油气按其组成物质分子中碳原子数递增的顺序排列
-
(2) 乙烯是石油裂解的主要产物之一,将乙烯通入溴的四氯化碳溶液中,观察到的现象是 ;其反应方程式为 .乙烯在一定条件下发生加聚反应的化学方程式是 ,其产物的名称是 ; 乙烯对水果具有 功能.
城市使用的燃料,现大多为煤气、液化石油气.煤气的主要成分是CO和H2的混合气体,它有煤炭与水蒸气在高温下反应制得,故又称水煤气.试回答:
-
(1) 写出制取水煤气的主要化学方式 ,该反应是 反应(填吸热、放热).
-
(2) 设液化石油气的主要成分为丁烷(C4H10),其充分燃烧后产物为C02和H2O,试比较完全燃烧等质量的C4H10及CO所需的氧气的质量比 (结果保留1位小数).
有关煤的综合利用如图所示.下列说法正确的是( )

A . 煤和水煤气均是二次能源
B . 煤中含有苯、甲苯、二甲苯等有机物
C . ①是将煤在空气中加强热使其分解的过程
D . B为甲醇或乙酸时,原子利用率均达到100%
天然海水中主要含有Na+、K+、Ca2+、Mg2+、Cl﹣、SO42﹣、Br﹣、CO32﹣、HCO3﹣等离子.火力发电燃煤排放的含SO2的烟气可利用海水脱硫,其工艺流程如图所示:  下列说法错误的是( )
下列说法错误的是( )
 下列说法错误的是( )
下列说法错误的是( )
A . 天然海水pH≈8的原因是由于海水中的CO32﹣、HCO3﹣水解
B . “氧化”是利用氧气将H2SO3、HSO3﹣、SO32﹣等氧化生成SO42﹣
C . “反应、稀释”时加天然海水的目的是中和、稀释经氧化后海水中生成的酸
D . “排放”出来的海水中SO42﹣的物质的量浓度与进入吸收塔的天然海水相同
海水是巨大的资源宝库,从海水中提取食盐和溴的过程如图1:

-
(1) 请列举海水淡化的两种方法:、.
-
(2) 步骤I中己获得Br2 , 步骤II中又将Br2还原为Br﹣ . 其目的是.
-
(3) 步骤II用SO2水溶液吸收Br2 , 吸收率可达95%.有关反应的离子方程式为.
-
(4) 某化学研究性学习小组为了了解从工业溴中提纯溴的方法.查阅了有关资料知:Br2的沸点为59℃.微溶于水,有毒并有强腐蚀性.他们参观生产过程后.画了如图2装置简图:

请你参与分析讨论:
①图中仪器B的名称是.
②整套实验装皿中仪器连接均不能用橡胶塞和橡胶管.其原因是.
③实验装置气密性良好,要达到提纯溴的目的,操作中如何控制关键条件?.
④C中液体颜色为.为除去该产物中仍残留的少量Cl2 , 可向其中加入NaBr,溶液,充分反应后.再进行的分离操作是.
实验室从含碘废液(除H2O外,含有CCl4、I2、I﹣等)中回收碘,其实验过程如下:

-
(1) 向含碘废液中加入稍过量的Na2SO3溶液,将废液中的I2还原为I﹣ , 其离子方程式为;该操作将I2还原为I﹣的 目的是.
-
(2) 操作X的名称为.
-
(3) 氧化时,在三颈烧瓶中将含I﹣的水溶液用盐酸调至pH约为2,缓慢通入Cl2 , 在40℃左右反应(实验装置如图所示).实验必须控制在较低温度下进行的原因是;
仪器a、b的名称分别为:a、b;
仪器b中盛放的溶液为.

-
(4) 已知二氧化氯为黄绿色易溶于水的气体,是高效、低毒的消毒剂和水处理剂.现用ClO2氧化酸性含I﹣废液以回收碘.
①写出ClO2氧化I﹣的离子方程式;
②若处理含相同物质的量的I﹣酸性废液以回收碘,所需Cl2的物质的量是ClO2的倍.
若将海水淡化作饮用水使用,下列方法在原理上完全不可行的是( )
A . 加明矾使海水中的盐分沉淀而淡化
B . 利用太阳能使海水蒸馏淡化
C . 利用电渗析法可以获取淡化的饮用水
D . 将海水通过离子交换树脂,以除去所含离子
给定条件下,下列选项中所示的物质间转化,均能一步实现的是( )
①SO2  (NH4)2SO3
(NH4)2SO3  (NH4)2SO4
(NH4)2SO4
②煤 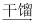 焦炭
焦炭  (CO+H2)
(CO+H2) 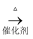 CH3OH
CH3OH
③C4H10  C2H4
C2H4![]()
④(C6H10O5)n(淀粉) 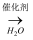 C6H12O6(葡萄糖)
C6H12O6(葡萄糖) 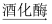 C2H5OH
C2H5OH
A . ①②③④
B . ①③④
C . ③④
D . ①②
化学无处不在,下列有关说法错误的是( )
A . 纽扣银锌电池体型小,含有害物质少,用后可以随意丢弃
B . 采用外加电流的阴极保护法可防止钢铁锈蚀
C . 裂化汽油与直馏汽油的成分不完全相同
D . 色谱法可用于分离、提纯有机物
下列叙述错误的是( )
A . 油脂、淀粉、蔗糖和蛋白质在一定条件都能发生水解反应
B . 甲烷和苯都不能与溴水、酸性高锰酸钾溶液发生反应,但苯不属于饱和烃
C . 将红热的铜丝迅速插入乙醇中,可观察到铜丝表面变红,并能闻到刺激性气味
D . 煤中含有苯、甲苯,可用先干馏后分馏的方法将它们分离出来
从海带中提取碘,设计如下实验方案,下列说法错误的是( )

A . 步骤①的操作方法:灼烧和溶解
B . 步骤①需用的主要仪器:坩埚和烧杯
C . 步骤③的试剂a必须是氧化剂
D . 步骤④的试剂b可选用酒精
化学与工业生产有着密切的联系,下列说法中正确的是( )
A . 与12C互为同素异形体的14C可用作文物鉴定
B . 因铝的化学性质活泼,故不能用铝槽车储运浓H2SO4
C . 海水淡化的方法有蒸馏法、电渗析法、明矾净水等方法
D . 石油裂解、煤的气化等过程中都包含化学变化
下列有关工业生产中,不正确的是( )
A . 制氯气:电解饱和食盐水
B . 硫酸工业:在接触室中SO2氧化为SO3
C . 炼铁:用CO在高温下还原铁矿石中的铁
D . 制钛:钠从四氯化钛水溶液中置换出钛
下列说法正确的是( )
A . 用石灰石-石膏法对燃煤烟气进行脱硫,最终生成CaSO3
B . 过量的Fe在干燥的氯气中点燃生成FeCl2
C . 等物质的量的氯气和甲烷在光照条件下反应能制得纯净的CH3Cl
D . 用焦炭在高温下还原二氧化硅制得粗硅的同时产生大量CO
人类的生产、生活离不开化学。
-
(1) 铝粉与某些金属氧化物组成的混合物叫铝热剂,铝热剂在高温下发生的反应叫铝热反应,如:2Al+Fe2O3
 2Fe+Al2O3 , 反应发生时放出大量的热。
2Fe+Al2O3 , 反应发生时放出大量的热。 ①“铝热反应”属于四种基本反应类型中的反应。
②信息中的“某些”指(填“比铝活泼”“比铝不活泼”或“任意”)。
③试写出铝粉与MnO2发生的铝热反应方程式:。
-
(2) 从海水中提取溴的工业流程如图:
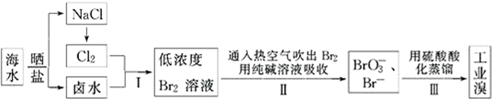
①步骤I中发生反应的离子方程式为。
②步骤II用热空气吹出的Br2被纯碱溶液吸收时,则被氧化和被还原的Br2的物质的量之比为。
-
(3) 海带中含有丰富的碘元素,某化学研究性学习小组用如图流程从海水中提取碘:

①若操作I用H2O2溶液(稀硫酸酸化)完成碘元素的转化,则反应的离子方程为。
②操作II的名称为、,此过程中可以选用的有机溶剂是(填一种)。
下列有关海洋资源的综合利用说法错误的是( )
A . 从海水中提取溴单质的工艺流程中包含了富集过程
B . 海底的资源非常丰富,含有铁、锰、钴等多种金属结核矿
C . 海水的淡化方法主要有蒸馏法、离子交换法、过滤法等
D . 开发海洋资源不能破坏环境,应遵循绿色环保的思想
下列说法正确的是( )
A . HF的电离方程式为:HF+H2O  H3O++F-
B . HCl的电子式为
H3O++F-
B . HCl的电子式为  C . 聚乙烯塑料、人造丝、尼龙绳都是合成材料
D . 煤的干馏、石油的分馏都是物理变化
C . 聚乙烯塑料、人造丝、尼龙绳都是合成材料
D . 煤的干馏、石油的分馏都是物理变化
 H3O++F-
B . HCl的电子式为
H3O++F-
B . HCl的电子式为
化学与生产生活密切相关,下列说法正确的是( )
A . 95%的酒精比75%的酒精消毒效果更好
B . 石油的分馏、裂化、裂解都属于化学变化
C . 对废旧电池进行回收处理,主要是为了环境保护和变废为宝
D . 食品检验是保证食品安全的重要措施,二氧化硫的含量不属于食品安全检测指标
最近更新



