实验1-1 蓝瓶子实验 知识点题库
为了除去粗盐中的CaCl2、MgCl2、Na2SO4及泥沙,可将粗盐溶于水,通过如下几个实验步骤,可制得纯净的食盐水:①加入稍过量的Na2CO3溶液;②加入稍过量的NaOH溶液;③加入稍过量的BaCl2 溶液;④滴入稀盐酸至无气泡产生;⑤过滤,不正确的操作顺序是( )
A . ⑤③②①⑤④
B . ⑤③①②⑤④
C . ⑤②③①⑤④
D . ⑤②①③⑤④
物质的加热是中学化学实验的重要基本操作.加热的方式常用的有三类:(1)直接在酒精灯上加热;(2)通过水浴加热;(3)通过石棉网用酒精灯加热.以下7个化学实验:
①浓盐酸与二氧化锰制取氯气;②苯与浓硝酸、浓硫酸的混合酸反应制硝基苯;③电石与水反应制乙炔;④乙醇与浓硫酸制取乙烯;⑤乙醛溶液与银氨溶液的银镜反应;⑥甲醛溶液与新制氢氧化铜悬浊液反应.
-
(1) Ⅰ、用酒精灯直接加热的有 (填序号,下同).
-
(2) Ⅱ、用酒精灯通过石棉网加热的有
-
(3) Ⅲ、通过水浴加热的有 ,其好处是
天津港“8.12”瑞海公司危险品仓库特大火灾爆炸事故,其二次爆炸威力巨大.据推测可能是由于某物质遇水燃烧而引发的连锁反应.下列常见危险品中最有可能具有这种性质的是( )
A . KNO3
B . NH4NO3
C . CaC2
D . P4(白磷)
以下是一些常用的危险品标志,装运乙醇的包装箱应贴的图标是( )
A .  B .
B .  C .
C . 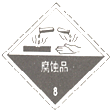 D .
D . 
 B .
B .  C .
C .  D .
D . 
2015年8月12日,天津滨海新区一危险品仓库发生爆炸,其中有一种危险品是氰化钠(NaCN),它遇水后会释放出剧毒物质氰化氢气体.盛装NaCN的罐上应该贴有的危险化学品标识是( )
A .  B .
B .  C .
C .  D .
D . 
 B .
B .  C .
C .  D .
D . 
下列仪器:①锥形瓶,②蒸馏烧瓶,③漏斗,④燃烧匙,⑤天平,⑥分液漏斗,⑦胶头滴管.常用于物质分离的是( )
A . ①③⑤
B . ②④⑦
C . ①②⑥
D . ②③⑥
实验是化学研究的基础,关于下列各实验装置图的叙述中,正确的是( )
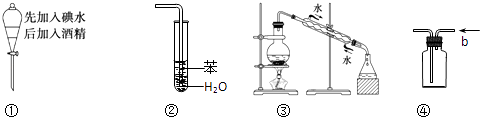
A . 溶液上层无色,下层紫红色
B . 装置②可用于吸收HCl气体,并防止倒吸
C . 装置③可用于制取蒸馏水
D . 装置④b口进气可收集H2、CO2等气体
下列说法正确的是 ( )
A . 配制一定物质的量浓度的NaOH溶液时,NaOH固体溶解后未恢复到室温就转移、定容,所配制的溶液浓度偏大
B . 用广范pH试纸测得氯水的pH为3
C . 用托盘天平称取5.86g食盐
D . 用细铁丝放在酒精灯火焰上灼烧至无色,然后蘸取少量待测液,透过蓝色钴玻璃观察火焰呈紫色,说明待测液中一定含有K+ , 没有Na+
下列实验操作和数据记录都正确的是( )
A . 用10mL量筒量取9.2 mL NaCl溶液
B . 用干燥的广泛pH试纸测稀盐酸的pH=3.2
C . 用25 mL碱式滴定管量取16.60 mL高锰酸钾溶液
D . 用托盘天平称量时,将NaOH固体放在左盘内的滤纸上,称得质量为10.2 g
下列各组混合物中能用分液漏斗进行分离的是( )
A . 乙醇和水
B . 苯和甲苯
C . 溴乙烷和水
D . 乙醇和乙酸
重铬酸钾(K2Cr2O7)在皮革、火柴、印染化学、电镀等方面应用广泛。回答下列问题:
-
(1) 酒驾醉驾危害社会安全,早期测定是否饮酒的方法是重铬酸钾法溶液橙红色变为绿色(Cr3+)则表明已经饮酒。写出重铬酸钾法检验饮酒的化学方程式:。
-
(2) 用铬铁矿(FeO·Cr2O3 , 含Al2O3杂质)为原料制备重铬酸钾的工艺:

已知:i.2CrO42-+2H+
 Cr2O72-+H2O;ii.Ksp[Al(OH)3]=1.3×10-33;iii.有关物质的溶解度曲线如图:
Cr2O72-+H2O;ii.Ksp[Al(OH)3]=1.3×10-33;iii.有关物质的溶解度曲线如图:
①上述工艺流程图中的操作I的主要反应为:
2FeO·Cr2O3+4Na2CO3+7NaNO3
 4Na2CrO4+Fe2O3+4CO2↑+7NaNO2 , 另外一个反应的化学方程式是。
4Na2CrO4+Fe2O3+4CO2↑+7NaNO2 , 另外一个反应的化学方程式是。②滤渣2的成分是(写化学式),常温时,其滤液中,c(Al3+)=mol·L-1
③工艺流程图中,操作“调节pH”的作用是。
④操作Ⅲ,加入KCl的目的是;实验室中,操作IV用到的玻璃仪器有酒精灯、烧杯、。
⑤为测定某次生产制备的K2Cr2O7的含量,某科研人员取m g产品样品,用500mL容量瓶配制成一定浓度的溶液然后取25.00mL,置于锥形瓶,再滴加2mol·L-1稀硫酸然后再加1.1gKI,充分溶解、反应锥形瓶中的铬元素完全以Cr3+存在,加指示剂,用标准液Na2S2O3溶液滴定,达到滴定终点,消耗30.00mL0.0250mol·L-1的标准液。则该次生产的样品中K2Cr2O7含量为%。(已知:2Na2 S2 O3+I2=Na2 S4O6+2NaI)
下列有关仪器的使用方法或实验操作正确的是( )
A . 用坩埚灼烧干海带制海带灰
B . 蒸馏时,温度计水银球插入液面以下
C . 用长颈漏斗分离CCl4萃取碘后的水层与有机层
D . 用容量瓶配制溶液时,若加水超过刻度线,用胶头滴管吸出多余液体
完成下列实验所选择的装置或仪器(夹持装置部分已略去)正确的是( )
A . 分离Na2CO3溶液和CH3CH2OH  B . 除去Cl2中含有的少量HCl
B . 除去Cl2中含有的少量HCl  C . 做SO2与NaOH溶液的喷泉实验
C . 做SO2与NaOH溶液的喷泉实验  D . 用NaOH标准溶液滴定锥形瓶中的盐酸
D . 用NaOH标准溶液滴定锥形瓶中的盐酸 
 C . 做SO2与NaOH溶液的喷泉实验
C . 做SO2与NaOH溶液的喷泉实验  D . 用NaOH标准溶液滴定锥形瓶中的盐酸
D . 用NaOH标准溶液滴定锥形瓶中的盐酸 
下列仪器不能加热的是( )
A . 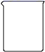 B .
B .  C .
C .  D .
D . 
下列说法错误的是( )
A . 纸层析法只能用于分离有色物质,否则无法看到色斑
B . 移液管或者滴定管可精确量取一定体积的溶液
C . 红外光谱仪用于测定有机化合物中的基团
D . 氯酸钾、高锰酸钾等强氧化剂或其混合物不能研磨
化学在生产和日常生活中有着重要的应用,下表中用途与其性质或原理错误的是( )
|
选项 |
现象或事实 |
解释 |
|
A |
Na2O2常用于潜水艇或呼吸面具的供氧剂 |
Na2O2与H2O、CO2反应产生O2 |
|
B |
常用铁盐做净水剂 |
Fe3+生成吸附能力强的Fe(OH)3胶体 |
|
C |
FeCl3溶液可用于刻制印刷铜电路板 |
发生反应2Fe3++Cu=2Fe2++Cu2+ |
|
D |
在医疗上烧碱可用于治疗胃酸过多 |
烧碱可与胃酸反应 |
A . A
B . B
C . C
D . D
下列叙述正确的是( )
A . 分散质微粒直径的大小关系:溶液>胶体>浊液
B . 把饱和FeCl3溶液滴到氢氧化钠溶液中加热煮沸能够制取氢氧化铁胶体
C . 利用丁达尔效应可以区别溶液与胶体
D . 胶体的本质特征是具有丁达尔效应
下列仪器使用前必须检僉是否漏水的是( )
A .  B .
B .  C .
C .  D .
D . 
 B .
B .
配制100mL0.1mol/L的NaCl溶液,不需要使用的仪器是( )
A . 烧杯
B . 胶头滴管
C . 100mL容量瓶
D . 漏斗
某同学用如图所示的装置(部分)制备乙酸乙酯,操作如下:连接实验装置,检查气密性。向圆底烧瓶中加入无水乙醇、浓硫酸、冰醋酸的混合物,并加入沸石,加热圆底烧瓶。充分反应后将该装置改成蒸馏装置,蒸馏获取粗产品。在获得的粗产品中加入饱和 溶液,充分反应至无气泡逸出,将混合液倒入分液漏斗中,振荡、静置,收集下层液体即得粗制乙酸乙酯。该实验操作及制备装置中存在的错误共有几处?( )
溶液,充分反应至无气泡逸出,将混合液倒入分液漏斗中,振荡、静置,收集下层液体即得粗制乙酸乙酯。该实验操作及制备装置中存在的错误共有几处?( )
 溶液,充分反应至无气泡逸出,将混合液倒入分液漏斗中,振荡、静置,收集下层液体即得粗制乙酸乙酯。该实验操作及制备装置中存在的错误共有几处?( )
溶液,充分反应至无气泡逸出,将混合液倒入分液漏斗中,振荡、静置,收集下层液体即得粗制乙酸乙酯。该实验操作及制备装置中存在的错误共有几处?( )
A . 2
B . 3
C . 4
D . 5
最近更新



