实验1-1 蓝瓶子实验 知识点题库
 蒸馏烧瓶
B .
蒸馏烧瓶
B .  B .
B .  C .
C .  D .
D . 
①用10mL量筒准确量取稀硫酸溶液8.0mL;
②用干燥的pH试纸测定氯水的pH;
③能说明亚硝酸是弱电解质的是:用HNO2溶液作导电试验,灯泡很暗;
④使用容量瓶配制溶液时,俯视液面定容后所得溶液的浓度偏大;
⑤将饱和FeCl3溶液滴入蒸馏水中即得Fe(OH)3胶体;
⑥圆底烧瓶、锥形瓶、蒸发皿加热时都应垫在石棉网上;
⑦除去铁粉中混有的少量铝粉.可加入过量的氢氧化钠溶液,完全反应后过滤;
⑧为测定熔融氢氧化钠的导电性,可在瓷坩埚中熔化氢氧化钠固体后进行测量;
⑨用食醋除去水壶中的水垢.
 读数
B .
读数
B .  稀释
C .
稀释
C .  爆炸品
B .
爆炸品
B .  遇湿易燃物品
C .
遇湿易燃物品
C .  氧化剂
D .
氧化剂
D .  腐蚀品
腐蚀品
| 分类组合 | 酸 | 碱 | 盐 | 非金属氧化物 | 金属氧化物 |
| A. | C2H5OH | Ca(OH)2 | K2CO3 | CO2 | CaO |
| B. | HNO3 | NaHCO3 | Na2SO4 | CuO | MgO |
| C. | NH3 | Ba(OH)2 | MgCl2 | P2O5 | CaO |
| D. | CH3COOH | NaOH | CaCO3 | SO2 | Mn2O7 |
-
(1) 按仪器的安装先后顺序排列以上提供的各组仪器(填序号):⑤→→→→①→②。
-
(2) 冷凝管中冷凝水应从下口(填“进”或“出”,下同),上口。
-
(3) 蒸馏时,温度计水银球应位于。
-
(4) 在蒸馏烧瓶中注入液体混合物后,加几片碎瓷片的目的是。
-
(5) 蒸馏后在锥形瓶中收集到的液体是,烧瓶中剩下的液体主要是。
 C .
C .  D .
D . 
-
(1) 下列操作中,容量瓶所不具备的功能有________________(填序号)。A . 配制一定体积准确浓度的标准溶液 B . 贮存溶液 C . 测量容量瓶规格以下的任意体积的溶液 D . 准确稀释某一浓度的溶液 E . 量取一定体积的液体 F . 用来加热溶解固体溶质
-
(2) 如图是某些仪器的刻度部分示意图,图中各仪器虚线为所示读数。其中为量筒的是 (填编号)。

-
(3) 实验室用98%的浓硫酸配制(浓硫酸的密度1.84g/mL)450 mL 0.1 mol/L的硫酸。回答下列问题:
①配制中应选用的玻璃仪器除量筒、烧杯、玻璃棒、还有,应量取mL 98%的浓硫酸。残留在量筒壁上的浓硫酸是否需要洗涤,并转入容量瓶(填是或否)。
②对浓硫酸稀释过程中遇到下列情况,使所配制的硫酸浓度大于0.1mol/L有(填序号)
A.未经冷却趁热将溶液注入容量瓶中
B.摇匀后发现液面低于刻度线,再加水至刻度线
C.容量瓶中原有少量蒸馏水
D.定容时俯视观察液面

 B .
B .  D .
D . 
反应原理:2NH3(g)+CO2(g)  NH2COONH4(s) △H<0。
NH2COONH4(s) △H<0。
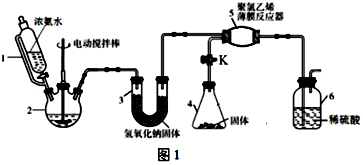
-
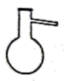
(1) 仪器2的名称是。仪器3中NaOH固体的作用是。
-
(2) ①打开阀门K,仪器4中由固体药品所产生的气体就立即进入仪器5,则该固体药品的名称为。
②仪器6的一个作用是控制原料气按反应计量系数充分反应,若反应初期观察到装置内稀硫酸溶液中产生气泡,应该(填“加快”、“减慢”或“不改变”)产生氨气的流速。
-
(3) 另有一种制备氨基甲酸铵的反应器(CCl4充当惰性介质)如图2:

①图2装置采用冰水浴的原因为。
②当CCl4液体中产生较多晶体悬浮物时,即停止反应, (填操作名称)得到粗产品。
为了将所得粗产品干燥可采取的方法是。
A.蒸馏 B.高压加热烘干 C.真空微热烘干
-
(4) ①已知氨基甲酸铵可完全水解为碳酸氢铵,则该反应的化学方程式为。
②为测定某样品中氨基甲酸铵的质量分数,某研究小组用该样品进行实验。已知杂质不参与反应,请补充完整测定某样品中氨基甲酸铵质量分数的实验方案:用天平称取一定质量的样品,加水溶解,,测量的数据取平均值进行计算(限选试剂:蒸馏水、澄清石灰水、Ba(OH)2溶液)。
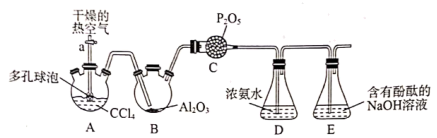
①按如图连接装置,检验装置的气密性,然后加装实验药品;
②打开活塞a.,向A中缓慢通入干燥的热空气;
③一段时间后,装置D中溶液会出现分层现象,且混合液上方有大量白色烟雾;
已知:3CCl4+Al2O3=3COCl2+2AlCl3
回答下列问题:
-
(1) 检验整个装置的气密性的方法:。
-
(2) 步骤②中通入干燥的热空气的作用为。
-
(3) 装置C的作用。
-
(4) 装置D中反应除生成尿素[CO(NH2)2]外,还有NH4Cl生成,该反应的化学方程式为。
-
(5) 分离装置D中混合液的操作名称为。
-
(6) 装置E中足量的NaOH溶液与少量的光气反应的离子方程式为:。
-
(7) 实验后,将D中溶液先蒸发结晶,再用重结晶的方法得到尿素晶体(含有少量的NH4Cl杂质),测定所得晶体中尿素的百分含量的方法:将7.07g晶体中所含氮完全转化为氨气所得氨气用100mL2.00mol•L-1的硫酸溶液完全吸收,取吸收液10mL用0.4000mol•L-1的氢氧化钠标准溶液滴定。
①到达滴定终点时,消耗氢氧化钠45.00mL,则该晶体中尿素的质量分数为(保留3位有效数字)。
②若滴定前未用氢氧化钠标准溶液润洗滴定管,则测得该体晶中尿素的质量分数(选填“偏大”或“偏小”)。

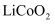 、Al、C等)的处理工艺(已知
、Al、C等)的处理工艺(已知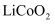 与NaOH不反应):
与NaOH不反应):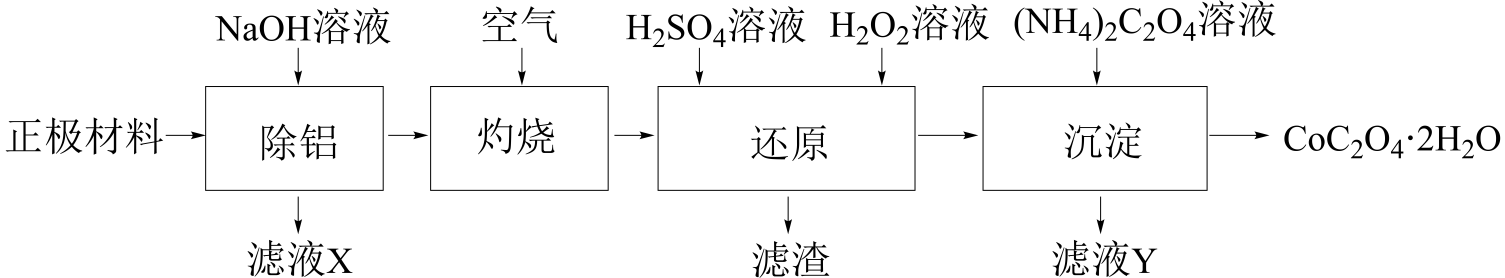
下列说法错误的是( )
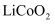 转化为
转化为 和
和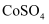 D . “除铝”、“还原”和“沉淀”三步共同的实验操作是过滤
D . “除铝”、“还原”和“沉淀”三步共同的实验操作是过滤



