实验1-2 氯气的生成及其性质的微型实验 知识点题库
要设计一套实验室利用液体和液体加热反应制备气体的装置,现设计了五步操作,正确的程序是( )
①将蒸馏烧瓶固定在铁架台上
②将酒精灯放在铁架台上,根据酒精灯确定铁圈高度,固定铁圈,放好石棉网
③用漏斗向蒸馏烧瓶中加入一种液体反应物,再向分液漏斗中加入另一种液体反应物,并将导气管放入气体收集器中
④检查装置的气密性(利用对固定装置微热的方法检查气密性)
⑤在蒸馏烧瓶上装好分液漏斗,连接好导气管
A . ②①⑤④③
B . ④①②⑤③
C . ①②⑤④③
D . ①⑤④②③
下列方法中,能用于实验室里制取气体的是( )
A . 加热试管中的氯化铵固体制取氨气
B . 用锌与稀硝酸反应制取氢气
C . 用石灰石与稀盐酸反应制取二氧化碳
D . 往过氧化氢中加入少量二氧化锰快速制取少量氧气
下列有关海水综合利用的说法正确的是( )
A . 海水晒盐后的母液中,直接加入CCl4可萃取Br2单质
B . 从海水制海盐主要是通过化学变化完成
C . 电解氯化钠溶液可以制得钠单质和氯气
D . 电解熔融的氯化镁可制备镁单质和氯气
某课外实验小组设计的如图实验合理的是( )
A .  配制一定浓度硫酸溶液
B .
配制一定浓度硫酸溶液
B .  制备少量氨气
C .
制备少量氨气
C .  制备并收集少量NO2气体
D .
制备并收集少量NO2气体
D .  制备少量氧气
制备少量氧气
 配制一定浓度硫酸溶液
B .
配制一定浓度硫酸溶液
B .  制备少量氨气
C .
制备少量氨气
C .  制备并收集少量NO2气体
D .
制备并收集少量NO2气体
D .  制备少量氧气
制备少量氧气
从海带中提取碘单质,成熟的工艺流程如下,下列关于海水制碘的说法,不正确的是( )

A . 实验室在蒸发皿中灼烧干海带,并且用玻璃搅拌
B . 含I﹣的滤液中加入稀硫酸和双氧水后,碘元素发生氧化反应
C . 在碘水中加入几滴淀粉溶液,溶液变蓝色
D . 碘水中加入CCl4得到I2的CCl4的溶液,该操作为“萃取”
空气中含量较多,且性质稳定的是( )
A . 氮气
B . 氧气
C . 二氧化碳
D . 水蒸气
二氧化锰与浓盐酸混合加热得到氯气,如图是制取并探究Cl2化学性质的装置图.

-
(1) 圆底烧瓶中发生反应的化学方程式为.
-
(2) 若要得到干燥纯净的气体,B、C中应分别盛放的试剂为、.
-
(3) E中若装有FeCl2溶液,反应的离子方程式为,E中若装有淀粉碘化钾溶液,能观察到的实验现象是
-
(4) 实验中发现:浓盐酸与MnO2混合加热生成氯气,稀盐酸与MnO2混合加热不生成氯气.针对上述现象某化学兴趣小组对“影响氯气生成的原因”进行了讨论,并设计了以下实验方案:
a.稀盐酸滴入MnO2中,然后通入HCl气体加热
b.稀盐酸滴入MnO2中,然后加入NaCl固体加热
c.稀盐酸滴入MnO2中,然后加入浓硫酸加热
d.MnO2与NaCl的浓溶液混合加热
e.浓硫酸与NaCl固体、MnO2固体共热
①实验b的目的是.实验c的目的是.
②实验现象:a、c、e有黄绿色气体生成,b、d没有黄绿色气体生成.由此得出影响氯气生成的原因是.
化学与人类生产,生活密切相关.下列有关说法不正确的是( )
A . 绚丽缤纷的烟花中添加了含钾,钙,钠,铜等金属元素化合物
B . 碳酸氢钠可用于制备纯碱,治疗胃酸过多的药物,食品发酵剂
C . 医用酒精使用淀粉类植物发酵经蒸馏制成,浓度通常为75%
D . “海水淡化”可以解决“淡水供应危机”,向海水中加入净水机明矾可以使海水淡化
海水是一个巨大的化学资源库,下列有关海水综合利用的说法错误的是( )
A . 海水中含有溴元素,需经过化学变化才可以得到溴单质
B . 无论是海水波浪发电还是潮汐发电,都是将化学能转化为电能
C . 从海水中可以得到NaCl,电解熔融NaCl可制备金属钠
D . 从海水中提取镁可以采用下列方法:海水海水 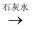 Mg(OH)2
Mg(OH)2  MgCl2溶液→MgCl2→MgCl2(熔解)
MgCl2溶液→MgCl2→MgCl2(熔解)  Mg
Mg
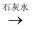 Mg(OH)2
Mg(OH)2  MgCl2溶液→MgCl2→MgCl2(熔解)
MgCl2溶液→MgCl2→MgCl2(熔解)  Mg
Mg
下列有关实验方法正确的是( )
A . 用铜片和浓硝酸反应制NO
B . 加热NH4Cl和Ca(OH)2固体混合物制取NH3
C . 用浓硫酸干燥NH3
D . 用排水法收集NO2
只运用物理方法就能从海水中获得的物质是( )
A . I2
B . Br2
C . Mg
D . NaCl
化学探究学习小组的同学用下图所示装置制取氯气并探究氯气的某些性质。

-
(1) 装置A中制取Cl2的化学方程式为。
-
(2) 装置C中发生反应的离子方程式为,反应后溶液中含Cl元素的分子有。
-
(3) 实验结束后,测得装置D溶液中存在大量SO42-。Cl2通过装置D溶液时发生反应的离子方程式为 。
-
(4) 装置F的作用是,该装置中发生反应的离子方程式。
钌(Ru)是一种硬而脆呈浅灰色的多价稀有金属,性质很稳定,且耐腐蚀性很强。实验室用H2还原RuO2来制备金属钌的装置如图所示。下列说法错误的是( )

A . 加热试管前,应先收集气体并点燃,通过爆鸣声判断气体的纯度
B . 洗气瓶中盛装的可能是NaOH溶液,用于除去HCl
C . 结束反应时,先停止加热,再关闭活塞K
D . 启普发生器也可用于二氧化锰与浓盐酸反应制备氯气
无机化合物可根据其组成和性质进行分类。

-
(1) 上图所示的氧化物指的是含种元素的化合物。
-
(2) 以Na、K、H、O、C、S、N中任两种或三种元素组成合适的物质,分别填在上表中②③⑥后面。
物质类别
酸
碱
盐
氧化物
氢化物
化学式
①HCl
②
③
④Ba(OH)2
⑤Na2CO3
⑥
⑦CO2
⑧Na2O
⑨NH3
⑩H2O2
-
(3) 写出⑦转化为⑤的化学方程式。
-
(4) 实验室制备⑦常用反应,检验该气体的方法是。
某学习小组的同学对氯气与铁的反应及产物进行了如下探究:

-
(1) 装置的连接顺序为a→→→→→b→c→f。
-
(2) 硬质玻璃管与收集器之间没有用导管连接,这样做的优点是。
-
(3) 反应一段时间,熄灭酒精灯,冷却后,将收集器及硬质玻璃管中的物质快速转移至锥形瓶中,加入过量的稀盐酸和少许植物油(反应过程中不振荡),充分反应后,进行如下实验:

试剂X中溶质的化学式为;固体产物的成分可能为(填字母)。
A.Fe和FeCl3
B.FeCl2 和FeCl3
C.Fe、FeCl2和FeCl3
D.Fe和FeCl2
-
(4) 加入少许植物油的作用是,加入新制氯水后溶液红色加深的原因:(用离子方程式表示)。
-
(5) 现有一含FeCl2和FeCl3混合物的样品,用离子交换法测得n(Fe):n(Cl)=1:2.1,则该样品中FeCl3的物质的量分数为。(计算结果保留两位有效数字)
实验室用如下装置制取氯气,并用氯气进行实验。回答下列问题:

-
(1) A中盛有浓盐酸,B中盛有MnO2 , 写出反应的化学方程式。
-
(2) D中放入浓H2SO4 , 其目的是。
-
(3) E中为红色干布条,F中为红色湿布条,可观察到的现象是,对比E和F中现象的差异可得出的结论及解释是。
-
(4) G处的现象是。
-
(5) 画出H处尾气吸收装置图并注明试剂。
-
(6) 家庭中常用消毒液(主要成分NaClO)与洁厕灵(主要成分盐酸)清洁卫生。某品牌消毒液包装上说明如下图。

①“与洁厕灵同时使用”会产生有毒的氯气,写出反应的离子方程式。
②需“密闭保存”的原因。
-
(7) 现在有一种名为“净水丸”的产品也能对饮用水进行快速的杀菌消毒,药丸通常分内外两层。外层的优氯净Cl2Na(NCO)3先与水反应,生成次氯酸起杀菌消毒作用;几分钟后,内层的亚硫酸钠(Na2SO3)溶出,可将水中的余氯(次氯酸等)除去。亚硫酸钠将水中多余次氯酸除去的离子反应方程式为。
用如图所示的实验装置和方法进行下列实验,能达到实验目的的是( )
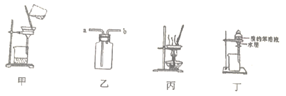
A . 利用装置甲除去NaCl中的氢氧化铁胶体
B . 用装置乙收集CO2时,气体应b管进a管出
C . 利用装置丙将CuSO4溶液蒸发获得CuSO4 · 5H2O
D . 将丁中的液体依次从下口放出水层,从上口放出有机层
如图是产生和收集气体的实验装置示意图,该装置适合于( )

A . 用浓硝酸和Cu制取NO2
B . 用H2O2溶液和MnO2制取O2
C . 用浓盐酸和MnO2制取Cl2
D . 用NH4Cl溶液和Ca(OH)2制取NH3
下列说法错误的是( )
A . 用浓硫酸在纸上书写的字迹变黑表现了浓硫酸的氧化性
B . 浓硫酸在加热条件下与铜反应体现了浓硫酸的强氧化性和酸性
C . 在雷雨天,空气中的氮气和氧气可反应生成NO
D . 氮气既可以作氧化剂又可以作还原剂
化学与科技、社会、生产密切相关,下列有关说法不正确的是( )
A . 从海水中可以提取镁、溴、铀和重水
B . 乙醇汽油的广泛使用不能减少汽车尾气中NOx的排放,目前,全球仍处于化石能源时期
C . 阿司匹林可用于治疗胃酸过多,碘酸钾可用作营养强化剂
D . 高炉炼铁时,增加炉子的高度,使CO和Fe2O3充分接触反应,不能减少尾气中CO的含量
最近更新



