第二单元 钠、镁及其化合物 知识点题库

①外观暗灰色,表皮光滑;
②在酒精灯上灼烧,火焰绿色,合金片熔化,但不滴落;
③取刮去表皮的金属10.0g,放入足量H2SO4 , 收集到标准状况下的H2 8.96L;
④另取刮去表皮的金属10.0g,放入足量NaOH(aq)中,也收集到标准状况下的H2 8.96L.
试据此判断,合金中一定含有的元素是(写元素符号);下列元素可能含有的是(填选项编号).
a.Ag b.Mg c.Na d.Fe
如果该合金中,只含2种元素,它们的质量比是.
-
(1) 取一小块金属钠,放在燃烧匙里加热,下列现象中正确的是
①熔成小球②在空气中燃烧火星四射③燃烧后得白色固体④火焰为黄色⑤燃烧后生成淡黄色固体
A . ①② B . ①②③ C . ①④⑤ D . ④⑤ -
(2) 取少量(1)中生成的固体放入试管中,滴几滴水,有无色无味气体放出.检验该气体的方法是
-
(3) 总结Na2O与H2O、Na2O2与H2O、Na2O与盐酸发生化学反应的规律,写出Na2O2与盐酸反应的化学方程式,并判断Na2O2是否为碱性氧化物(与酸反应生成盐和水的氧化物).
 B .
B .  C .
C .  D .
D . 
| 化合物 | 单质 | 混合物 | 电解质 | 非电解质 | |
| A | 烧碱 | 液态氧 | 冰水混合物 | 盐酸 | 三氧化硫 |
| B | 生石灰 | 白磷 | 胆矾 | 氧化铝 | 蔗糖 |
| C | 干冰 | 铁 | 氢氧化铁胶体 | 纯碱 | 酒精 |
| D | 空气 | 氮气 | 石灰乳 | 氯化铜 | 硫酸钡 |
| A | B | C | D | |
| 强电解质 | NaCl | H2SO4 | CaCO3 | HNO3 |
| 弱电解质 | HF | BaSO4 | HClO | CH3COOH |
| 非电解质 | Cl2 | CO2 | C2H5OH | H2O |
①酸性溶液中:Fe2+、Al3+、  、Cl-、I-
、Cl-、I-
②pH=13的溶液:Na+、  、
、  、
、  、S2-
、S2-
③水电离出来的c(H+)=10-13 mol/L的溶液:  、K+、
、K+、  、
、 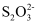
④加入铝片能放出H2的溶液:Na+、  、Cu2+、
、Cu2+、 
⑤滴加石蕊试液显红色的溶液:Fe3+、  、Cl-、
、Cl-、 
①pH试纸变成深蓝色的溶液中:SO  、S2O
、S2O  、Na+
、Na+
②含有大量S2-的溶液中:Na+、ClO-、Cl-、CO 
③AlCl3溶液中:K+、SiO  、NH
、NH  、NO
、NO 
④中性溶液中:Cu2+、Fe3+、SO  、Cl-
、Cl-
⑤加入铝粉放出氢气的溶液:Na+、Cl-、NH  、NO
、NO 
⑥在含有大量HCO  的溶液中:K+、Na+、AlO
的溶液中:K+、Na+、AlO  、Br-
、Br-
 、Cl-、Mg2+、Ba2+、
、Cl-、Mg2+、Ba2+、  、
、  ,现取三份100 mL溶液进行如下实验:
,现取三份100 mL溶液进行如下实验: ⑴第一份加入AgNO3溶液有沉淀产生;
⑵第二份加足量NaOH溶液加热后,收集到气体0.04 mol;
⑶第三份加足量BaCl2溶液后,得干燥沉淀6.63g,经足量盐酸洗涤、干燥,剩余沉淀质量为4.66 g。根据上述实验,以下推测错误的是( )
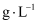 ,溶液E的焰色反应呈黄色。下列有关推断错误的是( )
,溶液E的焰色反应呈黄色。下列有关推断错误的是( ) 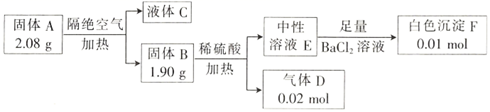
 B . 固体B具有还原性,是常用的抗氧化剂
C . 气体D能使品红溶液﹑酸性高锰酸钾溶液褪色
D . A,B,C,D,E,F均属于电解质
B . 固体B具有还原性,是常用的抗氧化剂
C . 气体D能使品红溶液﹑酸性高锰酸钾溶液褪色
D . A,B,C,D,E,F均属于电解质
 、
、  D . K+、Ba2+、
D . K+、Ba2+、  、Cl-
、Cl-



