金属活动性顺序及其应用 知识点题库
-
(1) 若反应前后溶液质量不变,A中一定含有。
-
(2) 若反应后溶液质量减少,B中一定含有的金属离子是。
【查阅资料】钠常温下就能与水发生剧烈反应,反应方程式为:2Na+2H2O==2NaOH +H2↑。
【提出猜想】猜想一:金属钠和硫酸铜溶液反应会有铜生成。
猜想二:金属钠和硫酸铜溶液反应,生成的沉淀只有氢氧化铜。
【实验及现象】切取不同大小的钠块分别投入到两种不同浓度的硫酸铜溶液中,有关产生沉淀
的现象如下表所示。
实验编号 | 钠块大小 | 硫酸铜溶液 | 实验中产生沉淀的现象 |
① | 绿豆大小 | 稀溶液10ml | 产生蓝绿色沉淀 |
② | 绿豆大小 | 浓溶液10ml | 产生蓝色絮状沉淀 |
③ | 豌豆大小 | 稀溶液10ml | 产生蓝色絮状沉淀 |
④ | 豌豆大小 | 浓溶液10ml | 产生蓝色絮状沉淀,并出现黑色固体 |
小科咨询老师后得知蓝绿色沉淀为碱式铜盐。
-
(1) 【实验结论】a.上述实验中均未观察到色固体生成,由此判断猜想一错误
b.实验①中观察到的沉淀是蓝绿色的,由此判断猜想二也错误。
-
(2) 【实验反思】
实验中生成氢氧化铜沉淀的原理是。 由上述实验可知,导致钠和硫酸铜溶液反应的产物不同的因素有
-
(3) 为了用钠置换硫酸铜中的铜元素,小科设计了如下实验方案:
方案一:把钠块和无水硫酸铜直接混合,在干燥的空气中加热。
方案二:把钠块和无水旒酸铜直接混合,隔绝空气加热。
请从两个方案中选出合理的方案,并说明理由。
① Cl2 + 2NaBr = Br2 + 2NaCl ② Br2 + 2NaI = I2 + 2NaBr
-
(1) Cl2、Br2 和 I2 单质的活动性由强到弱的顺序为。
-
(2) 经查阅资料得知:硫单质的活动性比 Cl2、Br2 和 I2 单质都要弱。结合第(1)小题结论, 你认为只需下列哪一个化学方程式就能证明该结论( )。
A . Cl2 + Na2S = S + 2NaCl2 B . Br2 + Na2S = S + 2NaBr C . I2 + Na2S = S + 2NaI

①Na、Mg、Zn三种金属都能置换出酸中的氢
②生成相同质量的氢气消耗金属的质量为Na>Mg=Zn
③生成相同质量的氢气消耗Na、Mg、Zn三种金属的质量 比为23:24:65
④生成相同质量的氢气消耗Na、Mg、Zn三种金属的原子个数比为2:1:1
查阅资料:欲比较金属的活动性,可采取在相同条件下比较金属与酸反应产生气泡速度的快慢,金属活动性越强产生气泡速度越快。
实验设计:相同温度下,取大小相同的两种金属薄片,用砂纸将表面擦光亮,分别投入等体积、等浓度且足量的稀盐酸中反应,观察现象。
请分析回答下列问题:
-
(1) 两种金属投入盐酸前用砂纸将表面擦光亮,其目的是____________。A . 除去氧化膜,便于直接反应 B . 使表面不平整,易反应 C . 使表面光亮,易观察 D . 提高金属温度,加快反应速度
-
(2) 根据下表中的现象填写结论。
金 属
铁
锰
与盐酸反应现象
放出气泡速度缓慢
放出气泡速度较快
结论
-
(3) 除了比较与酸反应产生气体速度的快慢,你还有其他化学方法可比较金属活动性的强弱吗?请举出一种方法(写出原理即可)。

-
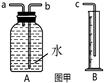
(1) 实验前需用98%的浓硫酸配制10%的硫酸溶液。现有烧杯、玻璃棒、 胶头滴管,还需要的仪器有。
-
(2) 利用图甲中A、B仪器可以组装一套实验室测量取氢气体积的装置,该装置导管的连接顺序是。
-
(3) 图乙中量气管和水准管也可以用来测量氢气体积,为了准确地测量氢气体积,在读取量气管中液面读数的过程中,应注意 (填字母编号)。A . 读数时视线与凹液面最低处相平 B . 读数前应上下移动水准管,待两管液面相平再读数 C . 保持水准管静止,待水准管中液面不再上升时再读数
-
(1) 【实验猜想】对滤液A所含的溶质有以下几种猜想:
①Mg(NO3)2、AgNO3、Cu(NO3)2 ②Mg(NO3)2、Cu(NO3)2
③Mg(NO3)2、AgNO3 ④只有Mg(NO3)2
经过讨论大家一致认为不合理的猜想是(填标号)。理由是.
-
(2) 【实验探究】若猜想④成立,通过以下实验可确定固体B的成分,请将下表填写完整。
实验步骤
现象
固体B的成分
有气泡产生
-
(1) 下列用品中,主要利用金属导电性的是 (填字母);A . 铂金饰品 B . 铁锅 C . 铝导线
-
(2) 为了验证铝、铜、银三种金属的活动性顺序,设计了下列四种方案,其中可行的是(填序号)①将铝、银分别浸入到硫酸铜溶液中;②将银分别浸入到硫酸铝、硫酸铜溶液中;③将铜、银分别浸入到硫酸铝溶液中 ④将铜分别浸入到硫酸铝、硝酸银溶液中。
-
(3) 某钢铁厂每天需消耗4900t含Fe2O376%的赤铁矿石,该厂理论上可日产含Fe98%的生铁的多少?
| 分组 | Ti | Mg | Cu |
| 现象 | 气泡速度缓慢 | 气泡速度快 | 无明显现象 |
则下列说法不正确的是( )
-
(1) 酸菜等酸性的食物不宜用铁质器具长期盛放,因为。
-
(2) 为减缓海水对铁质海轮外壳的腐蚀,制造海轮时,会在海轮船底四周镶嵌比铁更活泼的金属。下列金属适宜船底镶嵌的是 (填字母)。A . Pb(铅) B . Cu C . Pt(铂) D . Zn
-
(3) 对铁“发蓝”处理,其表面将形成致密氧化膜而有效避免腐蚀。
①致密氧化膜能有效阻止铁锈蚀的原因是。
②“发蓝”过程的化学方程式如下,则式中X的化学式为。
36Fe+4NaNO2+9NaNO3+26H2O=12X+13NaOH+13NH3↑
③为检验“发蓝”处理的铁质零件表面是否形成致密氧化膜,将该零件浸泡于硫酸铜溶液中,发现零件表面出现红色物质。由此可知该零件“发蓝”处理效果(选填“好”或“不好”),因为(用化学方程式表示)。

-
(1) 实验I中以“金属表面产生气泡的快慢”为标准来判断锌、铁的活动性强弱,有同学认为不够合理,理由是;
-
(2) 写出实验II中C试管内反应的化学方程式;
-
(3) 实验II中要验证Cu、Fe、Ag的活动性顺序,至少要做的实验是(填字母序号)。
-
(1) 判断C、Fe、Al的活动性顺序由强到弱为.
-
(2) 结合所学知识,下列各组物质能发生置换反应的是 .A . 碳与氧化铜 B . 锌与稀硫酸 C . 碳与氧化钙 D . 银与硫酸铜
-
(1) 湿法炼铜中的一个环节是铁和硫酸铜的反应,产生红色固体物质覆盖在铁表面。写出产生上述现象的化学方程式是:。
-
(2) 实验室可采用氢气和氧化铜反应制取金属铜,是因为氢气具有性。
|
选项 |
“禁忌” |
原理解释 |
|
A |
用锡壶装醋酸 |
活动性顺序:Sn<H |
|
B |
煤气泄漏时,开灯检查 |
电火花会点燃混合气体,发生爆炸 |
|
C |
用稀HCl除铁锈时,浸泡太久 |
6HCl+2Fe = 2FeCl+3H↑ |
|
D |
浓硫酸洒在手上,直接用水冲洗 |
浓硫酸具有吸水性 |



