饱和溶液和不饱和溶液相互转变的方法 知识点题库
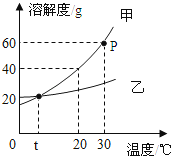
如图是甲、乙两种固体物质的溶解度曲线.据图回答:
(1)P点的含义 .
(2)要使接近饱和的甲溶液变成饱和溶液,可采用的方法有(写出一种),当甲中含有少量乙时,可采用的方法提纯甲.
(3)30℃时,将40g甲物质放入盛有50g水的烧杯中,所得溶液溶质的质量分数为 . 若烧杯内物质升温到50℃(不考虑蒸发),溶液中变化的是 (选填序号).
a.溶质的质量 b.溶液的质量 c.溶质的质量分数
(4)从图中还可获得的信息是 (答出一条).
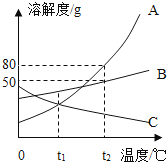
A、B、C三种固体物质的溶解度曲线如图所示,据图回答问题:
(1)温度为 ℃时,A与C物质的溶解度相等;
(2)将t1℃时A、B、C三种物质的饱和溶液升温到t2℃,有晶体析出的是 (填字母代号);
(3)t2℃时,把A、B物质各50g分别加到100g水中,不能形成饱和溶液的是 (填字母代号),若要使之达到饱和状态,还需要向溶液中加入 g该溶质.
①加入氢氧化钙②升高温度 ③降低温度 ④加入水 ⑤蒸发水,其中正确的是
如图是a、b、c三种物质的溶解度曲线,下列分析中不正确的是( )




①P点的意义是;
②t2℃时,将50g a物质放入50g水中充分溶解,得到a的溶液的质量为 g(a物质不含结晶水);
③t2℃时,a、b、c三种物质的溶解度由大到小的顺序为:;将t2℃时a、b、c三种物质的饱和溶液降温至t1℃时,所得溶液的溶质质量分数关系是;
④t2℃时,将c的饱和溶液变为不饱和溶液,可采用的方法.


-
(1) 分析图1,P点处A、B两种物质的溶解度关系是AB(填“>”、“<”或“=”);取一定质量的A的饱和溶液,将溶液温度从t℃降低到10℃,溶液中溶质的质量分数如何变化
-
(2) 分析图2,要使C的饱和溶液变成不饱和溶液,可采用的方法是:
①;②.
-
(3) 10℃时,A、B、C的饱和溶液中溶质的质量分数由大到小的顺序是.


-
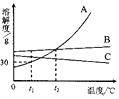
(1) 丙物质的饱和溶液变成不饱和溶液的一种方法是。
-
(2) 若要从乙物质的饱和溶液中得到乙固体, 宜采用的结晶方法。
-
(3) t1℃时,将甲、乙、丙三种物质的饱和溶液分别升 温到t2℃,所得溶液中溶质的质量分数由大到小的顺序是。
-
(4) t3℃时,将100g水加入到盛有30g甲物质的烧杯中,充分溶解后得到不饱和溶液,若想使溶液恰好饱和,可采用具体的方法是(答一种就可以):。
-
(5) t1℃时,将等质量的甲、乙、丙的饱和溶液升温到 t2℃,所得溶液的质量关系是。

A.甲、乙、丙三种物质的溶解度由大到小的顺序是:乙>甲=丙
B.将相同质量的甲、乙、丙三种物质的饱和溶液从t2℃降温到t1℃析出晶体最多的是甲
C.t2℃时,30g甲物质加入50g水中,充分搅拌后,所得溶液的溶质的质量分数为37.5%
D.欲将丙物质的不饱和溶液变为饱和溶液,可以采取(填“升高”或“降低”)温度的方法
-
(1) I水的组成:如图1为电解水的实验装置图,接通电源观察两电极都有气泡产生。
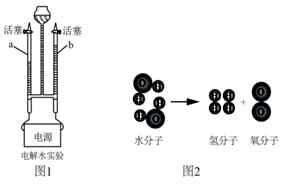
用化学方程式表示出玻璃管a中收集到的气体的一种用途。
-
(2) 图2为水分解的微观过程。
①水的分解过程中,没有发生变化的微粒是。(填具体的微粒名称)
②结合实验现象,写出电解水的化学方程式。
-
(3) II水的用途:水是常用的溶剂。
农业生产中,常需要用质量分数16%的NaCl溶液来选种,现要配制150Kg该溶液,需水Kg;
-
(4) 实验室中常用水作为溶剂配制溶液,王老师在讲授溶液时,用固体M做了如下实验,图一中甲、乙、丙、丁是充分搅拌后静置的现象,请回答相关问题(忽略水的挥发):
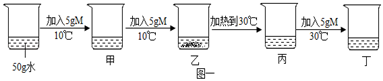
①甲、乙、丙、丁烧杯中的溶液一定呈饱和状态的是(填序号)。
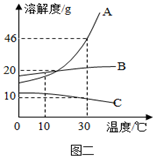
②根据图二,若固体M的图像是A,要使丁烧杯中的溶液恰好达到饱和状态,还需要加入g的M固体。
III水的净化:“硬水”是指含有较多可溶性钙镁化合物的水,硬水会给生产、生活带来许多不便。生活中常用煮沸的方法降低水的硬度,此过程中发生的化学反应之一是:碳酸氢钙[Ca(HCO3)2]受热分解生成碳酸钙、二氧化碳和水,写出该反应的化学方程式,

A.15℃时甲、乙的溶解度相等
B.甲的溶解度受温度影响比乙小
C.升高温度可使接近饱和的甲溶液变为饱和
D.30℃时甲的溶解度为
 向一定量的锌粒中加入足量的稀硫酸,生成氢气和稀硫酸的质量关系
B .
向一定量的锌粒中加入足量的稀硫酸,生成氢气和稀硫酸的质量关系
B .  某温度下向一定量不饱和氯化钠溶液中加入氯化钠晶体,溶质质量分数与加入氯化钠质量的关系
C .
某温度下向一定量不饱和氯化钠溶液中加入氯化钠晶体,溶质质量分数与加入氯化钠质量的关系
C .  向一定量氢氧化钠溶液中滴加稀盐酸
D .
向一定量氢氧化钠溶液中滴加稀盐酸
D .  向含有一定量稀盐酸和氯化钙的混合溶液中逐滴加入碳酸钠溶液,所加碳酸钠溶液质量与生成沉淀质量的关系
向含有一定量稀盐酸和氯化钙的混合溶液中逐滴加入碳酸钠溶液,所加碳酸钠溶液质量与生成沉淀质量的关系
温度/℃ | 10 | 20 | 30 | 40 | 50 |
KCl | 30g | 33g | 35g | 38g | 41g |
KNO3 | 21g | 31g | 45g | 65g | 88g |



