根据浓硫酸或烧碱的性质确定所能干燥的气体 知识点
根据浓硫酸或烧碱的性质确定所能干燥的气体 知识点题库
例如:缓慢氧化 铁钉表面生锈镑
-
(1) 氦气性质稳定且密度比空气小
-
(2) 二氧化碳能溶于水
-
(3) 浓硫酸具有吸水性
-
(4) 中和反应
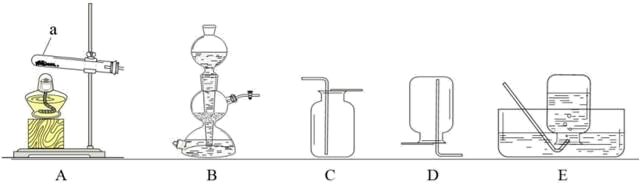
①仪器a的名称:。
②用氯酸钾和二氧化锰制取较干燥的氧气,可选用的装置组合是,反应的化学方程式为。
③实验室制取二氧化碳选用B 装置的优点是,反应的化学方程式为,若要证明该反应后的废液中含有盐酸,不可选用的试剂是。
A.锌粒 B.氧化铜 C.氢氧化铜 D.硝酸银溶液
④用以下仪器组装一套实验室制取CO2的发生装置,可选择B、C和(选填字母)。
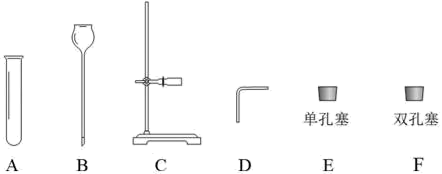
⑤含0.2mol过氧化氢的溶液与二氧化锰混合,充分反应后得到氧气g.(根据化学方程式列式计算)
-
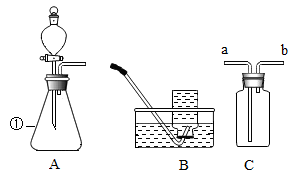
(1) 仅器①的名称是。
-
(2) 实验室制取氧气时,A中发生的化学方程式为。若用B装置收集氧气,则待导管口有时开始收集,否则收集的气体不纯。
-
(3) 若用A、C装置组合制取二氧化碳并验满,可将燃着的木条放在玻璃管(填“a”或“b”)端,如果熄灭则满了。
-
(4) 用C装置除去二氧化碳气体中少量水蒸气,C中放入的试剂是(填名称)。
-
(1) H2SO4溶液的pH7(填“>”、“<”或“=”),请写出用pH试纸测定稀硫酸pH的正确方法。
-
(2) 浓硫酸有吸水性,常用作某些气体的干燥剂,下列气体不能用浓硫酸干燥的是(填写序号)。
①H2
②CO2
③NH3
④HCl
-
(3) 实验室常用亚硫酸钠固体(Na2SO3)和70%左右的硫酸溶液发生复分解反应制取SO2 , 请写出该反应的化学方程式:。
-
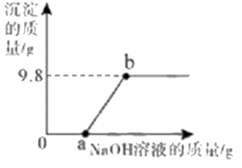
(4) 向160g含有H2SO4和CuSO4的混合溶液中逐滴加入NaOH溶液至过量,产生的沉淀质量与加入NaOH溶液质量的关系如图所示,请写出b点对应溶液的溶质(填写化学式),原混合溶液中CuSO4的质量分数是。
(查阅资料)
-
(1) ①硅胶:无色或白色颗粒,吸水量为 30%~35%,加热到200~350℃可以反复使用。其主要成分可看作是SiO2 , 其中Si元素的化合价为。
②生石灰:白色块状固体,吸水后生成熟石灰。
③浓硫酸:无色粘稠液体,有吸水性,在化学实验中常用它作干燥剂,但日常生活中却很少用它作除湿剂。其原因是(写出一条即可)。
-
(2) (问题一)除湿剂是否真的可以除湿?
(实验一)探究浓硫酸对氧气的干燥情况。用10%的过氧化氢溶液和二氧化锰制取的氧气,通过浓硫酸两次干燥,将湿度传感器放入收集氧气的密封保鲜袋内,连接数据采集器和电脑。实验装置如图1,约采集5 min,得到变化曲线如图2。
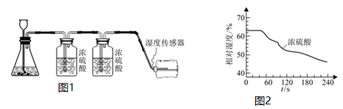
图1中发生的化学方程式为。分析图2曲线,袋内湿度明显降低,说明。随着时间变化,浓硫酸的吸水速率逐渐减小的原因是。
-
(3) (实验二)探究市售硅胶除湿剂是否真的可以除湿。实验如图3,用25 mL烧杯盛放等体积、等温度的两杯水,分别放在生化密闭实验器中,其中一个实验器中加20.0 g 硅胶,连接数据采集器和电脑。约采集 15 min,得到变化曲线如图4。
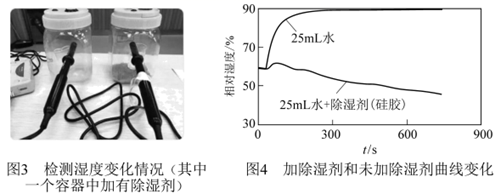
分析图4曲线,未加硅胶的实验器内相对湿度增大的原因是(从微观角度解释)。加硅胶的实验器内,说明硅胶除湿剂的确可以除湿。
-
(4) (问题二)哪种成分的除湿剂除湿效果更好?
(实验三)探究不同成分的除湿剂的除湿效果。实验方法和实验装置与实验二相同,分别称取硅胶、蒙脱石、氯化钙除湿剂各20.0 g,放入3个相同的生化密闭实验器中,连接数据采集器和电脑。约采集 20 min,得到变化曲线如图 5。
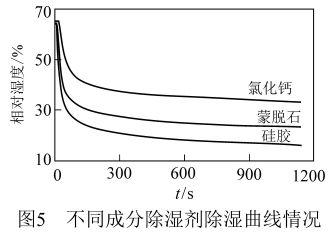
分析图5曲线,这三种除湿剂中单位时间内吸附水速率的快慢和除湿效果的强弱顺序都是。再通过图2、图5的曲线对比,发现的干燥效果都低于其他除湿剂,这是生活中很少用它作除湿剂的另一个原因。
-
(5) (实验结论)市售除湿剂的确可以除湿;对比的几种除湿剂中硅胶的除湿效果最好,速率最快。不同成分的除湿剂除湿效果除了与所含成分不同外,还可能与(写一条即可)等因素有关系。
-
(6) (拓展提升)
同学们查阅资料还发现:还原铁粉(灰色或黑色粉末,又称“双吸剂”),也能够吸收空气中的水分和氧气,常用于食品保鲜。检验使用一段时间后的“双吸剂”是否仍然有效的化学方法及现象是:。已知某袋装食品的脱氧剂由活性炭、铁粉和食盐,按质量比为 2:2:1混合而成。求5.0 g未经使用的该脱氧剂最多能够吸收氧气g (保留两位小数)。
-
(1) 活动一:气体物质的鉴别
【活动目的】鉴别空气与氧气
【操作及结论】
实验操作
实验现象
实验结论
向两种气体中分别伸入带火星的木条
木条
该气体为氧气
木条无明显变化
该气体为空气
-
(2) 活动二:固体物质的鉴别
【活动目的】鉴别氢氧化钠与氯化钠
【操作与结论】分别取少量固体于两个表面皿上,在空气中放置一会儿,观察到其中一种固体表面潮湿并逐渐溶解,该固体为,而表面无明显变化的为另一种固体。
-
(3) 【交流与讨论】经讨论后,小组同学认为只用水也可以鉴别两种物质,依据是:氢氧化钠溶于水,溶液温度(填“升高”或“降低”),氯化钠溶于水,溶液温度无明显变化。
-
(4) 活动三:液体物质的鉴别
【活动目的】鉴别稀硫酸与碳酸钠溶液
【查阅资料】碳酸钠溶液呈碱性
【实验操作】将两种溶液编号为甲溶液、乙溶液,并分别取样于两支试管中,分别滴加稀盐酸。
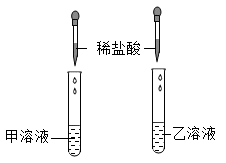
【实验现象】甲溶液中无明显现象,乙溶液中有气泡产生。
【实验结论】甲溶液为,乙溶液为另一种溶液。
乙溶液中产生气泡的化学方程式为。
-
(5) 【拓展延伸】下列物质还可以鉴别稀硫酸与碳酸钠溶液的是(填字母)。
A.酚酞溶液 B.氧化铜 C.铜
活动感悟:在进行物质鉴别时,首先要分析物质的组成、性质等,然后选择合适的方法进行实验,实验过程中必须产生,最后才能达到物质鉴别的目的。



