盐的化学性质 知识点题库
下列各组物质能按照关系图 ![]() (“→”表示反应一步完成)相互转化的是( )
(“→”表示反应一步完成)相互转化的是( )
X | Y | Z | |
A | Cu | CuO | Cu(OH)2 |
B | Ca(OH)2 | Ca(NO3)2 | CaCl2 |
C | Fe2O3 | Fe | FeSO4 |
D | Na2CO3 | NaOH | Na2SO4 |
选项 | 需区分的物质 | 方法一 | 方法二 |
A | 苏打和小苏打 | 分别加入稀盐酸 | 分别加热并将气体通石灰水 |
B | 氧气和二氧化碳 | 分别伸入燃烧的木条 | 分别通过灼热的铜网 |
C | 黄金和黄铜 | 加热后观察颜色 | 加稀盐酸观察现象 |
D | NH4NO3固体和K2SO4固体 | 加水后测溶液温度 | 加氯化钡溶液观察现象 |
-
(1) 上述实验中发生的反应有:①CaO+H2O=Ca(OH)2;②(写化学方程式).
Ⅰ.固体A成分的探究及测定
【猜想】
①固体A中只有CaCO3;
②固体A中含有CaCO3和Ca(OH)2;含有Ca(OH)2的理由是.
【实验】
取少量固体A于试管中加足量水,振荡、静置,向上层清液中滴加硫酸铜溶液,出现,猜想②成立.
-
(2) 【组成测定】
取8.7g固体A于试管中,加足量稀盐酸至固体完全溶解,收集到纯净CO2 2.2g,则固体A中CaCO3和Ca(OH)2的质量比为.
Ⅱ.溶液B的成分探究
【猜想】
①溶液B中的溶质是NaOH;
②溶液B中的溶质是NaOH和Na2CO3;
③溶液B中的溶质是NaOH和Ca(OH)2 .
根据对固体A成分的探究,小组同学认为猜想③正确,其理由是.
【实验】
取少量溶液B于试管中,滴加溶液,产生白色沉淀,证明猜想③正确.
-
(1) 【查阅资料】
①牙膏的成分有活性物质、摩擦剂、保持牙膏湿润的甘油等物质.
②常用的牙膏摩擦剂的主要成分有CaCO3、Al(OH)3、SiO2 .
③牙膏除了碳酸钙以外,其他物质均不与稀盐酸反应产生气体.
④SiO2不溶于水,也不与盐酸反应.Al(OH)3和氢氧化钠溶液反应生成偏铝酸钠(NaAlO2)和水,该反应的化学方程式为.偏铝酸钠和适量稀盐酸反应生成氢氧化铝,氢氧化铝和稀盐酸可以发生中和反应.
-
(2) 相关物质的溶解性表:
物质
Al(OH)3
NaAlO2
AlCl3
溶解性
不溶
溶
溶
该品牌牙膏含有上述摩擦剂中的两种成分,为探究摩擦剂的组成,化学兴趣小组取适量该牙膏加水充分搅拌、静置、过滤、洗涤、干燥,得到该牙膏中的摩擦剂.
【提出猜想】猜想1:摩擦剂的成分为Al(OH)3和CaCO3 .
猜想2:摩擦剂的成分为.
猜想3:摩擦剂的成分为SiO2和Al(OH)3 .
-
(3) 【设计实验】
实验步骤
预期实验现象
预期实验结论
组装如图装置进行实验.取少量摩擦剂于锥形瓶中,加入适量的.

固体全部溶解,有气泡,石灰水变浑浊
则猜想1成立
锥形瓶中发生的化学反应方程式为.
摩擦剂部分溶解
石灰水无明显变化
则猜想3成立
-
(4) 【实验结论】经过实验验证,猜想1成立.
【实验反思】同学们为进一步确认摩擦剂中含有氢氧化铝,先在少量牙膏样品中加入过量的氢氧化钠溶液,静置一段时间,取上层清液,再滴加稀盐酸至过量.整个实验过程中观察到的现象为,依据该现象可以判断摩擦剂中一定含有氢氧化铝.
-
(1) 【提出问题】滤液中溶质的成分是什么?
【作出猜想】猜想Ⅰ:NH4Cl 猜想Ⅱ:NH4Cl和NaHCO3
猜想Ⅲ:NH4Cl和NaCl 猜想Ⅳ:NH4Cl、NaHCO3和NaCl
【实验分析】
实验步骤
实验现象
实验结论
①取少量滤液于试管中,滴加足量的NaOH浓溶液并加热.
产生刺激性气味气体
证明滤液中含有NH4Cl,写出有关化学方程式:
②另取少量滤液于试管中,滴加.
产生无色无味气体
证明滤液中含有
③另取少量滤液于试管中,滴加稀HNO3酸化后,再滴加AgNO3溶液.
产生白色沉淀
(填“能”或“不能”)证明滤液中含有NaCl.
-
(2) 【结论解析】做完步骤③实验后,你得出相关结论的理由是:.
-
(3) 【查阅资料】
2NaHCO3
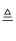 Na2CO3+CO2↑+H2O,
Na2CO3+CO2↑+H2O,NH4Cl
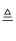 NH3↑+HCl↑
NH3↑+HCl↑【补充实验】另取少量滤液蒸干后充分灼烧,取灼烧后的残余固体溶于水,往其中滴加稀HNO3酸化后,再滴加AgNO3溶液,若观察到,证明猜想成立,化学方程式.
-
(1) [提出问题1] 该氢氧化钠溶液是否变质了呢?
[实验探究1]
实验操作
实验现象
实验结论
取少量该溶液于试管中,向溶液中滴加,并不断振荡。
有气泡产生。
氢氧化钠溶液一定变质了。
-
(2) [提出问题2] 该氢氧化钠溶液是全部变质还是部分变质呢?
[猜想与假设]猜想:1:氢氧化钠溶液部分变质。 猜想2:氢氧化钠溶液全部变质。
[查阅资料] (1) 氯化钙溶液呈中性。(2) 氯化钙溶液能与碳酸钠溶液反应:CaCl2+Na2CO3=CaCO3↓+2NaCl
[实验探究2]
实验步骤
实验现象
实验结论
①取少量该溶液于试管中,向溶液中滴加过量的溶液,并不断振荡。
有生成。
说明原溶液中一定有碳酸钠。
②取步骤①试管中的少量上层清液,滴加酚酞溶液。
溶液变红色。
说明原溶液中一定有。
-
(3) [实验结论] 该氢氧化钠溶液(填“部分”或“全部”)变质。
-
(4) [反思与评价]
①氢氧化钠溶液露置于空气中容易变质,请写出相关反应的化学方程式:
②在上述[实验探究2]中,小明提出可用氢氧化钙溶液代替氯化钙溶液,你认为该方案(填“可行”或“不可行”)。

-
(1) 往溶液A加入过量的氢氧化钙溶液,目的是。
-
(2) 操作1的名称是,沉淀K是(用化学式表示)。
-
(3) 在溶液B中加入盐酸是为了除去未反应的氢氧化钙,反应的化学方程式是。

-
(1) ⑥中溶液变为蓝色,说明;
-
(2) 作为对比实验的试管是(填编号);
-
(3) 再向④中滴加过量稀硫酸,观察到的现象是。

-
(1) 写出下列仪器的名称:a。
-
(2) 组装仪器,检査气密性。关闭K2 , 打开K1 , 开始实验。写出C装置中反应的化学方程式。为收集干燥的氧气,在B装置中加入,A装置验满氧气的方法为。
-
(3) 关闭K1 , 打开K2 , 一段时间后D中的现象为,E中发生反应的化学方程式为。

-
(1) 鸡蛋表面产生大量气泡的主要原因是(用化学方程式表示)。
-
(2) 为进一步确定该气体,小明将一块玻璃片涂上滴有酚酞溶液的澄清石灰水,再将其盖在杯子口(有试剂的一面朝下),一段时间后,观察到。
-
(1) 取少量白色粉末,向其中加入足量的水,充分搅拌后过滤,得到白色沉淀和无色滤液.则原白色粉末中一定不含有.
-
(2) 取实验(1)滤出的白色沉淀,向其中加入足量的盐酸,沉淀全部溶解,并产生无色气体.则原白色粉末中一定含有.
-
(3) 为进一步探究原白色粉末的组成,取实验(1)得到的滤液,向其中通入二氧化碳,产生白色沉淀,则可推断原白色粉末中一定还含有.
 向氢氧化钠溶液中不断加入水
B .
向氢氧化钠溶液中不断加入水
B .  加热一定质量的氯酸钾和二氧化锰的混合物
C .
加热一定质量的氯酸钾和二氧化锰的混合物
C .  向FeCl3和HNO3的混合溶液中加入NaOH溶液
D .
向FeCl3和HNO3的混合溶液中加入NaOH溶液
D .  向硫酸铜溶液中加入铝
向硫酸铜溶液中加入铝
-
(1) 取样后分别滴加酚酞溶液,发现溶液A和B使酚酞变红色,可确定A和B呈性;
-
(2) 取少量A分别与C、D、E的样品混合时,发现C和E中产生气泡、而D中无明显现象,至此,已有3种溶液被鉴别出来。利用已经鉴别出来的溶液,可将剩余的溶液鉴别开;
-
(3) 写出A和B反应的化学方程式。
-
(4) 上述鉴别实验完成后,将所有物质倒入同一个废液缸中,过滤后得到沉淀和无色溶液。取少量滤液,加入氯化钡溶液,没有明显现象。下列关于废液缸的沉淀和滤液的说法,错误的是_____。A . 可以用该沉淀除去氯化钡溶液中混有的盐酸 B . 废液缸中的滤液调至中性后,可排放到下水道中 C . 除指示剂外,滤液的溶质可能只有一种
(资料查阅)
①上述四种物质的相关信息如下:
|
物质 |
NaCl |
NaOH |
Na2CO3 |
NaHCO3 |
|
常温下的溶解度/g |
36 |
109 |
21.5 |
9.6 |
|
常温下稀溶液的pH |
7 |
13 |
11 |
9 |
②NaHCO3也能和盐酸发生复分解反应。
③Na2CO3+CaCl2=CaCO3↓+2NaCl
请回答下列问题:
-
(1) (实验探究1)

如上图乙所示,在操作①后可确定溶质不是NaCl,则实验现象应是;在进行操作②时有无色无味气体产生,由此又可排除的物质是。
-
(2) (探究结论)分析四种物质的相关信息,你认为该溶液中的溶质可能是上述四种物质中的,你的判断依据是。若上述探究结论是正确的,操作②发生反应的化学方程式为。
-
(3) (讨论质疑)有同学认为以上分析不严密,需要进一步实验确定,于是又进行了如下探究。
(实验探究2)向操作①后试管中的溶液中滴加过量CaCl2溶液(中性),充分反应后,试管中溶液颜色不变,但有白色沉淀产生。
(得出结论)通过实验探究2可确定原瓶溶液中的溶质应该是;
-
(4) (反思拓展)造成该溶液出现上述实验现象的原因是(用化学方程式表示)。



