化学科学简介 知识点题库
NA表示阿伏加德罗常数。下列说法错误的是( )
A . 32gO2所含的原子数目为NA
B . 18g水中含有的水分子数为NA
C . 17g氨气所含电子数目为10NA
D . 2.3gNa变成Na+时失电子数为0.1NA
硫酸锰是一.种重要的化工原料,在农业、电化学和建筑等领域均有广泛应用。以含锰废料(含有MnO2 、CuO、Fe和少量CaO)为原料制备MnSO4的一种流程如下:
 已知:
已知:
I .烧渣中含有MnO、CuO、Cu、Fe、CaO。
II.难溶电解质的溶度积常数如下表所示:

回答下列问题:
-
(1) “焙烧”过程加入煤粉的主要作用为。
-
(2) “酸浸”时所加稀H2SO4不宜过量太多的原因为.滤渣1的主要成分为(填化学式)。
-
(3) “氧化”过程中主要反应的离子方程式为。
-
(4) “调pH为4”的目的为;若“溶液”中c(Cu2+ )=0.022 mol/L,“滤液2”的体积是“溶液”体积的2倍,则“调pH为4”时Cu2+是否开始沉淀(通过计算说明)。
-
(5) (NH4)2S的电子式为。
-
(6) 已知:(NH4)2SO4与MnSO4的溶解度曲线如图所示。“操作”主要包括蒸发浓缩、过滤 、洗涤、干燥;其中用乙醇代替水洗涤的原因为,需控制温度为( 填选项字母)得到产品最多。
A.10℃ B.40 ℃ C.60 ℃ D.100℃

二氧化氯(ClO2)是世界卫生组织(WHO)推荐的Al级广谱、安全、高效消毒剂。以下是ClO2的两种制备方法:
方法一:2NaClO3 + 4HCl → 2ClO2↑+ Cl2↑+ 2NaCl + 2H2O
方法二:H2C2O4 + 2NaClO3 + H2SO4 → Na2SO4 + 2CO2↑ + 2ClO2↑ + 2H2O
完成下列填空:
-
(1) 在方法一中,当有0.2 mol电子发生转移时,参与反应的还原剂为 mol。
-
(2) 在方法二中,反应物H2C2O4(填序号)。
a.仅做氧化剂 b.既被氧化又被还原
c.发生氧化反应 d.既未被氧化也未被还原
-
(3) 两种方法相比,(填写“方法一”或“方法二”)制备的ClO2更适合用于饮用水的消毒,其主要原因是。
-
(4) 实验室也可用氯酸钠(NaClO3)和亚硫酸钠(Na2SO3)用硫酸酸化,加热制备二氧化氯,其化学反应方程式为 。
-
(5) 氯原子核外共有种不同运动状态的电子,氯离子的最外层电子排布式是。
-
(6) CCl4分子的空间构型为,CO2的电子式是。
-
(7) 相同压强下,部分元素氯化物的熔点见表:
氯化物
NaCl
KCl
CCl4
熔点/℃
804
773
-22.92
试解释表中氯化物熔点差异的原因:。
下列关于纯净物、混合物、电解质、非电解质的正确组合为( )
| 纯净物 | 混合物 | 电解质 | 非电解质 | |
| A | 纯盐酸 | 水煤气 | 硫酸 | 干冰 |
| B | 蒸馏水 | 蔗糖溶液 | 氧化铝 | 二氧化硫 |
| C | 胆矾 | 氢硫酸 | 铁 | 碳酸钙 |
| D | 过氧化钠 | 氯水 | 氯化铜 | 碳酸钠 |
A . A
B . B
C . C
D . D
2008年5月17日新疆电视台(午间新闻)报道:我国新增阿勒泰大气背景监测点。这标志着气候条件独特、空气质量优良的新疆阿勒泰市已成为我国第8个国家大气背景监测点。监测点安装的监测设备可监测日常二氧化硫、二氧化氮、一氧化氮等污染物。NO分子因污染空气而臭名昭著,近年来,发现少量的NO在生物体内许多组织中存在,它有扩张血管、免疫、增强记忆的功能,而成为当前生命科学的研究热点,NO亦被称为“明星分子”。请回答下列问题:
-
(1) NO对环境的危害在于________(填编号)。A . 破坏臭氧层 B . 高温下能使一些金属氧化 C . 造成酸雨 D . 与人体血红蛋白结合
-
(2) 在含Cu+的酶的活化中心,亚硝酸根离子(NO
 )可转化为NO,写出Cu+和亚硝酸根离子在酸性水溶液中反应的离子方程式:=。
)可转化为NO,写出Cu+和亚硝酸根离子在酸性水溶液中反应的离子方程式:=。
-
(3) “绿色奥运”是2008年北京奥运会的主题之一,为迎接奥运,减少空气污染,北京为汽车加装了“三效催化净化器”,可将尾气中的一氧化碳和一氧化氮转化为参与大气循环的无毒混合气体,该气体是(______)A . 二氧化碳和氮气 B . 二氧化碳和二氧化氮 C . 二氧化碳和氧气 D . 二氧化碳和氢气
-
(4) 氟利昂(如CCl2F2)可在光的作用下分解,产生氯原子,氯原子会对臭氧层产生长久的破坏作用(臭氧的分子式为O3)。有关反应如下:
O3
 O2+O Cl+O3=ClO+O2 ClO+O=Cl+O2 总反应:2O3=3O2
O2+O Cl+O3=ClO+O2 ClO+O=Cl+O2 总反应:2O3=3O2在上述臭氧变成氧气的过程中,Cl是。
下列离子方程式书写正确的是( )
A . 用KIO3氧化酸性溶液中的KI:  B . 草酸溶液使酸性KMnO4溶液褪色:
B . 草酸溶液使酸性KMnO4溶液褪色: 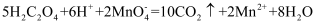 C . 铅蓄电池充电时正极反应:
C . 铅蓄电池充电时正极反应:  D . Na2S2O3溶液中加入稀硫酸:
D . Na2S2O3溶液中加入稀硫酸: 
 B . 草酸溶液使酸性KMnO4溶液褪色:
B . 草酸溶液使酸性KMnO4溶液褪色: 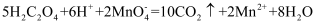 C . 铅蓄电池充电时正极反应:
C . 铅蓄电池充电时正极反应:  D . Na2S2O3溶液中加入稀硫酸:
D . Na2S2O3溶液中加入稀硫酸: 
化学与生活密切相关。下列说法错误的是( )
A . 非处方药的包装上印有“OTC”标示
B . 减少使用氟氯代烷作制冷剂,能保护臭氧层
C . 在酒化酶的作用下葡萄糖水解为乙醇和二氧化碳
D . 维生素 C具有还原性,在人体内起抗氧化作用
下列有关物质应用的说法错误的是( )
A . 氯气用于制备漂白粉
B . 单质硅用于制造光导纤维
C . 用明矾净化水
D . 燃煤时加入石灰石减少SO2排放
下列化学用语对事实的表述错误的是( )
A . 电解精炼铜的阴极反应:  B . 由Na和Cl形成离子键的过程:
B . 由Na和Cl形成离子键的过程: 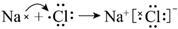 C . 常温时,0.1mol/L氨水的pH=11.1:
C . 常温时,0.1mol/L氨水的pH=11.1: 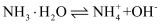 D . 石灰水敞口存放,出现白色固体:
D . 石灰水敞口存放,出现白色固体: 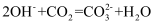
 B . 由Na和Cl形成离子键的过程:
B . 由Na和Cl形成离子键的过程: 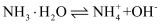 D . 石灰水敞口存放,出现白色固体:
D . 石灰水敞口存放,出现白色固体: 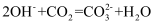
下列说法不正确的是( )
A . 应避免铵态氮肥与草木灰混合施用
B . 工业上可用离子交换法提高海带中碘的提取率
C . 电解饱和食盐水可以得到金属钠和氯气
D . 将生铁进一步炼制减少含碳量,能得到耐腐蚀的钢
离子方程式中,书写错误的是( )
A . 碳酸钠溶液跟稀硫酸混合:  B . 硝酸铜溶液中滴加烧碱溶液:
B . 硝酸铜溶液中滴加烧碱溶液:  C . 将
C . 将  通入足量的氢氧化钙溶液中:
通入足量的氢氧化钙溶液中: 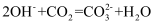 D .
D . 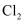 与NaOH溶液反应:
与NaOH溶液反应: 
 B . 硝酸铜溶液中滴加烧碱溶液:
B . 硝酸铜溶液中滴加烧碱溶液:  C . 将
C . 将  通入足量的氢氧化钙溶液中:
通入足量的氢氧化钙溶液中: 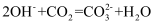 D .
D . 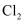 与NaOH溶液反应:
与NaOH溶液反应: 
某无色澄清溶液可能含有CO32-、SO42-、Ba2+、Na+、Ca2+、Cl-、Cu2+、MnO4-中的若干种根据要求回答下列问题。
①取100mL原溶液,加过量的氯化钡溶液,有白色沉淀产生,过滤,洗涤烘干得4.30克沉淀,再向所得沉淀中滴加过量的硝酸,沉淀部分溶解。最后得到2.33克沉淀。
-
(1) 取①中滤液少许,加过量的AgNO3溶液,有白色沉淀产生。根据题意可知:
①原溶液中一定存在的离子是;
②一定不存在的离子是;
③可能存在的离子是;
④求c(Na+)的取值范围;
-
(2) 已知在酸性条件下MnO4-能把Cl-氧化成氯气,自己变成Mn2+请写出它们之间反应的离子方程式。
已知下列实验事实:
①  固体既能溶于 KOH 溶液得到
固体既能溶于 KOH 溶液得到 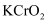 溶液,又能溶于硫酸得到
溶液,又能溶于硫酸得到 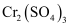
溶液;
②将  溶液滴加到淀粉和 KI 的混合溶液中,溶液变蓝;
溶液滴加到淀粉和 KI 的混合溶液中,溶液变蓝;
③向 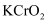 溶液中滴加溶液,再酸化可得
溶液中滴加溶液,再酸化可得  溶液。下列判断不正确的是( )
溶液。下列判断不正确的是( )
A . 化合物 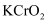 中 Cr 元素为+3 价
B . 实验①证明是两性氧化物
C . 实验②证明氧化性:
中 Cr 元素为+3 价
B . 实验①证明是两性氧化物
C . 实验②证明氧化性:  <
< 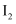 D . 实验②③推断
D . 实验②③推断  可以将
可以将  氧化为
氧化为 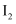
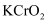 中 Cr 元素为+3 价
B . 实验①证明是两性氧化物
C . 实验②证明氧化性:
中 Cr 元素为+3 价
B . 实验①证明是两性氧化物
C . 实验②证明氧化性:  <
< 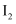 D . 实验②③推断
D . 实验②③推断  可以将
可以将  氧化为
氧化为 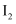
标准状况下,11.2 L由O2和N2组成的混合气体中含有的原子的总物质的量为( )
A . 2 mol
B . 1 mol
C . 0.5 mol
D . 0.25 mol
中华优秀传统文化涉及了很多化学知识。下列有关说法不正确的是( )
A . 《神农本草经》中“石胆……能化铁为铜、成金银”描述的是湿法炼铜
B . 刘长卿诗云“水声冰下咽,砂路雪中平”,固态冰转化为液态水需要吸热
C . “火树银花合,星桥铁锁开”中涉及化学能转化为热能和光能
D . 《本草纲目拾遗》中对强水的记载:“性最猛烈,能蚀五金”强水为强电解质
化学与科技生产、生活环境等密切相关,下列说法不正确的是( )
A . 市售暖贴的发热原理是利用原电池加快氧化还原反应速率
B . 明矾能用于净水是因为铝离子水解生成的氢氧化铝胶体具有吸附性
C . 减少燃煤的使用,改用风能、太阳能等能源,符合“低碳生活”理念
D . 电热水器用镁棒防止内胆腐蚀,利用了外加电源的阴极保护法
2022年2月4日,万众瞩目的第24届冬奥会在北京隆重开幕,本届冬奥会尽显化学高科技。下列有关说法不正确的是( )
A . “飞扬”火炬喷口外壳采用聚硅氮烷树脂,该树脂属于无机聚合物
B . “战袍”利用微信小程序,调控石墨烯片加热保暖,石墨烯和碳纳米管互为同分异构体
C . 国家速滑馆采用的硫化镉发电玻璃,可将太阳能转化为电能
D . 滑雪头盔采用碳纤维、玻璃纤维和弹性体三种成分合成的新材料,其中玻璃纤维和普通玻璃的成分相同
化合物Mg(OH)Cl属于( )
A . 有机化合物
B . 酸
C . 碱
D . 盐
为实现2060年前完成“碳中和”目标,已研究出 转化成有机物的多种反应,其中“原子经济性”最好的反应是原料中的原子全部转变成所需产物。
转化成有机物的多种反应,其中“原子经济性”最好的反应是原料中的原子全部转变成所需产物。
 转化成有机物的多种反应,其中“原子经济性”最好的反应是原料中的原子全部转变成所需产物。
转化成有机物的多种反应,其中“原子经济性”最好的反应是原料中的原子全部转变成所需产物。①
②
③
④
下列说法错误的是( )
A . 通过反应①光能转化为化学能
B . 反应②的“原子经济性”最好
C . 反应③生成的 有毒,该反应无应用价值
D . 反应④是工业生产乙烯的主要方法
有毒,该反应无应用价值
D . 反应④是工业生产乙烯的主要方法
 有毒,该反应无应用价值
D . 反应④是工业生产乙烯的主要方法
有毒,该反应无应用价值
D . 反应④是工业生产乙烯的主要方法
下列离子方程式书写正确的是( )
A . 碳酸钡和稀硫酸反应:BaCO3+2H+=Ba2++CO2↑+H2O
B . CO2通入足量的NaOH溶液:CO2+OH-=HCO3-
C . 向FeCl2溶液中通入Cl2反应生成FeCl3溶液:Fe2++Cl2=Fe3++2Cl-
D . 少量CO2通入澄清石灰水:CO2+Ca2++2OH-=CaCO3↓+H2O
最近更新



