化学科学简介 知识点题库
Ca(ClO)2与浓盐酸反应会生成Cl2 , 该反应的化学方程式:
Ca(ClO)2+4HCl(浓)=CaCl2+2Cl2↑+2H2O
-
(1) 浓盐酸在反应中显示的性质是 (填字母)。A . 只有还原性 B . 还原性和酸性 C . 只有氧化性 D . 氧化性和酸性
-
(2) 产生0.2 mol Cl2时,转移电子的物质的量为mol。
-
(3) 该反应中氧化产物与还原产物的质量比为。
-
(4) Ⅱ.质量相同的O2、NH3、H2、Cl2四种气体中,在相同温度和相同压强条件下,体积最大的是。
-
(5) 下列物质中,既能与盐酸反应,又能与氢氧化钠溶液反应的是(填序号)。
①NaAlO2 ②Ca(OH)2 ③Na2CO3 ④Al(OH)3
-
(6) Ⅲ.奥运金牌“金镶玉”环形碧玉由昆仑玉制成,昆仑玉的成分可简单看成是Ca2Mg5Si8O22(OH)2 , 则其用二氧化硅和金属氧化物的形式可表示为。
下列物质性质与应用对应关系错误的是( )
A . 浓硝酸、浓盐酸均为易挥发的强酸,两者混合配成的“王水”具有强腐蚀性
B . 浓氨水具有挥发性,可用于检验运送氯气的管道是否发生泄露
C . 石墨具有导电性、稳定性,可用作电极材料
D . 氯化铝是电解质,可以用于电解法冶炼金属铝
臭氧层是地球生命的保护神,臭氧比氧气具有更强的氧化性。实验室可将氧气通过高压放电管来制取臭氧:3O2  2O3。
2O3。
 2O3。
2O3。
-
(1) 若在上述反应中有30%的氧气转化为臭氧,所得混合气的平均摩尔质量为 g·mol-1(保留一位小数)。
-
(2) 将8 L氧气通过放电管后,恢复到原状况,得到气体6.5 L,其中臭氧为 L。
-
(3) 在臭氧发生装置中装入氧气100 mL,经反应最后气体体积变为95 mL(体积均在标准状况下测定),则混合气体的密度是g·L-1(保留一位小数)
-
(4) 实验室将氧气和臭氧的混合气体0.896 L(标准状况),通入盛有20.0 g铜粉的反应容器中,充分加热后,粉末的质量最终变为21.6 g。则原混合气中臭氧的体积分数
下列表达方式正确的是( )
A . 24 Cr的外围电子排布式:3d44s2
B . CO2的立体结构模型  C . 基态碳原子的价电子排布图为
C . 基态碳原子的价电子排布图为  D . S2-的结构示意图:
D . S2-的结构示意图: 
下列解释事实的方程式错误的是( )
A . 用K3[Fe(CN)6]检验Fe2+的离子反应方程式:2Fe(CN)63- + 3Fe2+= Fe3[Fe(CN)6]2 ↓
B . 含氟牙膏防治龋齿的原理是氟离子会跟羟基磷灰石发生沉淀转化生成氟磷灰石的离子反应方程式:Ca5(PO4)3(OH) +F-  Ca5(PO4)3F +OH -
C . 用TiCl4制备TiO2的化学方程式:TiCl4+(x+2)H2O
Ca5(PO4)3F +OH -
C . 用TiCl4制备TiO2的化学方程式:TiCl4+(x+2)H2O  TiO2·xH2O↓+4HCl
D . 已知在重铬酸钾溶液中存在着如下平衡:Cr2O72-+ H2O
TiO2·xH2O↓+4HCl
D . 已知在重铬酸钾溶液中存在着如下平衡:Cr2O72-+ H2O  H++ 2CrO42-
H++ 2CrO42-
 Ca5(PO4)3F +OH -
C . 用TiCl4制备TiO2的化学方程式:TiCl4+(x+2)H2O
Ca5(PO4)3F +OH -
C . 用TiCl4制备TiO2的化学方程式:TiCl4+(x+2)H2O  TiO2·xH2O↓+4HCl
D . 已知在重铬酸钾溶液中存在着如下平衡:Cr2O72-+ H2O
TiO2·xH2O↓+4HCl
D . 已知在重铬酸钾溶液中存在着如下平衡:Cr2O72-+ H2O  H++ 2CrO42-
H++ 2CrO42-
下列化学用语正确的是( )
A . CO2分子的电子式为  B . 基态Cu原子核外电子排布式为1s22s22p63s23p63d94s2
C . Cl-的结构示意图为
B . 基态Cu原子核外电子排布式为1s22s22p63s23p63d94s2
C . Cl-的结构示意图为  D . HClO的结构式为H—Cl—O
D . HClO的结构式为H—Cl—O
下列离子方程式正确的是( )
A . 铁粉溶于过量稀硝酸:  B .
B .  溶液中通入过量的
溶液中通入过量的  C . 向
C . 向 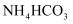 溶液中加入过量
溶液中加入过量  溶液:
溶液:  D .
D .  溶液中滴入少量
溶液中滴入少量 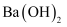 溶液:
溶液: 
 B .
B .  溶液中通入过量的
溶液中通入过量的  C . 向
C . 向 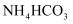 溶液中加入过量
溶液中加入过量  溶液:
溶液:  D .
D .  溶液中滴入少量
溶液中滴入少量 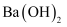 溶液:
溶液: 
下图是一个形象有趣的有机合成反应:

下列说法中正确的是( )
A . 该反应符合绿色化学的理念,原子利用率为100%
B . 化合物X的一氯代物有3种
C . 化合物Y中有5个碳原子共一条直线
D . 化合物Z能使酸性KMnO4溶液褪色,但不能与HCN反应
下列表示错误的是( )
A . 硅原子的结构示意图  B . 丙烷的比例模型
B . 丙烷的比例模型 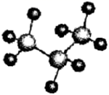 C . 乙烯的最简式
C . 乙烯的最简式  D . 氯化钙的电子式
D . 氯化钙的电子式 
 B . 丙烷的比例模型
B . 丙烷的比例模型  C . 乙烯的最简式
C . 乙烯的最简式  D . 氯化钙的电子式
D . 氯化钙的电子式 
类推是化学学习和研究中常用的思维方法,下列类推正确的是( )
A . 晶体中有阴离子,必有阳离子,则晶体中有阳离子,也必有阴离子
B . CuSO4溶液在空气中蒸干得到CuSO4固体,故Fe2(SO4)3溶液在空气中蒸干得到Fe2(SO4)3固体
C . 适量CO2通入Ca(ClO)2溶液中可生成CaCO3和HClO,故适量SO2通入Ca(ClO)2溶液中可生成CaSO3和HClO
D . Fe和S反应生成FeS,则Cu和S反应生成CuS
下列指定反应的离子方程式正确的是( )
A . 用  溶液腐蚀铜板:
溶液腐蚀铜板:  B . 向碳酸钙粉末中加入醋酸:
B . 向碳酸钙粉末中加入醋酸:  C . 用硫化亚铁处理含
C . 用硫化亚铁处理含  的废水:
的废水:  D . 向
D . 向 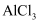 溶液中加入过量氨水:
溶液中加入过量氨水: 
 溶液腐蚀铜板:
溶液腐蚀铜板:  B . 向碳酸钙粉末中加入醋酸:
B . 向碳酸钙粉末中加入醋酸:  C . 用硫化亚铁处理含
C . 用硫化亚铁处理含  的废水:
的废水:  D . 向
D . 向 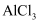 溶液中加入过量氨水:
溶液中加入过量氨水: 
下列物质属于纯净物的是( )
A . 汽油
B . 食醋
C . 漂白粉
D . 小苏打
NA为阿伏加德罗常数的值。下列说法错误的是( )
A . 常温常压下,3.2g N2H4所含共价键的数目为 0.5NA
B . 7g乙烯与7g环丙烷组成的混合物中所含氢原子数为2 NA
C . 0.5mol SO2与足量O2在适宜条件下充分反应转移电子数小于NA
D . 1L0.1mol/L的NaHSO3溶液中HSO  和SO
和SO  的粒子数之和为0.1NA
的粒子数之和为0.1NA
 和SO
和SO  的粒子数之和为0.1NA
的粒子数之和为0.1NA
高锰酸钾是锰的重要化合物和常用的氧化剂。以下是工业上用软锰矿制备高锰酸钾的一种工艺流程。
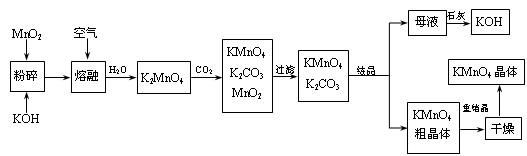
-
(1) KMnO4稀溶液是一种常用的消毒剂。其消毒机理与下列___(填序号)物质相似。A . 75%酒精 B . 双氧水 C . 苯酚 D . 84消毒液(NaClO溶液)
-
(2) 写出MnO2、KOH的熔融混合物中通入空气时发生的主要反应的化学方程式:
。
-
(3) 向K2MnO4溶液中通入CO2以制备KMnO4 , 该反应中的还原剂是:。
-
(4) 上述流程中可以循环使用的物质有石灰、二氧化碳、和(写化学式)。
-
(5) 若不考虑物质循环与制备过程中的损失,则1 mol MnO2可制得mol KMnO4。
下列反应对应的离子方程式正确的是( )
A . 将铁粉加入盐酸中:2Fe+6H+=2Fe3++3H2↑
B . NaOH溶液中加入Al粉:2Al+4OH-=2  +2H2O
C . NaOH溶液通入过量CO2:OH-+CO2=
+2H2O
C . NaOH溶液通入过量CO2:OH-+CO2=  D . Ba(OH)2溶液与稀硫酸:Ba2++
D . Ba(OH)2溶液与稀硫酸:Ba2++  ═BaSO4↓
═BaSO4↓
 +2H2O
C . NaOH溶液通入过量CO2:OH-+CO2=
+2H2O
C . NaOH溶液通入过量CO2:OH-+CO2=  D . Ba(OH)2溶液与稀硫酸:Ba2++
D . Ba(OH)2溶液与稀硫酸:Ba2++  ═BaSO4↓
═BaSO4↓
下列物质分类正确的是( )
A . 稀豆浆、淀粉溶液均为胶体
B .  、
、 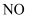 均为酸性氧化物
C . 冰醋酸、干冰均为电解质
D . 玻璃、水晶均为无机硅酸盐材料
均为酸性氧化物
C . 冰醋酸、干冰均为电解质
D . 玻璃、水晶均为无机硅酸盐材料
 、
、 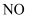 均为酸性氧化物
C . 冰醋酸、干冰均为电解质
D . 玻璃、水晶均为无机硅酸盐材料
均为酸性氧化物
C . 冰醋酸、干冰均为电解质
D . 玻璃、水晶均为无机硅酸盐材料
稀土金属镨 可用于石油催化裂化。下列关于
可用于石油催化裂化。下列关于 和
和 的说法错误的是( )
的说法错误的是( )
 可用于石油催化裂化。下列关于
可用于石油催化裂化。下列关于 和
和 的说法错误的是( )
的说法错误的是( )
A .  和
和 互为同位素
B .
互为同位素
B .  的核外电子数为59
C .
的核外电子数为59
C .  的中子数与核外电子数之差为84
D .
的中子数与核外电子数之差为84
D .  和
和 的质子数、原子序数、核外电子数均相等
的质子数、原子序数、核外电子数均相等
 和
和 互为同位素
B .
互为同位素
B .  的核外电子数为59
C .
的核外电子数为59
C .  的中子数与核外电子数之差为84
D .
的中子数与核外电子数之差为84
D .  和
和 的质子数、原子序数、核外电子数均相等
的质子数、原子序数、核外电子数均相等
 C、
C、 N、
N、 Na、
Na、 H、
H、 U、
U、 K、
K、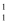 H、
H、 U中共有种元素, 种核素,和互为同位素。
U中共有种元素, 种核素,和互为同位素。
下列离子能大量共存,且加入相应试剂后发生反应的离子方程式书写正确的是( )
选项 | 离子 | 加入试剂 | 加入试剂后发生反应的离子方程式 |
A |
| 少量盐酸 |
|
B |
| 足量铜粉 |
|
C |
| 少量氯气 |
|
D |
| 足量NaOH |
|
A . A
B . B
C . C
D . D
根据下列事实所得结论正确的是( )
事实 | 结论 | |
A | SO2的水溶液能导电 | SO2属于电解质 |
B | 纯碱溶液显碱性 | 纯碱属于碱 |
C | Na2O2能与H2O反应生成NaOH和O2 | Na2O2属于碱性氧化物 |
D | CO2能与NaOH反应生成Na2CO3和H2O | CO2属于酸性氧化物 |
A . A
B . B
C . C
D . D
最近更新
 、
、 、
、 、
、

 、
、 、
、
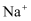 、
、 、
、 、
、

 、
、 、
、




