铜的电解精炼 知识点题库
关于电解法精炼铜的下列说法正确的是( )
A . 电解结束后,在阳极底部会有阳极泥产生,主要成分是铁、金和银
B . 电解结束后,溶液中Cu2+浓度变大
C . 纯铜作阳极,粗铜作阴极,硫酸铜为电解质溶液
D . 粗铜作阳极,纯铜作阴极,硫酸铜为电解质溶液
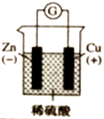
关于如图所示各装置图的叙述不正确的是( ) 

A . 用装置①精炼铜,a极为粗铜,电解质溶液为硫酸铜溶液
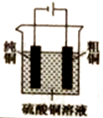
B . 装置②盐桥中KCl的Cl﹣ 移向乙烧杯
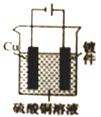
C . 装置③中钢闸门应与外接电源的负极相连
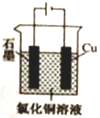
D . 装置④可以验证温度对化学平衡的影响
根据如图回答,下列说法不正确的是( )

A . 此装置用于铁表面镀铜时,a为铁
B . 此装置用于电镀铜时,硫酸铜溶液的浓度不变
C . 燃料电池中正极反应为  O2+2e﹣+2H+═H2O
D . 若用该装置进行粗铜的精炼,当有1 mol水生成时,可得到64 g精铜
O2+2e﹣+2H+═H2O
D . 若用该装置进行粗铜的精炼,当有1 mol水生成时,可得到64 g精铜
 O2+2e﹣+2H+═H2O
D . 若用该装置进行粗铜的精炼,当有1 mol水生成时,可得到64 g精铜
O2+2e﹣+2H+═H2O
D . 若用该装置进行粗铜的精炼,当有1 mol水生成时,可得到64 g精铜
下列四个装置图均与电化学有关,请根据图示回答相关问题:

-
(1) 这四个装置中,利用电解原理的是(填装置序号);
-
(2) 装置①若用来精炼铜,则a极的电极材料是(填“粗铜”或“精铜”),电解质溶液为;
-
(3) 装置②的总反应方程式是.
下列有关说法正确的是( )
A . 氮氧化合物、PM 2.5颗粒、CO2都会导致酸雨
B . 氯水和二氧化硫混合使用能增强漂白效果
C . 硫酸铜溶液可用于泳池消毒是利用了Cu2+能使蛋白质盐析
D . 轮船上挂锌锭防止铁腐蚀属于牺牲阳极的阴极保护法
下列装置中铜电极的连接错误的是( )
A:铜锌原电池 | B:电解精炼铜 | C:镀件上镀铜 | D:电解氯化铜溶液 |
|
|
|
|
A . A
B . B
C . C
D . D
某粗铜产品中含有Zn、Ag、Au等杂质,如图所示,用CH3OH-碱性燃料电池电解硫酸铜溶液。闭合电键K进行电解。下列说法中不正确的是( )

A . 左池负极反应式为CH3OH -6e-+8OH-=CO32-+ 6H2O
B . 通电一段时间后,Ag、Au杂质金属沉积在电解槽底部
C . 若粗铜电极质量减少6.4g,则纯铜电极增重大于6.4g
D . 电解过程中右池纯铜和粗铜分别为阴极和阳极
从废旧液晶显示器的主材 ITO(主要成分是含铟、锡的氧化物)回收铟和锡,流程示意图如下。

资料:
物质 | 铟(In) | 锡(Sn) |
周期表位置 | 第五周期、第IIIA族 | 第五周期、第IVA族 |
颜色、状态 | 银白色固体 | 银白色固体 |
与冷酸作用 | 缓慢反应 | 缓慢反应 |
与强碱溶液 | 不反应 | 反应 |
-
(1) 为了加快步骤①的反应速率,可以采取的措施有(至少答两点)。
-
(2) 步骤①中铟的氧化物转化成In3+的离子方程式是。
-
(3) 步骤②中加入过量铟能够除去溶液中的Sn2+ , 根据所给资料分析其原因是。
-
(4) 步骤④和⑤中NaOH溶液的作用是。
-
(5) 下图是模拟精炼铟的装置图,请在方框中填写相应的物质。

如图中,甲是电解饱和食盐水,乙是铜的电解精炼,丙是电镀,回答:

-
(1) b极上的电极反应式为,甲电池的总反应化学方程式是。
-
(2) 在粗铜的电解过程中,图中c电极的材料是(填“粗铜板”或“纯铜板”);在d电极上发生的电极反应为;若粗铜中还含有Au、Ag、Fe等杂质,则沉积在电解槽底部(阳极泥)的杂质是,电解一段时间后,电解液中的金属离子有。
-
(3) 如果要在铁制品上镀镍(二价金属,相对原子质量59),则f电极的材料是(填“铁制品”或“镍块”,下同),e电极的材料是。
-
(4) 若e电极的质量变化118 g,则a电极上产生的气体在标准状况下的体积为。
印刷电路板(PCB)是用腐蚀液将覆铜板上的部分铜腐蚀掉而制得。一种用FeCl3溶液制作PCB并将腐蚀后废液回收再生的流程如图:

下列说法错误的是( )
A . 腐蚀池中发生反应的化学方程式是:Cu+2FeCl3=CuCl2+2FeCl2
B . 腐蚀后的废液中,主要的金属阳离子有Fe3+、Cu2+、Fe2+
C . 置换池中发生的主要反应为:Fe+Cu2+=Cu+Fe2+和Fe+2Fe3+=3Fe2+
D . 再生池中加入酸化的H2O2 , 反应过程中pH降低
NA为阿伏加德罗常数的值。下列说法正确的是( )
A . 0.1mol 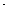 L-1NH4Cl溶液中,Cl-的数量为0.1NA
B . 60g的乙酸和葡萄糖混合物充分燃烧消耗2NA个O2
C . 常温下,1LpH=9的醋酸钠溶液中,水电离出的H+数为10-9NA
D . 用电解粗铜的方法精炼铜,当电路中通过的电子数为2NA时,阳极应有64gCu转化为Cu2+
L-1NH4Cl溶液中,Cl-的数量为0.1NA
B . 60g的乙酸和葡萄糖混合物充分燃烧消耗2NA个O2
C . 常温下,1LpH=9的醋酸钠溶液中,水电离出的H+数为10-9NA
D . 用电解粗铜的方法精炼铜,当电路中通过的电子数为2NA时,阳极应有64gCu转化为Cu2+
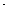 L-1NH4Cl溶液中,Cl-的数量为0.1NA
B . 60g的乙酸和葡萄糖混合物充分燃烧消耗2NA个O2
C . 常温下,1LpH=9的醋酸钠溶液中,水电离出的H+数为10-9NA
D . 用电解粗铜的方法精炼铜,当电路中通过的电子数为2NA时,阳极应有64gCu转化为Cu2+
L-1NH4Cl溶液中,Cl-的数量为0.1NA
B . 60g的乙酸和葡萄糖混合物充分燃烧消耗2NA个O2
C . 常温下,1LpH=9的醋酸钠溶液中,水电离出的H+数为10-9NA
D . 用电解粗铜的方法精炼铜,当电路中通过的电子数为2NA时,阳极应有64gCu转化为Cu2+
下列实验装置符合实验目的是( )
| 目的 | 粗铜的精炼 | 验证NaCl溶液(含酚酞)的产物 | 在铁制品上镀铜 | 构成原电池 |
| 装置 | | | | |
| 选项 | A | B | C | D |
A . A
B . B
C . C
D . D
下列关于铜电极的叙述错误的是( )
A . 锌铜原电池中铜是正极
B . 在镀件上镀铜时可用金属铜作阳极
C . 用电解法精炼粗铜时粗铜作阳极
D . 将铜板与地下钢管相连,可保护地下钢管不受腐蚀
NA为阿伏加德罗常数的数值,下列说法错误的是( )
A . 电解精炼铜时,若阳极质量减少64 g,则转移到阴极的电子数不一定等于2NA
B . 18 g氨基(-ND2)中含有的电子数为10NA
C . 用惰性电极电解100 mL 0.1 mol·L-1的CuSO4溶液,当阴、阳两极产生相同条件下等体积的气体时,电路中转移电子数为0. 04NA
D . 工业合成氨每断裂NA个N≡N键,同时断裂6NA个N-H键,则反应达到平衡
电解原理在化学工业中有广泛的应用。如图表示一个电解池,装有电解液a;X、Y是两块电极板,通过导线与直流电源相连。请回答以下问题:

-
(1) 若X、Y都是惰性电极,a是饱和NaCl溶液,实验开始时,同时在两边各滴入几滴酚酞试液,则:
①电解池中X电极上的电极反应式为,在X极附近观察到的现象是。
②Y电极上的电极反应式为,检验该电极反应产物的方法是。
-
(2) 如要用电解方法精炼粗铜,电解液a选用CuSO4溶液,则:
①X电极的材料是,电极反应式为。
②Y电极的材料是,电极反应式为。
③溶液中的c(Cu2+)与电解前相比(填“变大”、“变小”或“不变”)。
下列有关电解的叙述正确的是( )
A . 工业上用电解熔融  的方法制取
的方法制取 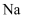 时,阳极材料可以是石墨或铁
B . 可以用电解熔融的
时,阳极材料可以是石墨或铁
B . 可以用电解熔融的 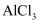 来制取
来制取 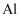 C . 工业上电解饱和食盐水制备烧碱,采用阳离子交换膜
D . 电解精炼铜时,溶液中铜离子的浓度不变
C . 工业上电解饱和食盐水制备烧碱,采用阳离子交换膜
D . 电解精炼铜时,溶液中铜离子的浓度不变
 的方法制取
的方法制取 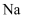 时,阳极材料可以是石墨或铁
B . 可以用电解熔融的
时,阳极材料可以是石墨或铁
B . 可以用电解熔融的 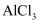 来制取
来制取 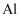 C . 工业上电解饱和食盐水制备烧碱,采用阳离子交换膜
D . 电解精炼铜时,溶液中铜离子的浓度不变
C . 工业上电解饱和食盐水制备烧碱,采用阳离子交换膜
D . 电解精炼铜时,溶液中铜离子的浓度不变
下列对应的电极反应式中,正确的是( )
A . 用惰性电极电解饱和食盐水时,阳极的电极反应式:  B . 酸性氢氧燃料电池正极的电极反应式:
B . 酸性氢氧燃料电池正极的电极反应式:  C . 粗铜精炼时,与电源正极相连的电极上的电极反应式:
C . 粗铜精炼时,与电源正极相连的电极上的电极反应式:  D . 钢铁发生吸氧腐蚀时,铁电极的电极反应式:
D . 钢铁发生吸氧腐蚀时,铁电极的电极反应式: 
 B . 酸性氢氧燃料电池正极的电极反应式:
B . 酸性氢氧燃料电池正极的电极反应式:  C . 粗铜精炼时,与电源正极相连的电极上的电极反应式:
C . 粗铜精炼时,与电源正极相连的电极上的电极反应式:  D . 钢铁发生吸氧腐蚀时,铁电极的电极反应式:
D . 钢铁发生吸氧腐蚀时,铁电极的电极反应式: 
关于下列各装置图的叙述正确的是( )

A . 用图①装置实现租铜精炼,a极为精铜
B . 图②装置盐桥中  的
的  移向右烧杯
C . 图③装置运用的是牺牲阳极的阴极保护法
D . 图④两个装置中通过导线的电子数相同时,两池负极质量消耗不等
移向右烧杯
C . 图③装置运用的是牺牲阳极的阴极保护法
D . 图④两个装置中通过导线的电子数相同时,两池负极质量消耗不等
 的
的  移向右烧杯
C . 图③装置运用的是牺牲阳极的阴极保护法
D . 图④两个装置中通过导线的电子数相同时,两池负极质量消耗不等
移向右烧杯
C . 图③装置运用的是牺牲阳极的阴极保护法
D . 图④两个装置中通过导线的电子数相同时,两池负极质量消耗不等
一种甲烷燃料电池的工作原理如图所示。

-
(1) X电极为(填“正极”或“负极”),该电极的电极反应式为。
-
(2) 放电过程中,
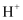 向(填“X极”或“Y极”)移动。
向(填“X极”或“Y极”)移动。
-
(3) 若用该燃料电池进行粗铜精炼,则M极连接的是(填“粗铜”或“精铜”),N极的电极反应式为。
-
(4) 若用该燃料电池进行电镀铜,则N极连接的是(填“镀件”或“精铜”),理论上每消耗
 甲烷时,M极变化(增加或减少)的质量为g。
甲烷时,M极变化(增加或减少)的质量为g。
设NA为阿伏加德罗常数的值,下列叙述正确的是( )
A . 6.8g液态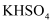 中含有0.05NA个阳离子
B .
中含有0.05NA个阳离子
B .  溶液中含有
溶液中含有 微粒数小于0.1NA
C . 电解精炼铜时,电路中通过NA个电子,阳极消耗32g铜
D . 标况下,2.24L氯气溶于水中,所得溶液中
微粒数小于0.1NA
C . 电解精炼铜时,电路中通过NA个电子,阳极消耗32g铜
D . 标况下,2.24L氯气溶于水中,所得溶液中
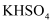 中含有0.05NA个阳离子
B .
中含有0.05NA个阳离子
B .  溶液中含有
溶液中含有 微粒数小于0.1NA
C . 电解精炼铜时,电路中通过NA个电子,阳极消耗32g铜
D . 标况下,2.24L氯气溶于水中,所得溶液中
微粒数小于0.1NA
C . 电解精炼铜时,电路中通过NA个电子,阳极消耗32g铜
D . 标况下,2.24L氯气溶于水中,所得溶液中
最近更新