相似相溶原理及其应用 知识点
相似相溶原理及其应用 :从广义上讲,相似相溶原理的意思是“结构相似者易互溶,结构越相似溶解得越好;结构不相似者不易互溶”.从狭义上讲,相似相溶原理的意思是“极性分子组成的溶质易溶于极性分子组成的溶剂;非极性分子组成的溶质易溶于非极性分子组成的溶剂”.相似相溶原理在化工、科研以及人们的日常生活中有着广泛的应用,推断物质的溶解性大小已知某些物质的极性大小,根据相似相溶原理可推断它们在某些溶剂中的溶解性大小。
相似相溶原理及其应用 知识点题库
下列对分子性质的解释中,不正确的是( )
A . 碘易溶于四氯化碳,甲烷难溶于水都可用相似相溶原理解释
B . 乳酸(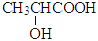 )存在对映异构体,因为其分子中含有一个手性碳原子
C . 在NH3分子中存在极性共价键和配位键
)存在对映异构体,因为其分子中含有一个手性碳原子
C . 在NH3分子中存在极性共价键和配位键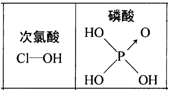 D . 由上图知酸性:H3PO4>HClO,因为H3PO4分子中有非羟基氧原子
D . 由上图知酸性:H3PO4>HClO,因为H3PO4分子中有非羟基氧原子
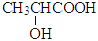 )存在对映异构体,因为其分子中含有一个手性碳原子
C . 在NH3分子中存在极性共价键和配位键
)存在对映异构体,因为其分子中含有一个手性碳原子
C . 在NH3分子中存在极性共价键和配位键 D . 由上图知酸性:H3PO4>HClO,因为H3PO4分子中有非羟基氧原子
D . 由上图知酸性:H3PO4>HClO,因为H3PO4分子中有非羟基氧原子
下列叙述中,正确的是( )
A . C60溶于CS2可用相似相溶原理解释
B . 两种元素组成的分子中一定只有极性键
C . 分子中原子的组成和排列相同则一定是同一种分子
D . 冰结构中(如图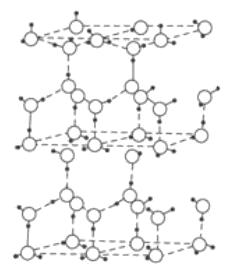 )每个水分子可以和二个水分子形成氢键
)每个水分子可以和二个水分子形成氢键
 )每个水分子可以和二个水分子形成氢键
)每个水分子可以和二个水分子形成氢键
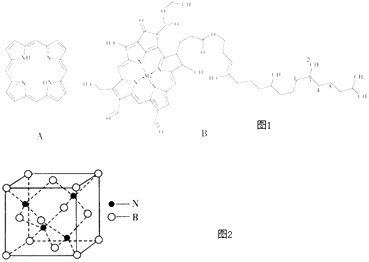
含氮化合物种类繁多,卟吩(图A)连有取代基时即称为卟啉,卟啉的四个氮原子易与金属离子结合生成叶绿素(图B)等多种物质.请回答:
-
(1) 卟吩中N原子采用的轨道杂化方式是
-
(2) 下列有关叶绿素分子的说法正确的是 (填选项序号).A . 图1中1﹣5号C中有三个具有手性 B . 分子中存在配位键 C . 图1中1、2、3、4号C共面 D . N的第一电离能大于O
-
(3) 卟啉与Fe2+合即可形成血红素,Fe2+的电子排布式为
-
(4) 氰化氢(HCN)是一种含氮剧毒化合物,其分子中σ键与π键的个数比为.由分子结构推测,氰化氢(填“易”或“不易”)溶于水,原因是.氰化氢进人人体后产生的CN﹣能使人迅速中毒,请举出两种CN﹣的等电子体.
-
(5) N与B能够形成一种硬度接近金刚石的物质,其晶体结构如图2,若其晶胞边长为apm,则其密度为g.cm﹣3(只列算式).
下列最适合溶解硫粉(S6)的溶剂是( )
A . H2O
B . CH3OH
C . CS2
D . CH3COOH
苯、四氯化碳、乙醇、汽油是常见的有机溶剂,能与水互溶的是,不溶于水,且密度比水小的是.
下列三种有机物:①苯酚,②花生油,③木糖醇[CH2OH(CHOH)3CH2OH],它们在常温下的水溶性大小顺序正确的是( )
A . ①>②>③
B . ③>①>②
C . ③>②>①
D . ②>①>③
推测下列最适合溶解白磷(P4)的溶剂是( )
A . 水
B . CH3OH(甲醇)
C . CS2 (二硫化碳)
D . CH3COOH (乙酸)
下列说法不正确的是( )
A . CF4、CCl4、CBr4、CI4的熔点沸点升高与范德华力有关
B . H2O的熔、沸点大于H2S的是由于H2O之间存在氢键
C . 乙醇与水互溶可以用相似相溶原理解释
D . 分子晶体中分子一定紧密堆积
下列物质易溶于水的是,易溶于CCl4的是 (均填序号).
①NH3②CH4③ 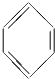 ④HCl ⑤C2H4⑥Br2⑦HNO3⑧SO2 .
④HCl ⑤C2H4⑥Br2⑦HNO3⑧SO2 .
根据“相似相溶”原理,你认为下列物质在水中溶解度较大的是( )
A . 乙烯
B . 二氧化碳
C . 二氧化硫
D . 氢气
下列说法正确的是( )
A . 物质的溶解性为难溶,则该物质不溶于水
B . 不溶于水的物质溶解度为0
C . 绝对不溶解的物质是不存在的
D . 某离子被沉淀完全是指该离子在溶液中的浓度为0
邮票背面的粘合剂可用水浸除去,根据“相似相溶”原理,该粘合剂的成分可能是( )
A . 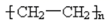 B .
B . 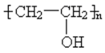 C .
C . 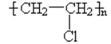 D .
D . 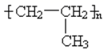
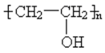 C .
C . 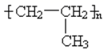
下列物质与水混合后静置,不会出现分层现象的是( )
A . 汽油
B . 苯
C . 四氯化碳
D . 乙醇
现有七种元素A、B、C、D、E、F、G,其中A、B、C为三个不同周期的短周期元素,E、F、G为第四周期元素。请根据下列相关信息,回答问题。
|
A元素的核外电子数和电子层数相等,也是宇宙中最丰富的元素 |
|
B元素原子的核外p电子数与s电子数相等 |
|
C基态原子的价电子排布为nsn-1npn+1 |
|
D的能层数与C相同,且电负性比C大 |
|
E元素的主族序数与周期数的差为1,且第一电离能比同周期相邻两种元素都大 |
|
F是前四周期中电负性最小的元素 |
|
G在周期表的第五列 |
-
(1) C基态原子中能量最高的电子,其电子云在空间有个方向,原子轨道呈形,C简单离子核外有种运动状态不同的电子。
-
(2) A2B2难溶于CS2 , 简要说明理由:。
-
(3) G位于族区,它的一种氧化物常用于工业生产硫酸的催化剂,已知G在该氧化物中的化合价等于其价电子数,则该氧化物的化学式为;F晶体的空间堆积方式为。
-
(4) ED3分子的VSEPR模型名称为,其中E原子的杂化轨道类型为。
过氧乙酸是一种绿色生态杀菌剂,结构简式为 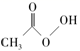 下列说法错误的是( )
下列说法错误的是( )
 下列说法错误的是( )
下列说法错误的是( )
A . 分子中2个碳原子的杂化方式不相同
B . 其熔点主要取决于所含化学键的键能
C . 过氧乙酸中含有极性共价键和非极性共价键
D . 过氧乙酸易溶于水
下列叙述正确的是( )
A . 氯仿、四氯甲烷和苯是工业上重要的有机溶剂
B .  、
、 、
、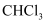 、
、 是同系物
C . 烷烃分子中的碳原子与其它原子的结合方式是通过两个共价键
D . 在一定条件下,
是同系物
C . 烷烃分子中的碳原子与其它原子的结合方式是通过两个共价键
D . 在一定条件下, 可与
可与 、
、 浓硫酸发生化学反应
浓硫酸发生化学反应
 、
、 、
、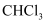 、
、 是同系物
C . 烷烃分子中的碳原子与其它原子的结合方式是通过两个共价键
D . 在一定条件下,
是同系物
C . 烷烃分子中的碳原子与其它原子的结合方式是通过两个共价键
D . 在一定条件下, 可与
可与 、
、 浓硫酸发生化学反应
浓硫酸发生化学反应
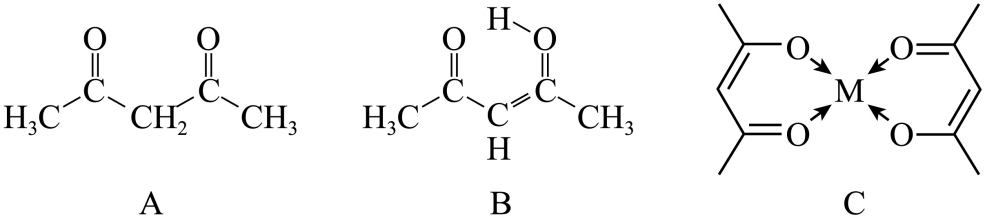
乙酰丙酮是“种有酯气味的无色透明液体,常用作溶剂、有机合成中间体、金属络合剂等。它有两种主要互变异构体A、B,与Be2+、Mg2+、Cu2+、Zn2+等形成配合物C。回答下列有关问题:
-
(1) 基态Cu2+离子的价电子排布式为,Be和Mg第一电离能较大的是原子。
-
(2) A中C原子杂化轨道类型有 ;按VSEPR预测B中∠HCC约为、(填角度)。B在碱性条件下断裂极性最大的键,是 键。 具有分子内氢键的是(填“A”或“B”)。
-
(3) C中σ键与π键数目之比为。
-
(4) 乙酰丙酮易溶于醇、氯仿、丙酮等多数有机溶剂,理由是。
-
(5) 金属铜的某些参数如下:
金属
堆积类型
密度/g·cm-3
相对原子质量
Cu
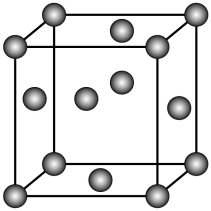
ρ
64
根据上述数据,计算Cu的原子半径为pm (列出计算表达式,设NA是阿伏加德罗常数的值)。
利巴韦林为广谱抗病毒药,其结构如图所示。下列说法错误的是( )
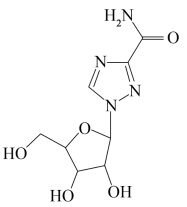
A . 分子中有5个手性碳原子
B . 利巴韦林水溶性较好,可以与盐酸反应
C . 利巴韦林能够发生氧化、取代反应和消去反应
D . 羟基中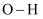 的极性强于亚甲基(-CH2-)中
的极性强于亚甲基(-CH2-)中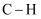 的极性
的极性
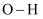 的极性强于亚甲基(-CH2-)中
的极性强于亚甲基(-CH2-)中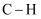 的极性
的极性
交警用三氧化铬( )硅胶可以查酒驾。元素
)硅胶可以查酒驾。元素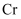 的几种化合物转化关系如图所示。下列判断错误的是( )
的几种化合物转化关系如图所示。下列判断错误的是( )
 )硅胶可以查酒驾。元素
)硅胶可以查酒驾。元素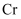 的几种化合物转化关系如图所示。下列判断错误的是( )
的几种化合物转化关系如图所示。下列判断错误的是( ) A.根据相似相溶原理,乙醇易溶于水
A.根据相似相溶原理,乙醇易溶于水
A .  中各原子均满足8电子稳定结构
B .
中各原子均满足8电子稳定结构
B .  、
、 都只有极性键但分子极性不同
C . 基态铬原子的价电子排布式为
都只有极性键但分子极性不同
C . 基态铬原子的价电子排布式为
 中各原子均满足8电子稳定结构
B .
中各原子均满足8电子稳定结构
B .  、
、 都只有极性键但分子极性不同
C . 基态铬原子的价电子排布式为
都只有极性键但分子极性不同
C . 基态铬原子的价电子排布式为
下列现象不能用“相似相溶”规律解释的是( )
A . 甲烷不溶于水
B . 氯化氢易溶于水
C . 单质碘易溶于苯
D . 氯气易溶于NaOH溶液
最近更新



