相似相溶原理及其应用 知识点题库
下列解释中,不正确的是( )
A . 水很稳定(1000℃以上才会部分分解)是因为水中含有大量的氢键所致
B . 由于NaCl晶体和CsCl晶体中正负离子半径比不相等,所以两晶体中离子的配位数不相等
C . 碘易溶于四氯化碳,甲烷难溶于水都可用相似相溶原理解释
D . MgO的熔点比MgCl2高主要是因为MgO的晶格能比MgCl2大
现有下列物质,请按要求回答问题:
①NaOH ②H2O ③NaCl ④CCl4⑤ ⑥
⑥ ⑦I2 ⑧H2O2 ⑨SiO2 ⑩NH4Cl
⑦I2 ⑧H2O2 ⑨SiO2 ⑩NH4Cl
-
(1) 在上述物质中溶于水只断离子键的有: ;(用序号作答,下同),气化时不止克服范德华力且其晶体类型是分子晶体的是:
-
(2) 在上述物质中含有极性键的非极性分子有:
-
(3) 在上述物质中为什么⑦在②中的溶解度小于在④的溶解度:
-
(4) 在上述物质中在上述物质中②⑤⑥熔沸点由小到大的顺序为 ,其原因是
下列现象不能用“相似相溶规则”原理解释的是( )
A . 氯化氢易溶于水
B . 氯气易溶于氢氧化钠溶液
C . 碘易溶于四氯化碳
D . 碘难溶于水
根据相似相溶规则和实际经验,下列叙述不正确的是( )
A . 白磷(P4)易溶于CS2 , 但难溶于水
B . NaCl易溶于水,也易溶于CCl4
C . 碘易溶于苯,微溶于水
D . 卤化氢易溶于水,难溶于CCl4
下列有关有机化合物的叙述正确的是( )
A . 分子式为C2H6O的有机物具有相同的化学性质
B . 分子式为C8H10的芳香烃共有3种
C . 在水中的溶解度:甲酸甲酯<乙酸
D . 可以用酸性高锰酸钾溶液除去甲烷中的乙烯
下列对分子的性质的解释中,错误的是( )
A . 水很稳定(1000℃以上才会部分分解)是因为水中含有大量的氢键所致
B . 乳酸(  )有一对手性异构体,因为其分子中含有一个手性碳原子
C . 碘易溶于四氯化碳,甲烷难溶于水都可用相似相溶原理解释
D . 酸性:H3PO4>HClO,因为H3PO4的非羟基氧原子数比HClO的多
)有一对手性异构体,因为其分子中含有一个手性碳原子
C . 碘易溶于四氯化碳,甲烷难溶于水都可用相似相溶原理解释
D . 酸性:H3PO4>HClO,因为H3PO4的非羟基氧原子数比HClO的多
下表是元素周期表的一部分,表中所列的字母分别代表一种化学元素。

试回答下列问题:
-
(1) M的元素符号为,P的元素名称为
-
(2) D元素原子的价电子排布图为,该元素形成的单质中σ键和π键个数比为;与该单质分子互为等电子体的常见分子的分子式为
-
(3) NE2I2常温下为深红色液体,能与CCl4、CS2等互溶,据此可判断NE2I2是(填“极性”或“非极性”)分子。
-
(4) 在① 苯、②CH3OH、③ HCHO、④CS2、⑤CCl4五种有机溶剂中,碳原子采取sp2杂化的分子有(填序号)。
-
(5) 元素O可以形成分子式为Co(NH3)5BrSO4 , 配位数均为6 的两种配合物,若往其中一种配合物的溶液中加入BaCl2溶液时,无明显现象,若加入AgNO3溶液时,产生淡黄色沉淀,则该配合物的化学式为
下列现象不能用“相似相溶”原理解释的是( )
A . 氯化氢易溶于水
B . 氯气易溶于  溶液
C . 用
溶液
C . 用  萃取碘水中的碘
D . 苯与水混合静置后分层
萃取碘水中的碘
D . 苯与水混合静置后分层
 溶液
C . 用
溶液
C . 用  萃取碘水中的碘
D . 苯与水混合静置后分层
萃取碘水中的碘
D . 苯与水混合静置后分层
下列对分子结构及其性质的解释中,错误的是( )
A . 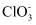 与
与  中心原子的价层电子对数相同
B . 液态氟化氢的化学式有时写成(HF)n的形式与氢键有关
C . 碘易溶于四氯化碳、甲烷难溶于水都可用相似相溶原理解释
D . 酸性:H3PO4>HClO,是因为H3PO4分子中氢原子数比HClO的多
中心原子的价层电子对数相同
B . 液态氟化氢的化学式有时写成(HF)n的形式与氢键有关
C . 碘易溶于四氯化碳、甲烷难溶于水都可用相似相溶原理解释
D . 酸性:H3PO4>HClO,是因为H3PO4分子中氢原子数比HClO的多
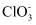 与
与  中心原子的价层电子对数相同
B . 液态氟化氢的化学式有时写成(HF)n的形式与氢键有关
C . 碘易溶于四氯化碳、甲烷难溶于水都可用相似相溶原理解释
D . 酸性:H3PO4>HClO,是因为H3PO4分子中氢原子数比HClO的多
中心原子的价层电子对数相同
B . 液态氟化氢的化学式有时写成(HF)n的形式与氢键有关
C . 碘易溶于四氯化碳、甲烷难溶于水都可用相似相溶原理解释
D . 酸性:H3PO4>HClO,是因为H3PO4分子中氢原子数比HClO的多
d区金属元素钛有“太空金属”“未来金属”等美誉,在航空航天、海洋产业等行业有重要作用。回答下列问题:
-
(1) 我国科学家用
 和
和 , 制备超导材料TiN,反应原理为
, 制备超导材料TiN,反应原理为 。
。①基态钛原子的核外电子排布式为。原子中运动电子有两种相反的自旋状态,若一种自旋状态用
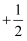 表示,与之相反的则用
表示,与之相反的则用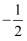 表示,称为电子的自旋磁量子数。对于基态钛原子,其价电子自旋磁量子数的代数和为。
表示,称为电子的自旋磁量子数。对于基态钛原子,其价电子自旋磁量子数的代数和为。②已知部分物质的熔沸点如下表。


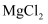
TiN
熔点/℃
800(分解)
-25
714
2950
沸点/℃
700(升华)
136.4
1412
(略)
 属于晶体,中心Ti原子的杂化方式为。
属于晶体,中心Ti原子的杂化方式为。 -
(2)
 是铂的重要配位化合物。它有甲、乙两种同分异构体,其中甲为极性分子,乙为非极性分子。甲、乙的水解产物化学式均为
是铂的重要配位化合物。它有甲、乙两种同分异构体,其中甲为极性分子,乙为非极性分子。甲、乙的水解产物化学式均为 , 但只有甲的水解产物能与草酸(HOOC-COOH)反应生成
, 但只有甲的水解产物能与草酸(HOOC-COOH)反应生成 。
。①根据相似相溶的规律,可推断(填“甲”或“乙”)在水中的溶解度较大。
②
 发生水解反应的化学方程式是。
发生水解反应的化学方程式是。③
 和
和 中铂的配体数分别为和。
中铂的配体数分别为和。④查阅资料可知,甲、乙均为平面结构。画出乙的水解产物的空间结构并推测其不能与草酸反应生成
 的原因:。
的原因:。 -
(3)
 晶体中,
晶体中, 的重复排列方式如图1所示,该晶体中存在着由
的重复排列方式如图1所示,该晶体中存在着由 围成的正四面体空隙(如1、3、6、7号
围成的正四面体空隙(如1、3、6、7号 围成)和正八面体空隙(如3、6、7、8、9、12号
围成)和正八面体空隙(如3、6、7、8、9、12号 围成)。
围成)。 中有一半的
中有一半的 填充在正四面体空隙中,另一半
填充在正四面体空隙中,另一半 和
和 分别填充在不同的正八面体空隙中,则
分别填充在不同的正八面体空隙中,则 晶体中,正四面体空隙和正八面体空隙阳离子的填充率之比为。
晶体中,正四面体空隙和正八面体空隙阳离子的填充率之比为。
-
(4) 铜的晶胞如图2所示,则晶胞中原子的空间利用率为(用含π的最简式表示)。
石墨烯具有优异的光学、电学、力学特性,在材料学、微纳加工、能源和生物医学等方面具有广阔的应用前景,石墨烯可采用化学方法制备,如以六氯苯、六溴苯为原料可制备石墨烯。下表是六氯苯、六溴苯、苯六酸的熔点和水溶性:
物质 | 六氯苯
| 六溴苯
| 苯六酸
|
熔点/℃ | 231 | 325 | 287 |
水溶性 | 不溶 | 不溶 | 易溶 |
下列说法正确的是( )
A . 苯六酸所含元素的电负性:C>O>H
B . 从结构上看,六氯苯、六溴苯和苯六酸均为极性分子
C . 六氯苯、六溴苯和苯六酸分子中C的杂化方式均为sp2杂化
D . 苯六酸与六氯苯、六溴苯的水溶性存在明显的差异是因为其分子结构庞大
阿司匹林是一种合成药物,化学名称为乙酰水杨酸,具有解热镇痛作用。人体血液的 范围为7.35~7.45,长期大量服用阿司匹林会引发酸中毒,可静脉滴注
范围为7.35~7.45,长期大量服用阿司匹林会引发酸中毒,可静脉滴注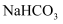 溶液进行缓解。阿司匹林的发现源于柳树皮中含有的一种物质——水杨酸,阿司匹林以水杨酸为原料进行生产,反应如下:
溶液进行缓解。阿司匹林的发现源于柳树皮中含有的一种物质——水杨酸,阿司匹林以水杨酸为原料进行生产,反应如下:
 范围为7.35~7.45,长期大量服用阿司匹林会引发酸中毒,可静脉滴注
范围为7.35~7.45,长期大量服用阿司匹林会引发酸中毒,可静脉滴注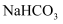 溶液进行缓解。阿司匹林的发现源于柳树皮中含有的一种物质——水杨酸,阿司匹林以水杨酸为原料进行生产,反应如下:
溶液进行缓解。阿司匹林的发现源于柳树皮中含有的一种物质——水杨酸,阿司匹林以水杨酸为原料进行生产,反应如下:
用乙二醇将乙酰水杨酸与聚甲基丙烯酸连接起来,可得到缓释阿司匹林,其结构如下:

下列关于缓释阿司匹林制备及其性质,说法正确的是( )
A . 相同温度下,阿司匹林在水中的溶解度大于缓释阿司匹林
B . 缓释阿司匹林的每个链节中含有4个碳原子
C . 聚甲基丙烯酸能使酸性高锰酸钾溶液褪色
D . 酸性条件下,缓释阿司匹林完全水解可得到三种有机物
最简单的氨基酸是甘氨酸( ),它是人体非必需的一种氨基酸。下列有关说法错误的是( )
),它是人体非必需的一种氨基酸。下列有关说法错误的是( )
 ),它是人体非必需的一种氨基酸。下列有关说法错误的是( )
),它是人体非必需的一种氨基酸。下列有关说法错误的是( )
A . 1个分子中σ键与π键数目比为8∶1
B . 碳原子的杂化轨道类型是sp3和sp2
C . 分子间可以形成不止3种类型的氢键
D . 易溶于极性溶剂,难溶于非极性溶剂
最近更新






