化学式及其计算 知识点题库
某混合物含有氯化钠、碳酸钠和氯化钾。经分析知其中氯的质量分数为35.5%,则该混合物中碳酸钠的质量分数可能为( )
A . 20%
B . 30%
C . 45%
D . 55%。
K35ClO3与K37Cl在酸性溶液中反应生成氯气,则该氯气的相对分子质量为( )
A . 70.7
B . 70.2
C . 72
D . 73.3
已知98克A的物质的量为1mol,则A的摩尔质量为 ,相对分子质量为
由环己烷、乙醇、乙醚(C4H10O)组成的混和物,经测定其中碳的质量分数为72%,则氧的质量分数为( )
A . 14.2%
B . 16%
C . 17.8%
D . 19.4%
甲苯和甘油组成的混合物中,若碳元素的质量分数为60%,那么可推断氢元素的质量分数是( )
A . 0.05
B . 0.087
C . 0.174
D . 无法计算
甲醛、乙酸和丙醛(C3H6O)组成的混合物中,氧元素的质量分数37%,则碳元素的质量分数为( )
A . 27%
B . 28%
C . 54%
D . 无法计算
常温下,A、B组成的混合气体(MA>MB)经分析发现无论怎样混合,气体中仅含的C、O两种元素的质量比总小于3:8,若混合气体中C、O质量比为1:8,则A、B两气体的体积比可能为( )
①3:4 ②2:1 ③4:1 ④4:3 ⑤1:2.
A . 只有⑤
B . ①②
C . ④⑤
D . ②④
一个12C原子的质量为a kg,一个12C16O2分子的质量为b kg,若以12C16O2中的一个氧原子质量的  作为相对原子质量标准,则12C16O2的相对分子质量为( )
作为相对原子质量标准,则12C16O2的相对分子质量为( )
 作为相对原子质量标准,则12C16O2的相对分子质量为( )
作为相对原子质量标准,则12C16O2的相对分子质量为( )
A .  B .
B .  C .
C .  D .
D . 
 B .
B .  C .
C .  D .
D . 
目前,一些发达国家已基本采用新一代饮用水消毒剂ClO2 , 有的国家还颁布了强制使用ClO2的法律和法规.请回答下列有关ClO2的问题:
-
(1) ClO2读作,它是由(几种)种元素组成的;
-
(2) ClO2中氯元素的化合价为,氧元素的质量分数为.
取VmL某溶液(其质量分数为A%),加入等体积的水稀释后其质量分数为0.6A%,则原溶液的密度(忽略混合时溶液体积的变化( )
A . 大于1g/cm3
B . 等于1g/cm2
C . 小于1g/cm3
D . 无法确定
在相同条件下,CO和CO2混合气体密度是H2密度的16倍,则CO与CO2的质量之比为( )
A . 11:21
B . 21:11
C . 1:3
D . 3:1
-
(1) 某实验小组尝试用燃烧法确定有机物M的分子式,所用装置如下:
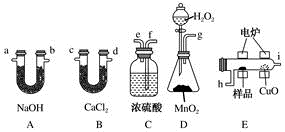
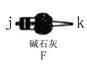
①产生的氧气按从左到右方向流动,所选装置各导管的连接顺序是(以上装置不能重复使用):g→fe→hi→ → →jk。
②F装置作用是。
③若准确称取有机物M(只含C、H、O三种元素中的两种或三种)3.24g,经充分燃烧后,A管质量增加9.24g,B管质量增加2.16 g,则该有机物的实验式为。
④已知在相同条件下该M蒸气相对氢气的密度为54,且能与Na反应但不与NaOH溶液反应,写出该物质在灼热的铜丝条件下与氧气的反应方程式 。
-
(2) 在常温下测得的某烃C8H10(不能与溴水反应)的核磁共振谱上,观察到两种类型的H原子给出的信号,其强度之比为2∶3,试确定该烃的结构简式为;该烃在光照下生成的一氯代物在核磁共振谱中产生的吸收峰强度比为。
绿矾(FeSO4·7H2O)是自然界存在的一种矿石,翠绿如宝石,很早就引起人们的重视。
材料一 《唐本草》和《天工开物》等古籍都记载中国很早就能焙烧绿矾制备铁红(主要成分是Fe2O3)。铁红颜色鲜艳,稳定无毒,是中国传统红色颜料的重要着色剂。
材料二 公元8世纪,阿拉伯炼金家查比尔曾提出,把绿矾焙烧可以蒸馏出“矾精”,它具有比较大的溶解力。绿矾焙烧是一种生产硫酸的古老方法。
-
(1) 某研究性学习小组用下图所示试验装置对绿矾的焙烧反应进行探究。

①实验过程中,装置A玻管中可观察到的实验现象是。
②装置C的作用是。
③该小组学生设计如下实验方案验证“矾精”是硫酸溶液:取U形管中的溶液少许于试管中,滴入(填试剂名称),溶液呈红色,说明“矾精”中含有H+;检验“矾精”中含有SO42-的方法是。
-
(2) 某工厂计划用绿矾焙烧工艺生产高纯度铁红(Fe2O3)160 kg,计算理论上所需绿矾的质量,写出计算过程。
称取有机物A 6.0 g,在足量氧气中充分燃烧,并使产物依次缓慢通过浓硫酸、碱石灰,两者分别增重7.2 g和13.2
g。已知有机物A气态时的密度是相同条件下氢气密度的30倍。
请计算:
-
(1) 有机物A的分子式。
-
(2) 另取A 6.0 g,跟足量的金属钠反应生成1.12 L氢气(标准状况),A可能的结构简式为 。
下列各组中的两种有机物,无论以何种比例混合,只要混合物总质量不变,完全燃烧时生成水的质量就不变,符合这一条件的组合是( )
A . CH3OH和C2H4O2
B . C8H10和C4H10
C . C2H4和C2H4O
D . C8H8和C6H6
下面有机物的同系物中,完全燃烧产生的水和二氧化碳的物质的量之比恒定的是①饱和一元醇②饱和一元醛③饱和一元羧酸④饱和一元醇和饱和一元羧酸生成的酯⑤乙炔的同系物⑥苯的同系物( )
A . ①④
B . ②③④⑤⑥
C . ②③
D . ②③④
将有机物完全燃烧,生成CO2和H2O。将12g该有机物完全燃烧后的产物通过浓H2SO4 , 浓H2SO4增重14.4g,再通过碱石灰,碱石灰增重26.4g。该有机物分子式为( )
A . C3H8O2
B . C2H6O
C . C3H8O
D . С3Н4O2
某兴趣小组为确定Cu(NO3)2·xH2O的结晶水数目,称取样品5.92g,加热使其完全分解,得到1.60g黑色固体产物,同时分解产生的红棕色混合气体经冷凝得到3.2mL无色液体,无气体剩余。请计算:
-
(1) x=。(写出计算过程,下同)
-
(2) 无色液体的浓度为 mol·L-1。
某烷烃在氧气中完全燃烧,生成物先通过浓硫酸,再通过碱石灰,如果生成物完全全被二者吸收,浓硫酸增重27g,碱石灰增重44g。该有机物的化学式为( )
A . CH4
B . C2H6
C . C3H8
D . C4H10
一种以硼镁石[主要含 , 还含有少量
, 还含有少量 ]为原料制取
]为原料制取 的工艺流程如下:
的工艺流程如下:
 , 还含有少量
, 还含有少量 ]为原料制取
]为原料制取 的工艺流程如下:
的工艺流程如下:
-
(1)
 与
与 焙烧时生成
焙烧时生成 、
、 、
、 、
、 、
、 和
和 。写出焙烧时
。写出焙烧时 发生反应的化学方程式:。
发生反应的化学方程式:。
-
(2) 由于部分铵盐的分解,焙烧反应所得的气体中除
 和
和 外,还可能含有
外,还可能含有 和
和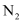 , 其中
, 其中 和
和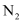 的体积比为。
的体积比为。
-
(3)
 易溶于水,溶于水后生成硼酸
易溶于水,溶于水后生成硼酸 , 硼酸在冷水中溶解度小,溶于水的硼酸可发生电离:
, 硼酸在冷水中溶解度小,溶于水的硼酸可发生电离:


 。硼酸属于元酸。
。硼酸属于元酸。
-
(4) 用氨水调
 的目的是沉淀
的目的是沉淀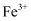 和
和 , 已知实验条件下,部分金属离子开始沉淀的
, 已知实验条件下,部分金属离子开始沉淀的 和对应氢氧化物的
和对应氢氧化物的 如下表所示;溶液中金属离子浓度
如下表所示;溶液中金属离子浓度 , 可以认为沉淀完全。
, 可以认为沉淀完全。

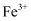
开始沉淀的

8.6
3.7
2.2
氢氧化物的




调
 时需控制的范围是。
时需控制的范围是。 -
(5) 取
 加热分解,所得残留固体的质量与温度的关系如下图所示。
加热分解,所得残留固体的质量与温度的关系如下图所示。 时所得固体的成分为。
时所得固体的成分为。
最近更新



