制备实验方案的设计 知识点题库
CuSO4是一种重要的化工原料,其有关制备途径及性质如图所示.下列说法不正确的是( )

-
(1) Ⅰ、制取氯化锌主要工艺如图:

下表列出了相关金属离子生成氢氧化物沉淀的pH(开始沉淀的pH按金属离子浓度为1.0mol•L﹣1计算).
金属离子
开始沉淀的pH
沉淀完全的pH
Fe3+
1.1
3.2
Zn2+
5.2
6.4
Fe2+
5.8
8.8
①加入H2O2溶液发生反应的离子方程式为.
②流程图中,为了降低溶液的酸度,试剂X不可以是(选填序号);pH应调整到
a.ZnO b.Zn(OH)2 c.Zn2(OH)2CO3 d.ZnSO4
③氯化锌能催化乳酸(2﹣羟基丙酸)生成丙交酯(C6H8O4)和聚乳酸,丙交酯的结构简式为,聚乳酸的结构简式为.
-
(2) Ⅱ、制取金属锌采用碱溶解{ZnO(s)+2NaOH(aq)+H2O(l)═Na2[Zn(OH)4](aq)},然后电解浸取液.
①以石墨作电极电解时,阳极产生的气体为;阴极的电极反应为.
②炼锌烟尘采用碱溶,而不采用酸溶后电解,主要原因是
有关数据列表:
乙醇 | 1,2﹣二溴乙烷 | 乙醚 | |
状态 | 无色液体 | 无色液体 | 无色液体 |
密度/g•cm﹣3 | 0.79 | 2.2 | 0.71 |
沸点/℃ | 78.5 | 132 | 34.6 |
熔点/℃ | ﹣130 | 9 | ﹣116 |
溶解性 | 易溶水 | 难溶水 | 微溶于水 |
请回答下列问题:

-
(1) 在此制备实验中,要尽可能迅速地把反应温度提高到170℃左右,其主要目的是(填正确选项前的字母;
a、引发反应 b、加快反应速度 c、防止乙醇挥发 d、减少副产物乙醚生成
-
(2) 在装置C中应加入,其目的是;(填正确选项前的字母)
a、水 b、浓硫酸 c、氢氧化钠溶液 d、酸性KMnO4溶液
-
(3) 判断该制备反应已经结束的最简单的方法是.
-
(4) 将1,2﹣二溴乙烷粗产品置于分液漏斗中加水,振荡后静置,产物应在层(填“上”或“下”);
-
(5) 在装置B中较长玻璃导管的作用是;
-
(6) 反应过程中应用冷水冷却装置D,其主要目的是,但又不能过度冷却(如用冰水),其原因是;
-
(7) 本实验中,1,2﹣二溴乙烷的产率为.

-
(1) 试管a中需加入浓硫酸、乙酸各2mL,乙醇3mL,应该先加入,再加入,最后加入.
-
(2) 试管a中发生反应的化学方程式是,反应类型是,通常加入几片碎瓷片,其作用是.
-
(3) 试管b中加入饱和Na2CO3溶液,其作用是.
-
(4) 反应结束后,振荡试管b,静置.观察到的现象.

-
(1) 流程中可以循环利用的物质有气体Ⅰ、气体Ⅱ和(填化学式)。
-
(2) “碳化”时发生反应的离子方程式为,该过程中通入气体Ⅰ和气体Ⅱ的顺序是。
-
(3) 工业上常用电解氯化钠和氯化钙熔融物来制备金属钠,原理如下图所示:

①电解过程中,加入氯化钙的目的是。
②石墨电极发生的电极反应方程式为。
③电解得到的Na中约含1%的Ca,除去其中少量Ca的方法为。
已知部分物质的熔沸点如下表:


-
(1) 装置A的作用是:;
-
(2) 为确定反应后装置B硬质玻璃管中固体的成分,小组同学取适量固体于试管中,加入足量的蒸馏水溶解,形成溶液M,无气泡产生,则该固体中不含,该小组同学继续进行探究。
-
(3) 【提出问题】反应后硬质玻璃管中固体的成分是什么?
【做出猜想】猜想一:Na2CO3 猜想二:NaOH 猜想三:Na2CO3和NaOH,经过讨论,大家一致认为猜想二不合理,理由是:(用化学方程式表示)。
-
(4) 【实验验证】小组同学取上述形成的溶液M于试管中,向其中加入过量的溶液,若产生白色沉淀,过滤,向滤液中滴加几滴酚酞试液,溶液变红,则证明猜想三成立。
-
(5) 【交流反思】小组中有同学认为,将上述滤液中滴加的酚酞试液换成硝酸铜溶液,也能得出同样的结论,你认为该同学的观点(填“正确”或“错误”),理由是:(用化学方程式表示)。
-
(6) 【拓展延伸】在盛有氯化铵浓溶液的试管中,加入足量的过氧化钠(Na2O2)固体,有气泡产生, 试管口湿润的红色石蕊试纸变蓝,产生的气体是。

已知:I 在酸性条件下,H2O2能将Cr2O72-还原为Cr3+
II相关金属离子形成氢氧化物沉淀的pH范围如下:

回答下列问题:
-
(1) 滤渣②的主要成分为(填化学式)。
-
(2) 写出“氧化”步骤中反应的化学方程式。
-
(3) “加热”操作的目的是。
-
(4) “酸化”过程中发生反应2CrO42-+2H+
 Cr2O72-+H2O (K=4×1014L3.mol3)已知,“酸化”后溶液中c(Cr2O72-)=1.6×10-3mol/L则溶液中c(CrO42-)=
Cr2O72-+H2O (K=4×1014L3.mol3)已知,“酸化”后溶液中c(Cr2O72-)=1.6×10-3mol/L则溶液中c(CrO42-)=
-
(5) “结晶”后得到K2Cr2O7(M=294g.mol-1)产品0.5000 g,将其溶解后用稀H2SO4酸化,再用浓度为1.0000 mol.L-l (NH4)2Fe(SO4)2 标准溶液滴定,滴定终点消耗标准溶液的体积为9.00 mL,则产品的纯度为。[滴定反应为:K2Cr2O7+6(NH4)2Fe(SO4)2+7H2SO4 =K2SO4 +Cr2(SO4)3 +6(NH4)2SO4+3Fe2(SO4)3+7H2O]
-
(6) 在K2Cr2O7存在下,可利用微生物电化学技术实现含苯酚废水的有效处理,其工作原理如下图所示。

①负极的电极反应式为;
②一段时间后,中间室中NaCl溶液的浓度(填“增大”、“减小”或“不变”)。
-
(1) 甲、乙两位同学设计的过氧化钙实验室制法如下,其中产率较低的是(填A、B)
方法A Ca (OH)2(s) + H2O2⇌CaO2(s) + 2H2O
方法B CaCl2(s) + H2O2⇌CaO2(s) + 2HCl
方法A所得产品中纯度不高,所含杂质主要是(填化学式)
如果不加入稳定剂,则两种方法都需在5℃以下进行实验,原因可能是。
-
(2) 丙同学认为CO2、SO2与过氧化钙的反应原理相同,丁同学认为SO2具有较强的还原性,而CO2没有,故而反应原理不相同。他们设计了如下实验装置,通过测量装置E中所得气体体积判断反应情况:

①试剂B的作用是。
②若实验中SO2足量,且与过氧化钙充分反应,取反应后的固体进行探究,以验证过氧化钙与SO2反应的生成物。若SO2未被氧化,则反应的化学方程式为:。
③装置E中收集到的氧气体积为V L(已换算成标准状况下),若SO2完全被氧化,则V =。
-
(3) 某工厂利用电石渣(主要成分为氢氧化钙)生产过氧化钙的生产流程如下:

用上述方法制备过氧化钙(CaO2·8H2O),搅拌步骤的化学方程式是。
②某小组采用单变量法确定温度、H2O2浓度对产率的影响,结果如下,则实际生产应选择的适宜条件为。
H2O2%
30%
25%
20%
15%
10%
5%
产率
60.40
62.42
64.54
63.20
63.10
62.40
温度(℃)
50
40
30
20
10
0
产率
43.24
52.80
64.54
63.80
60.45
52.40

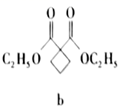
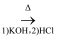

 已知:i.叠氮化钠受热或剧烈撞击易分解,具有较强的还原性。
已知:i.叠氮化钠受热或剧烈撞击易分解,具有较强的还原性。
ii.相关物质的物理性质如下表:
| 相关物质 | 熔点℃ | 沸点℃ | 溶解性 |
| CH3OH | -97 | 67.1 | 与水互溶 |
| 亚硝酸甲酯(CH3ONO) | -17 | -12 | 溶于乙醇、乙醚 |
| 水合肼(N2H4·H2O) | -40 | 118.5 | 与水、醇互溶,不溶于乙醚和氯仿 |
| NaN3 | 275 | 300 | 与水互溶,微溶于乙醇,不溶于乙醚 |
-
(1) 步骤I总反应的化学方程式为。
-
(2) 实验室模拟工艺流程步骤II、III的实验装置如图。

①步骤II三颈烧瓶中发生反应的化学方程式为。该反应放热,但在20℃左右选择性和转化率最高,实验中控制温度除使用冷水浴,还需采取的措施是。
②步骤II开始时的操作为(选填字母编号)。步骤III蒸馏时的操作顺序是(选填字母编号)。
a.打开K1、K2 b.关闭K1、K2 c.打开K3 d.关闭K3 e.水浴加热 f.通冷凝水
-
(3) 步骤IV对B溶液加热蒸发至溶液体积的三分之一,冷却析出NaN3晶体,减压过滤,晶体用乙醇洗涤2~3次后,再干燥。精制NaN3的方法是。
-
(4) 实验室用滴定法测定产品纯度。测定过程涉及的反应为:
2(NH4)2Ce(NO3)6+2NaN3=4NH4NO3+2Ce(NO3)3+2NaNO3+3N2↑
Ce4++Fe2+=Ce3++Fe3+
称取2.50 g产品配成250 mL溶液,取25.00 mL置于锥形瓶中,加入V1 mLc1 mol·L-1(NH4)2Ce(NO3)6溶液,充分反应后稍作稀释,向溶液中加适量硫酸,滴加2滴邻菲哕啉指示剂,用c2 mol·L-1(NH4)2Fe(SO4)2标准溶液滴定过量的Ce4+ , 消耗标准溶液V2 mL。
①产品纯度为。
②为了提高实验的精确度,该实验还需要。
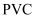 )的合成路线。
)的合成路线。

下列说法错误的是( )
 、
、 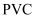 的链节为
的链节为  D . 烃A的结构简式为
D . 烃A的结构简式为 

试剂相关性质如表:
苯甲酸 | 乙醇 | 苯甲酸乙酯 | |
常温性状 | 白色针状晶体 | 无色液体 | 无色透明液体 |
沸点/℃ | 249.0 | 78.0 | 212.6 |
相对分子量 | 122 | 46 | 150 |
溶解性 | 微溶于冷水,溶于热水,易溶于乙醇、乙醚等有机溶剂 | 与水任意比互溶 | 难溶于冷水,微溶于热水,易溶于乙醇和乙醚 |
回答下列问题:
-
(1) 反应前为了提高原料苯甲酸的纯度,可采用的纯化方法为,步骤“酯化”中的反应方程式为。
-
(2) 步骤“酯化”的装置如图所示(加热和夹持装置已略去),将一小团棉花放入仪器
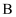 中靠近活塞孔处,将吸水剂放入仪器
中靠近活塞孔处,将吸水剂放入仪器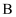 中,在仪器
中,在仪器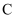 中加入
中加入 纯化后的苯甲酸晶体,
纯化后的苯甲酸晶体, 无水乙醇(约
无水乙醇(约 )和
)和 浓硫酸,加入沸石,加热至微沸,回流反应
浓硫酸,加入沸石,加热至微沸,回流反应 。
。
①仪器
 的名称是,冷凝回流的物质是。
的名称是,冷凝回流的物质是。②仪器
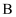 中加入吸水剂的目的是,
中加入吸水剂的目的是,③仪器
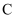 中反应液应采用的加热方式是。
中反应液应采用的加热方式是。 -
(3) 反应结束后,对
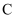 中混合液进行分离提纯。
中混合液进行分离提纯。①操作Ⅰ的名称是。
②试剂
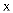 是冷的
是冷的 溶液,其作用是。最终得到产物纯品
溶液,其作用是。最终得到产物纯品 , 实验产率为。
, 实验产率为。
|
|
|
|
|
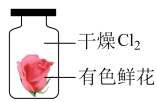
| A.验证干燥的氯气没有漂白性 |
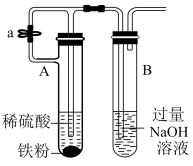
B.不能较长时间观察到Fe(OH)2白色絮状沉淀 |
C.证明氧化性: Cl2>Br2>I2 |
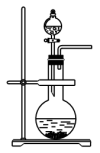
D.选择合适的药品,可用于制备少量的Cl2、O2等气体 |

已知:①MnO2有较强的氧化性,能将金属硫化物中的硫氧化为单质硫;
②该条件下:Ksp[Fe(OH)3]=1.0×10-38 ,Ksp[Cu(OH)2]= 1.0×10-20 ,Ksp[Mn(OH)2]=1.0×10-14。
回答下列问题:
-
(1) 滤渣1的主要成分是(写化学式),酸浸时,Cu2S和MnO2反应的化学方程式为。
-
(2) 检验浸出液中是否含有Fe2+ ,可用K3Fe(CN)6溶液,浸出液中含有Fe2+ 的现象是。
-
(3) 试剂x为某种酸式盐,从产品纯度来看,x最好为(写化学式)。
-
(4) 本工艺中可循环使用的物质是(写化学式)。
-
(5) 若浸出液中c(Mn2+)=c(Cu2+)=1.0 mol·L-1 , 则流程中调节浸出液pH=a,其中a的范围为(当离子浓度≤1.0×10-5 mol·L-1时,沉淀完全)。
-
(6) 除Fe3+也可以用合适的萃取剂,Fe3+的萃取率与pH的关系如图所示,pH>1.7后,随pH增大,Fe3+萃取率下降的原因是。

 (铋酸钠,浅黄色不溶于冷水的固体)是分析化学常用试剂。工业上以辉铋矿粉(主要成分是
(铋酸钠,浅黄色不溶于冷水的固体)是分析化学常用试剂。工业上以辉铋矿粉(主要成分是 , 含少量
, 含少量 、
、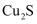 、
、 等杂质)为原料制备铋酸钠的流程如下:
等杂质)为原料制备铋酸钠的流程如下: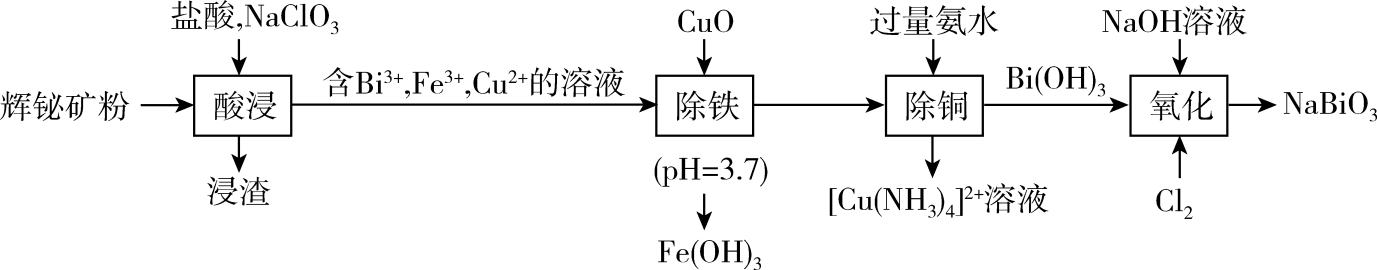
请回答下列问题:
-
(1) “浸渣”的主要成分是(填化学式)。用硝酸替代“盐酸,
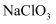 ”也可以实现“酸浸”,从环保角度考虑,存在的缺点是。
”也可以实现“酸浸”,从环保角度考虑,存在的缺点是。
-
(2) 检验“酸浸”液中是否含
 , 可选择的试剂是____(填标号)。
A . KSCN溶液 B .
, 可选择的试剂是____(填标号)。
A . KSCN溶液 B .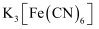 溶液
C . KSCN溶液和双氧水
溶液
C . KSCN溶液和双氧水
-
(3) “除铁”的离子方程式为。
-
(4) 已知
 ,
, 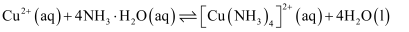 的平衡常数
的平衡常数 。
。 的平衡常数
的平衡常数 。
。
-
(5) 探究
 的性质:
的性质:实验
操作
现象
Ⅰ
取少量
 粉末于试管中,加入浓盐酸,振荡;用镊子夹一块湿润的淀粉KI试纸放置在试管口上方
粉末于试管中,加入浓盐酸,振荡;用镊子夹一块湿润的淀粉KI试纸放置在试管口上方浅黄色固体溶解,产生黄绿色气体,试纸变蓝
Ⅱ
在稀硫酸酸化的
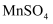 溶液中加入
溶液中加入 粉末,振荡
粉末,振荡无色溶液变紫红色溶液
①实验Ⅱ中发生反应的离子方程式为。
②结合上述实验及所学知识,在酸性条件下,
 、
、 、
、 的氧化性由强到弱的顺序是。(填化学式)。
的氧化性由强到弱的顺序是。(填化学式)。③结合上述流程中“氧化”步骤中发生的反应,说明
 和
和 的氧化性相对强弱不一致的主要原因是。
的氧化性相对强弱不一致的主要原因是。
 、
、  、NiO、
、NiO、 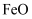 、
、  ]为原料,采用硫酸铵焙烧法选择性提取镍并回收副产物黄铵铁矾[化学式可表示为
]为原料,采用硫酸铵焙烧法选择性提取镍并回收副产物黄铵铁矾[化学式可表示为  ,摩尔质量为
,摩尔质量为  ]的工艺流程如图所示:
]的工艺流程如图所示:

已知:
①  ②
② 
-
(1) 除铁时加入的
 的用量高于理论用量的原因是。(写出2点)
的用量高于理论用量的原因是。(写出2点)
-
(2) 经分析矿样中大部分铁仍以氧化物形式存在于“浸渣”中,只有部分FeO在空气中焙烧时与
 反应生成
反应生成 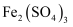 该反应的化学方程式为;“浸渣”的主要成分除含有铁元素的化合物外还有(填化学式)。
该反应的化学方程式为;“浸渣”的主要成分除含有铁元素的化合物外还有(填化学式)。
-
(3) 该工艺条件下,
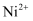 生成
生成  沉淀,
沉淀,  生成
生成 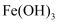 或黄铵铁矾沉淀,开始沉淀和沉淀完全时的pH如下表:
或黄铵铁矾沉淀,开始沉淀和沉淀完全时的pH如下表: 沉淀物

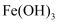
黄铵铁矾
开始沉淀时的pH
7.1
2.7
1.3
沉淀完全
 时的pH
时的pH9.2
3.7
2.3
若残留在浸出液中的铁完全转化为黄铵铁矾除去,“除铁”时通入
 调节溶液pH的范围是。
调节溶液pH的范围是。 -
(4) “沉镍”时pH调为8.0,滤液中
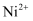 浓度约为mo/L
浓度约为mo/L  。
。
-
(5) 由所得滤液获得
 晶体时,常用无水乙醇代替蒸馏水作洗涤剂,原因是(写出2点)
晶体时,常用无水乙醇代替蒸馏水作洗涤剂,原因是(写出2点)
-
(6) 对黄铵铁巩进行热分解实验,其结果如下图所示,则黄铵铁矾的化学式为。(已知:黄铵铁矾在300℃前分解释放的物质为
 ,300-575℃之间只有
,300-575℃之间只有  和
和  放出,此时残留固体只存在Fe、O、S三种元素,670℃以上得到的是纯净的红棕色粉末)。
放出,此时残留固体只存在Fe、O、S三种元素,670℃以上得到的是纯净的红棕色粉末)。

 是一种金黄色油状液体(沸点138℃),用作除草剂、橡胶硫化剂等。制备装置如图(夹持和加热装置略)。
是一种金黄色油状液体(沸点138℃),用作除草剂、橡胶硫化剂等。制备装置如图(夹持和加热装置略)。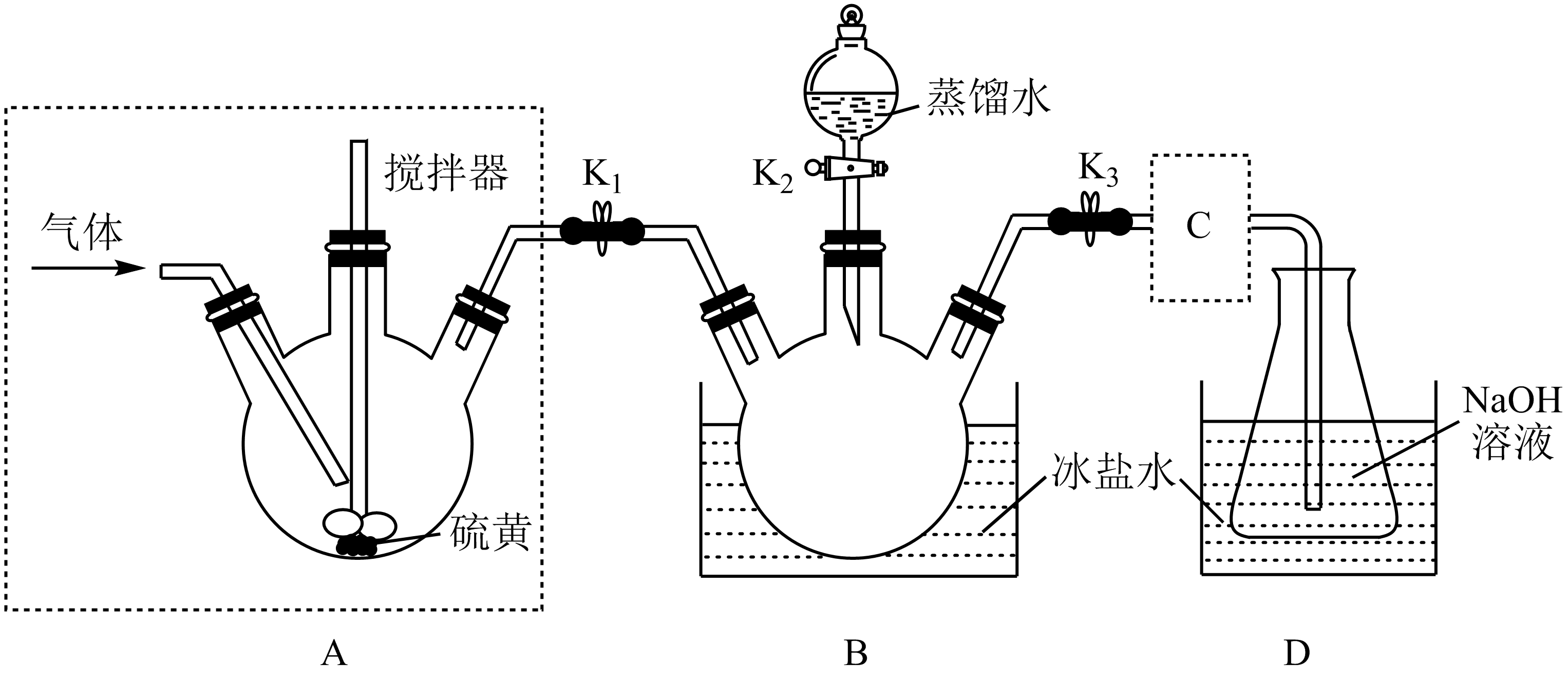
已知: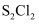 遇水发生反应
遇水发生反应 ;热稳定性差;能被
;热稳定性差;能被 氧化为
氧化为 ;硫黄的熔点为113℃,沸点为445℃,
;硫黄的熔点为113℃,沸点为445℃,
回答下列问题:
-
(1)
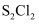 电子式为。
电子式为。
-
(2) 制备
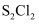 的实验步骤如下:
的实验步骤如下:步骤1:检查装置气密性,加入硫黄,通氮气;
步骤2:一段时间后加热A中三颈烧瓶至110℃~115℃,使硫黄熔化;
步骤3:改通氯气,于115℃~125℃氯化一段时间后改通氮气;
步骤4:......;
步骤5:停止加热,持续通氮气至冷却。
①步骤1开始时需打开关闭(填“
 ”、“
”、“ ”或“
”或“ ”)。通氮气的目的是;步骤4是。
”)。通氮气的目的是;步骤4是。②证明有
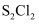 生成的现象是。反应过程应控制
生成的现象是。反应过程应控制 的量,原因是;装置C可选择(填标号)。
的量,原因是;装置C可选择(填标号)。
-
(3) 为测定产物纯度,实验操作如下:
Ⅰ.实验前称重B装置为
 , 实验后称重为
, 实验后称重为 (均不包含冰盐水),取出
(均不包含冰盐水),取出 产品备用,剩余产品进行后续实验;
产品备用,剩余产品进行后续实验;Ⅱ.撤掉装置A、C和B中冰盐水,重新更换足量的NaOH溶液,直接连接装置B、D;
Ⅲ.打开
 、
、 、
、 , 并不断向B中通入水蒸气、将
, 并不断向B中通入水蒸气、将 和
和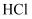 全部赶出;
全部赶出;Ⅳ.实验结束后,取下锥形瓶,滴加几滴酚酞,用
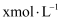 盐酸标准溶液滴定剩余的
盐酸标准溶液滴定剩余的 溶液,消耗盐酸
溶液,消耗盐酸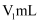 ;
;Ⅴ.不加样品,做空白对照实验,消耗盐酸
 。
。①产品中
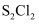 的纯度为(写出表达式)。
的纯度为(写出表达式)。②下列操作可能会导致测定结果偏高的是(填标号)。
a.水蒸气的通入时间较短
b.操作Ⅳ滴定后仰视滴定管读数
c.操作Ⅴ滴定前滴定管尖嘴处有气泡,滴定后无气泡
-
(1) 高铁酸钾的制备,装置如图1所示。
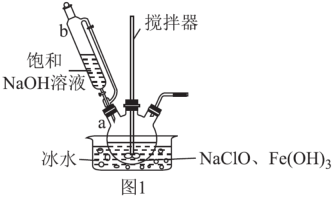
步骤一:将b中饱和NaOH溶液全部逐滴滴入a中,充分反应;
步骤二:由b向a中反应后液体中加入饱和KOH溶液;
步骤三:将a中所得浊液移出,分离提纯。
①仪器b的名称是,其侧管的作用为。
②a中制备Na2FeO4反应的离子方程式为。
③K2FeO4悬浊液经过滤、洗涤,可得粗产品。粗产品中的可溶性杂质可通过方法进一步提纯。
-
(2) K2FeO4遇水转化为Fe(OH)3 , 则其能用于净水的原理为:。
-
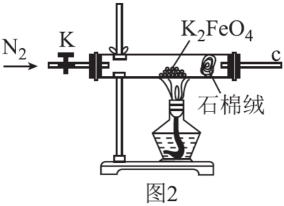
(3) 用图2所示装置探究K2FeO4受热分解的产物。设计实验方案证明完全分解后的固体产物中不含Fe(II):取完全分解后的少量固体,溶于稀硫酸,。
-
(4) 实验室可用间接碘量法测定含少量KCl杂质的K2FeO4样品的纯度:称取0.9000gK2FeO4样品溶于碱性KI溶液中,调节pH使混合液充分反应。用1.000mol·L-1的Na2S2O3标准溶液进行滴定,消耗Na2S2O3标准溶液15.00mL。请计算K2FeO4样品的纯度:。
已知:
 +4I-+8H+=Fe2++2I2+4H2O;I2+2
+4I-+8H+=Fe2++2I2+4H2O;I2+2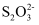 =
=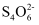 +2I-。
+2I-。

-
(1) 浸取:将软锰矿与硫铁矿粉碎混合,用硫酸浸取。研究发现,酸浸时,FeS2和MnO2颗粒构成两个原电池反应,其原理如图所示(部分产物未标出)。

①若FeS2原电池中生成单质S,其电池总反应的离子方程式为。
②随硫铁矿的增加,锰的浸出率降低,可能的原因是。
-
(2) 除钙镁:向已除去Fe、Al、Si元素的MnSO4溶液中(pH约为5)加入NH4F溶液,将Ca2+、Mg2+转化为氟化物沉淀。则
 =。 [已知Ksp(MgF2)=5×10-11 , Ksp(CaF2)=5×10-9]
=。 [已知Ksp(MgF2)=5×10-11 , Ksp(CaF2)=5×10-9]
-
(3) 氧化:将“沉淀”步骤所得含少量Mn2(OH)2SO4的Mn(OH)2固体滤出,洗净,加水打成浆,浆液边加热边持续通空气,制得Mn3O4。
①写出由Mn(OH)2反应得到Mn3O4的化学方程式。
②沉淀加热通空气过程中溶液pH随时间变化如图所示,其中pH先基本不变后迅速下降的原因是。

③所得产物中锰元素含量随通入空气时间的变化如图所示,当通空气时间超8小时,产物中锰元素含量减小的原因是。


 B . 装置丙的主要作用是吸收尾气中的氯化氢
C . 装置丁中发生反应的化学方程式为
B . 装置丙的主要作用是吸收尾气中的氯化氢
C . 装置丁中发生反应的化学方程式为 D . 冰水混合物的作用是降温,防止
D . 冰水混合物的作用是降温,防止 挥发
挥发