溶解度的影响因素 知识点题库
为探究固体A、B在水中的溶解情况,小明同学实验如下:取两支试管,分别加入一定质量的粉末A和粉末B(A、B均不与水反应),然后逐渐加入适量的水充分振荡并观察记录实验数据,得到了如图所示的图象(横坐标表示水的质量,纵坐标表示溶质的质量)。

-
(1) 所加粉末A和粉末B的质量大小关系是。
-
(2) 当加入30g水时,A溶液的质量为。
-
(1) 在t℃时,A物质的溶解度是多少?
-
(2) 原A溶液中A的质量分数是多少?
-
(1) 如表是KNO3、NaCl在不同温度下的溶解度(单位:g/100g水)
温度(℃)
0
10
20
30
40
50
60
70
80
90
100
KNO3
13.3
20.9
32
45.8
64
85.5
110
138
169
202
246
NaCl
35.7
35.8
36
36.3
36.6
37
37.3
37.8
38.4
39
39.8
Ⅰ.20℃时,NaCl的溶解度是 g.
Ⅱ.30℃时,KNO3溶液的最大浓度(溶质质量分数)为(只列计算式,不需要计算结果).
Ⅲ.KNO3中含少量氯化钠时,提纯硝酸钾的一般方法是.
Ⅳ.根据表内数据可知,KNO3和NaCl在某一温度时具有相同的溶解度X,则X的取值范围是.
-
(2) 如图是对20℃一定质量的甲的溶液进行恒温蒸发结晶的实验过程,请回答.

Ⅰ.蒸发前原溶液是(填“饱和”或“不饱和”)溶液.n的数值是.
Ⅱ.依据上述实验,你认为甲的溶解度随温度变化的趋势是(填字母).
A.随温度升高而增大 B.随温度升高而减小 C.无法判断.
是 ( )
①用高压锅煮饭,可以增大锅内气体的压强,使水的沸点(“升高”或“降低”),饭菜熟得更快. |
|
②切菜刀磨得很锋利,是为了切菜时,(“增大”、“减小”) 刀对菜的压强. |
|
③洗碗的时候我们发现:油很难在水中溶解,而易溶于洗洁精,这说明物质的溶解性和有关.(“温度”、“气压”或“溶质和溶剂的性质) |
|
④厨房里我们常用吸钩挂抹布,其实吸钩能够吸在墙上是因为的作用. |
|

-
(1) 衣服上的或手上的沾有的油污用水洗不容易洗去,而用汽油很容易去,其原因是。
-
(2) 烧开水时,随着温度的升高,沸腾前会出现气泡,想一想这些气泡产生的原因是。

| 0℃ | 10℃ | 20℃ | 30℃ | |
| 氯化钠 | 35.7g | 35.8g | 36.0g | 36.3g |
| 碳酸钠晶体 | 7.0g | 12.5g | 21.5g | 38.8g |
分析表中数据,下列几种说法中正确的是( )
|
温度(℃) |
0 |
10 |
20 |
30 |
40 |
|
|
溶解度(g) |
A |
35 |
35.5 |
36 |
36.5 |
37 |
|
B |
6 |
10 |
18 |
36.5 |
50 |
|
-
(1) 若将B物质从溶液中结晶析出,宜采用的方法是:。
-
(2) 我国有许多盐碱湖,湖中溶有大量的氯化钠和碳酸钠,那里的人们“冬天捞碱,夏天晒盐”。据此你认为表中(填“A”或“B”)物质的溶解度与氯化钠相似。



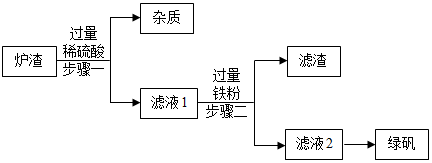
查阅资料:氧化亚铁与稀硫酸、铁与硫酸铁反应均可生成硫酸亚铁。
-
(1) 步骤一中的操作名称是。
-
(2) 步骤一中,写出其中反应的化学方程式为。
-
(3) 将滤液2蒸发浓缩、降温结晶、过滤,冰水洗涤,低温干燥后得到FeSO4·7H2O晶体,其中冰水洗涤的作用是。
-
(4) pH大小关系:滤液1<滤液2,造成该结果的原因是。







