有关化学式的计算和推断 知识点题库
维生素是人体必需的营养物质,某维生素D2的化学式为C28H44O,试计算:
-
(1) 维生素D2的相对分子质量:。
-
(2) 维生素D2中的碳、氢、氧三种元素的质量比:。
-
(3) 198克维生素D2含碳元素多少克?
央视二套《这是真的吗)栏目播出了电脑浸在液体中也能正常工作的新鲜事,原来这种无色的液体是被称作“绝缘液”的液态―氟二氯乙烷,这种液体可为手机电脑“洗澡",用来清洗电子产品,一氟二氯乙烷的化学式为(CCl2FCH3),下列对一氟二氯乙烷的认识,正确的是( )
A . 一氟二氯乙烷是氧化物
B . 一氟二氯乙烷的相对分子质量为117克
C . 一氟二氯乙烷由5种元素组成
D . ―氟二氯乙烷中碳元素与氢元素的质量比为8:1
氯酸钾(KClO3)相对分子质量的计算式,正确的是( )
A . 39×1+35.5×1+16×3
B . (39+35.5+16)×3
C . 39×1+35.5×1+16×1+3
D . 39+35.5×16×3
过碳酸钠俗称固体双氧水(化学式2Na2CO2·3H2O2),是一种无味、无毒的固体,有漂白杀菌、强力去污等多种功效,在高温下或者遇到水时容易分解产生大量氧气。下列说法错误的是( )
A . 过碳酸钠是混合物
B . 过碳酸钠可以作为急救供氧剂
C . 过碳酸钠遇到水容易分解属于化学性质
D . 过碳酸钠与洗涤剂配合,可制成高效洗涤剂
相同分子数的 CO 和 CO2 , 氧元素的质量比为,相同质量的 CO 和 CO2 , 氧元素的质量比为,使 CO2 和 CO 中含有相同质量的氧元素,则 CO2和 CO 的质量比是。
氯霉素属于广谱抗生素,能杀灭细菌,但摄入过多容易导致血液疾病,所以国家严令禁止在食品中使用。今年,广州市有关部门在抽检中发现,有些不法商贩向黄金贝、花蛤等海产品中添加氯霉素,来延长海鲜的存活期。这种滥用氯霉素的现象引起了市民的警觉。
-
(1) 氯霉素性质稳定,不易分解,这种性质属于(填“物理”或“化学”)性质。
-
(2) 氯霉素(化学式为C11H12Cl2N2O5)中碳元素和氧元素的质量比为。
-
(3) 长期使用氯霉素,细菌能对氯霉素产生耐药性。这是氯霉素对细菌进行的结果。
PLA是一种新型可降解塑料,能有效缓解塑料垃圾造成的白色污染。已知PLA由碳、氢、氧三种元素组成,为了测定7.2gPLA样品中的各种元素质量比,某化学兴趣小组进行了以下探究。
【实验设计】

以上实验装置如图正确的连接顺序是:A→→E→→C。
①【分析与结论】实验中选择纯净的氧气而不用空气的原因是。
②装置 C 的作用是。
③正确连接装置后,确认气密性良好。充分燃烧7.2gPLA样品,已知燃烧产物被完全吸收,测得相关实验数据见下表:
| 装置 | B | C | D | E |
| 实验前质量/g | 160 | 150 | 150 | 100 |
| 实验后质量/g | 163.6 | 150 | 163.2 | 100 |
通过分析与计算,该 PLA 样品中碳、氢、氧三种元素质量比为。
有些酸随着浓度的改变会表现出不同的化学性质。请回答下列问题:
-
(1) 用毛笔蘸取稀硫酸在竹片上画花,然后把竹片放在小火上烘干,再用水洗净,在竹片上就得到一幅精美的呈黑色或褐色的竹片画。在烘干的过程中稀硫酸变为浓硫酸,在制作竹片画的过程中利用了浓硫酸的性;
-
(2) 在加热的条件下浓硫酸与铜反应的化学方程式是Cu+2 H2SO4(浓)
 CuSO4+SO2↑ +2X,则X的化学式是。但足量的铜和浓硫酸充分反应后溶液中仍有少量硫酸剩余,其原因是。
CuSO4+SO2↑ +2X,则X的化学式是。但足量的铜和浓硫酸充分反应后溶液中仍有少量硫酸剩余,其原因是。
香烟的烟气中含有几百种有毒物质,其中的一氧化碳能与血红蛋白结合,可能导致人体缺氧室息。血红素是血红蛋白分子上的主要稳定结构,其化学式是C34H32N4FeO4。根据你现有的知识,请回答:
-
(1) 一个血红素分子中含有个原子,其中C、H、O、N、Fe各元素的原子个数比是。
-
(2) 经测定血红蛋白中铁元素的质量分数为0.335%,平均每个血红蛋白分子中含有n个铁原子,则血红蛋白的相对分子质量可用含n的代数式表示为。(不必化简)
瑞德西韦一度被认为是治疗新冠肺炎较为有效的药物,其主要成分的化学式是C27H35N6O8P,对此分析可得出的信息是( )
A . 相对分子质量为602克
B . 一个C27H35N6O8P,分子中有35个氢原子
C . 该分子由五种元素组成
D . 该物质是氧化物
化学上常用燃烧法确定有机物的组成。这种方法是在电炉加热时用纯氧气氧化管内样品,根据产物的质量确定有机物的组成。下图所列的是用燃烧法确定有机物分子式组成的装置,D装置用来产生氧气,反应方程式为: 2H2O2 2H2O+O2↑ 。
2H2O+O2↑ 。
 2H2O+O2↑ 。
2H2O+O2↑ 。
把上面所列的装置正确连接成实验装置后进行实验,回答下列问题:

-
(1) 图E中CuO的作用是。
-
(2) 若正确称取0.9克样品(只含C、H、O三种元素中的两种或三种),经充分燃烧后,A管质量增加1.32克,B管质量增加0.54克,则有机物的化学式(最简式)为 。
今年元宵节仙居美食“咸酸粥”成网红,一天内连续数次上央视。咸酸粥里面有各种各样的食材,其中必不可少的一种食材是芋艿。新鲜芋艿在去皮时会产生一种白色汁液,汁液内含有一种碱性物质---皂角素(C27H42O3),沾上它会奇痒难忍。

-
(1) 下列厨房物质可用来涂抹止痒的是 。(填字母)A . 食醋 B . 食盐水 C . 纯碱。
-
(2) 皂角素分子中碳与氢原子个数比为。
-
(3) 828克皂角素(C27H42O3)中含克碳元素。
某学校探究小组为了测定市面销售的某品牌纯碱(杂质为NaCl)中碳酸钠的质量分数。进行了如下实验: ①在三个烧杯中都加入了11克样品及足量的水配成溶液;②向三个烧杯加入质量不同的CaCl2粉末;③将充分反应后生成的沉淀过滤、洗涤、干燥得到W克的白色固体。实验数据如下:
|
烧杯I |
烧杯Ⅱ |
烧杯Ⅲ |
|
|
加入CaCl2的质量/克 |
5.55 |
12 |
15 |
|
W/克 |
5 |
10 |
10 |
-
(1) 碳酸钠中钠、碳、氧三种元素的质量比(最简比)为。
-
(2) 将烧杯Ⅱ的滤液蒸干,得到的固体成分是(只填化学式)。
-
(3) 样品中碳酸钠的质量是多少?
机动车尾气排放出的NO是城市空气主要污染源之一。关于NO的叙述中,错误的是( )
A . 由氮元素和氧元素组成
B . 一个NO分子中共有两个原子
C . 它的名称叫一氧化氮
D . NO中N元素的化合价为+1
为了实现碳中和,植树造林是人类抵消自身产生的二氧化碳排放,实现二氧化碳“零排放”的重要 手段之一。纤维素[(C6H10O5)n]是植物细胞壁的主要成分, 占植物界碳含量的 50%以上。
-
(1) 纤维素属于(填“有机物”或“无机物”)。
-
(2) 纤维素中碳、氢、氧元素质量比。
-
(3) 纤维素在氧气中完全燃烧的产物是。
尿素[CO(NH2)2]作为一种有机氮肥,是目前含氮量最高的氮肥。工业上可用 CO2 和 NH3 在一定条件下合成。常温下,尿素是一种无色或白色针状或棒状结晶体,呈弱碱性。
-
(1) 尿素中氮元素的质量分数约为。(计算结果精确至0.1%)
-
(2) 证明尿素呈碱性的具体实验操作是:。
-
(3) 不合理施用化肥导致氮、磷元素过剩, 不仅造成化肥的流失, 而且还给人类的生活 环境造成了巨大的影响,其中不包括____。A . 水土大量流失 B . 地表水和地下水污染 C . 近海赤潮频繁发生 D . 湖泊水库、沿海水体富营养化
-
(4) 小科购买了一款氮肥, 相关信息如图所示, 请计算该氮肥中尿素[CO(NH2)2]的质量 分数约是多少? (计算结果精确至 0.1%)
氮肥(尿素) [CO(NH2)2] 净重: 50kg
含氮量: 46%
氮肥能促使作物的茎、叶生长茂盛,叶色浓绿。某同学发现她家花盆中的花草生长迟 缓,便施用了一种氮肥。右图是该氮肥包装标签的部分文字。试根据相 关信息计算:

-
(1) 碳酸氢铵由种元素组成
-
(2) 碳酸氢铵中的碳元素和氧元素的质量比是(最简整数比)
-
(3) 通过计算碳酸氢铵中氮元素的质量分数确定此氮肥是否为合格产品?
央视《这是真的吗》栏目播出了电脑浸在液体中也能正常工作的新鲜事,原来这种无色的液体是被称作“绝缘液”的液态-氟二氯乙烷(CCl2FCH3),这种液体可为手机电脑“洗澡”,用来清洗电子产品。
-
(1) 一氟二氯乙烷是。(填“无机物”或“有机物”)。
-
(2) 一氟二氯乙烷中碳、氢、氯三种元素的质量比为。
-
(3) 117 g一氟二氯乙烷中碳元素的质量为g。
小乐为了获知某化肥(主要成分为NHHCO3 , 杂质不含氮元素)的含氮量,设计了如图所示实验装置进行测定。

已知:①NH4HCO3 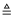 NH3↑+CO2↑+H2O;
NH3↑+CO2↑+H2O;
②NH3能被浓硫酸吸收,不能被氢氧化钠固体吸收。
-
(1) 装置B的作用是。
-
(2) 将化肥样品装入试管前,必须进行的一步操作是。
-
(3) 待装置符合实验要求后,取20克化肥样品装装置「反应前质量/克T反应后质量/克入试管,通入氮气排尽试管内的空气,然后点燃酒精灯,每步都充分反应后,再通入氮气。装置B和C反应前后质量如表所示:则反应生成的氨气的质量为克; 此化肥的含氮量为。
装置
反应前质量/克
反应后质量/克
B
186
198.4
C
159
162.4
定性和定量结合是科学研究的重要思想。某科学学思小组为检测实验室用H2还原CuO所得红色固体Cu中是否含有Cu2O(红色),进行了如下探究。
【查阅资料】
①无水CuSO4遇水变蓝;
②高温灼烧CuO生成Cu2O和O2;
③Cu2O与稀H2SO4反应:Cu2O+H2SO4═Cu+CuSO4+H2O
【设计实验方案】

-
(1) 为确保探究的科学、合理、安全。方案中还应采取的措施有 (填序号);
①加热前先排尽装置中的空气
②在氢气发生器与玻璃管之间加一个干燥装置
③在盛有无水硫酸铜的干燥管后再连接一个装有浓H2SO4的洗气瓶
-
(2) 实验可以通过来来判断红色固体中是否含有Cu2O。
方案2:利用高温灼烧红色固体,通过比较质量来确定红色固体中是否含有Cu2O。如图2所示,称得干燥坩埚(常用于固体加热的容器)的质量为ag,取红色固体置于坩埚中称得总质量为bg,在空气中高温灼烧至质量恒定,称得最后坩埚与固体总质量为cg。
-
(3) 若确认红色固体中含有Cu2O,则c与a、b应符合的数学关系式为。
-
(4) 除上述方法之外,你还有什么方法判断上述红色固体中是否含有Cu2O?。
最近更新



