氧气的检验和验满 知识点题库
化学实验操作的正确性、规范性是科学探究成败的关键因素之一.下列实验操作中,错误的是( )
A . 熄灭酒精灯火焰 B . 氧气验满
B . 氧气验满 C . 检查装置的气密性
C . 检查装置的气密性 D . 蒸发食盐水
D . 蒸发食盐水
 B . 氧气验满
B . 氧气验满 C . 检查装置的气密性
C . 检查装置的气密性 D . 蒸发食盐水
D . 蒸发食盐水
实验小组同学做了如下实验.

-
(1) A中反应的化学方程式为 ,将带火星的木条置于a处,若观察到 , 说明已有氧气产生.
-
(2) B中现象是迅速涌出柱状的泡沫,可形象地称为“大象牙膏”,其原理主要是H2O2在某些催化剂作用下迅速分解产生水和氧气.反应的化学方程式为 .
下图分别是实验室氧气制备、收集、验满、验证性质的操作,其中正确的是( )
A .  B .
B .  C .
C .  D .
D . 
 B .
B .  C .
C .  D .
D . 
利用下图所示的装置回答问题。

A B C
-
(1) 写出图中仪器a的名称。
-
(2) 实验室用过氧化氢溶液制取氧气,选用的发生装置是(填字母序号)。
-
(3) 用D装置收集氧气时,验满的方法是。
下列实验设计或操作,能达到实验目的是( )
A .  干燥氢气
B .
干燥氢气
B .  检验氧气是否集满
C .
检验氧气是否集满
C .  检验X溶液中是否含有
检验X溶液中是否含有 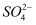 D .
D .  验证Zn、Fe、Cu的活动性强弱
验证Zn、Fe、Cu的活动性强弱
 干燥氢气
B .
干燥氢气
B .  检验氧气是否集满
C .
检验氧气是否集满
C .  检验X溶液中是否含有
检验X溶液中是否含有 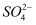 D .
D .  验证Zn、Fe、Cu的活动性强弱
验证Zn、Fe、Cu的活动性强弱
实验室检验氧气应该选用( )
A . 灼热的氧化铜
B . 澄清石灰水
C . 紫色石蕊溶液
D . 带火星的木条
根据下列实验装置图,回答问题:

-
(1) 写出图中仪器①的名称。
-
(2) 实验室制取氧气,在加入药品前必须进行的一步操作是。
-
(3) 若用过氧化氢溶液和二氧化锰制取干燥的氧气,所选气体发生、干燥和收集装置的接口连接顺序是(用接口字母和“→”表示)。
-
(4) 用排水法收集氧气时,当水槽中集气瓶内的水排尽后,把集气瓶转移到桌面上的操作是。
-
(5) 检验瓶中气体为氧气的操作是。
按下列装置实验,不能达到对应目的的是 ( )
A .  收集H2
B .
收集H2
B .  O2验满
C .
O2验满
C .  配制20%的Ca(OH)2溶液
D .
配制20%的Ca(OH)2溶液
D .  除去CO中的CO2
除去CO中的CO2
 收集H2
B .
收集H2
B .  O2验满
C .
O2验满
C .  配制20%的Ca(OH)2溶液
D .
配制20%的Ca(OH)2溶液
D .  除去CO中的CO2
除去CO中的CO2
小黄为了探究过氧化钠(Na2O2)和CO2的反应,设计了如图实验,同时也查阅了相关资料:

资料一:过氧化钠与二氧化碳和水都能发生反应,且都放出热量。化学方程式分别为
2Na2O2+2CO2=2Na2CO3+O2
2Na2O2+2H2O=4NaOH+O2↑
资料二:氢氧化钙的溶解度随着温度的升高而降低。
-
(1) 为了证明过氧化钠与二氧化碳反应是否产生氧气,请在a处增加一个实验操作:。
-
(2) 实验装置C中无水硫酸铜的作用是。
-
(3) 请解释D装置中饱和澄清石灰水变浑浊的原因:。
区别空气和氧气两瓶气体的方法是 ( )
A . 比较气体的颜色
B . 闻气味
C . 用带火星的木条试验
D . 分别倒入澄清的石灰水
如图所示的演示实验中,集气瓶中的气体为( )

A . 二氧化碳
B . 氧气
C . 氢气
D . 氮气
根据下列实验方案进行实验,不能达到相应实验目的的是( )

A . 甲:测定空气中氧气的含量
B . 乙:检验氧气是否收集满
C . 丙:验证物质燃烧需要氧气
D . 丁:探究影响物质溶解性的因素
小龙通过图示实验装置(夹持部分已略去)及药品,按如下实验步骤,验证了可燃物燃烧的条件。其中实验装置气密性良好,所用药品均足量(已知红磷的着火点为240℃,白磷的着火点为40℃)。


步骤一:向大烧杯中注入足量的冷水,打开K1关闭K2 , 向下压左侧注射器活塞,使生成的氧气持续通入U形管,并观察U形管中现象;
步骤二:关闭K1、打开K2 , 向下压右侧注射器活塞,使生成的二氧化碳将U形管内的氧气排尽,然后将烧杯中的冷水换成等量的80℃的热水,并观察U形管中现象;
步骤三……并观察U形管中现象。
-
(1) 根据图示信息,写出生成氧气的化学方程式。
-
(2) 简述步骤二中判断U形管内氧气已经排尽的方法。。
-
(3) 补充完整步骤三的操作,并写出U形管中应观察到的现象。。
科学发现往往源于对实验现象的观察与研究。

-
(1) 如图甲进行白糖溶解实验,根据图中现象判断:溶液②(填“是”“不是”或“可能是")白糖的饱和溶液。
-
(2) 如图乙所示,小科利用集气瓶收集从导管导出的氧气时,每隔一段时间,他就取出导管,再用带火星的木条放在瓶口验满。可是他始终没有观察到带火星木条复燃,小科实验操作中出现的错误是。
乙炔气体燃烧会放出大量热量,乙炔在烧焊金属时有重要作用。乙炔燃烧的反应过程:
如图所示:

实验室检验物质乙的方法是,反应中甲、乙两种物质分子个数比是。
如图所示为李强同学做“氧气的制取、收集和验满”实验的主要步骤,其中正确的( )
A . 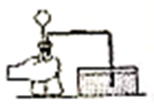 检查装置气密性
B .
检查装置气密性
B .  加入药品
C .
加入药品
C .  收集气体
D .
收集气体
D . 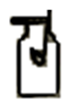 验满
验满
 检查装置气密性
B .
检查装置气密性
B .  加入药品
C .
加入药品
C .  收集气体
D .
收集气体
D .  验满
验满
如图甲所示为电解水实验的装置图,电解水时,常在水中加入氢氧化钠来增强溶液的导电性,而氢氧化钠在此过程中不会变成其他物质。

-
(1) 由图甲可知(选填“a”或“b”)管中的气体是氢气。
-
(2) 写出检验b管中气体的方法:。
-
(3) 在图乙方框中将电解水反应的微观过程补充完整。
-
(4) 在电解过程中,氢氧化钠的溶质质量分数(选填“变大”“变小”或“不变”)。
2021年10月,神舟十三号成功进驻天宫空间站,开启了新的旅程。他们将在轨生活6个月。空间站的氧气源自电解水。如图是某空间站能量转化系统局部示意图。

-
(1) 其中燃料电池系统实现的能量转化是。
-
(2) 水电解系统中若想检验产生的气体是氧气的方法是。
小宁在网上观看了“吹气生火”的实验视频,只见向包有过氧化钠(Na2O2)粉末的脱脂 棉上用导管吹气,脱脂棉燃烧了起来。那过氧化钠到底发生了什么反应呢?为此他设计了如图所示装置,打开K向过氧化钠粉末中不断吹气,观察到过氧化钠粉末由淡黄色逐渐变为白色,在导管口P处放置带火星木条条复燃,说明试管内生成了。

那试管内的白色固体是什么呢?
他查阅资料得知:①吹出的气体主要成分有氮气、二氧化碳和水蒸气;
②过氧化钠与氮气不反应。
[提出猜想] 猜想1:CO2参加反应,固体成分是Na2CO3;
猜想2:H2O参加反应,固体成分是NaOH;
猜想3:CO2和H2O均参加反应,固体成分是Na2CO3和NaOH。
[实验验证] 取残留白色固体于试管中配成溶液,向其中加入溶液,产生白色沉淀;静置后取适量的上层清液于试管中,向其中滴加无色酚酞,溶液变红。
[实验结论] 猜想正确。
[拓展延伸] 化工厂存有过氧化钠时,一旦失火,不能选用(填字母序号,可多选)灭火。
A.二氧化碳 B.细沙 C.水
下图是电解水的简易装置。

-
(1) 水中加入氢氧化钠是为了。
-
(2) 怎么检验试管1 中气体。
-
(3) 写出该反应的文字表达式。
最近更新



