金属锈蚀的条件及其防护 知识点
防护:保持表面洁净干燥、涂保护层如涂油、刷漆等
金属锈蚀的条件及其防护 知识点题库
试根据图中及文字信息回答下列问题:
(1)厨房中的铁质水龙头表面镀一层金属铬,其目的是;
(2)如图玉米由于缺乏氮元素导致叶子发黄,为了使玉米增产增收,可以施用含有氮元素的化肥,该类化肥的作用是 ;
(3)汽车用铅蓄电池中含有的酸的化学式是。
(1)性质决定用途.以下连线正确的是 (填字母).

(2)用Fe粉制成的食品保鲜剂使用一段时间后,会逐渐变为 色的氧化铁.
(3)铁制品易发生锈蚀,请写出一种防止铁生锈的方法 .
(4)用氯化物 (填化学式)溶液可以一次性验证Fe、Cu、Ag三种金属的活动性顺序.
-
(1) 铁与空气中的水和直接接触会导致铁制品的锈蚀.
-
(2) 不锈钢属于 (填序号).A . 纯净物 B . 金属材料 C . 合成材料 D . 复合材料
-
(3) 某化学兴趣小组的同学为了探究锰、镁、铜三种金属的活动性,他们首先将锰片插入到氯化镁溶液中,一段时间后观察到锰片表面无明显变化;将锰片插入到氯化铜溶液中,一段时间后观察到锰片表面有红色物质生成.
①根据以上实验判断,三种金属的活动性由强到弱的顺序是.
②写出单质锰(Mn)与氯化铜溶液反应的化学方程式(该化合物中Mn元素显+2价).

-
(1) A中细铁丝燃烧生成黑色固体物质的化学式是;
-
(2) B中铁钉最易生锈的部位是(填“a”、“b”或“c”);
-
(3) C试管内发生反应的化学方程式是;
-
(4) D中反应一段时间后,试管内溶液质量与反应前相比 (填增大、不变或减小),发生反应的方程式为.
-
(1) 用铜制电线主要是利用铜具有良好的性;
-
(2) 铁制品锈蚀,实际上是铁跟空气中的发生了化学反应.
-
(1) 根据下列实验方案进行实验(图1),能达到相应实验目的是( )
 A . 图A比较Zn和Fe的金属活动性强弱 B . 图B探究铁钉生锈时O2是否参与反应 C . 图C比较红磷和白磷的着火点 D . 图D测定空气中O2的含量
A . 图A比较Zn和Fe的金属活动性强弱 B . 图B探究铁钉生锈时O2是否参与反应 C . 图C比较红磷和白磷的着火点 D . 图D测定空气中O2的含量 -
(2) 某同学对硫在氧气中燃烧的实验作了如图所示的改进
①硫在氧气中燃烧时火焰的颜色为.
②硫燃烧产生的SO2可以溶解在NaOH溶液中,该反应与CO2溶解在NaOH溶液中的反应相似,该反应的化学方程式为.
③该改进实验的最大优点是.
-
(3) 某同学在实验室中用盐酸与石灰石反应制气体,将制得的气体通入澄清石灰水中,发现石灰水始终不变浑浊,于是该同学对不变浑浊的原因进行了如下实验探究(图2).
【查阅资料】CO2既不与AgNO3溶液反应,也不与饱和NaHCO3溶液反应.
【提出猜想】①澄清石灰水已经变质.②制得的气体中除CO2外还含有其他成分.
【实验探究】
活动一:为了验证猜想①,该同学做了一个对照实验:把稀硫酸滴入盛有碳酸钾溶液的试管中,并将产生的气体通入这种澄清石灰水,石灰水变浑浊了,则稀硫酸与碳酸钾溶液反应的化学方程式为.由该实验得出的结论是:猜想①(填“成立”或“不成立”).
活动二:将盐酸与石灰石反应制得的气体通入硝酸银溶液中,观察到有产生,说明制得的气体中含有HCl气体.
【实验反思】制得的气体中混有HCl的原因是;澄清石灰水始终不变浑浊又是因为(用化学方程式表示).
【拓展应用】若要除去CO2中混有的HCl和水蒸气,下列装置(图3)可以满足要求的是.
-
(1) “小苏打”的化学名称是.
-
(2) 防止菜刀生锈的常用方法是.
-
(3) 小明在家看到爸爸欲将碳酸氢铵与草木灰混用,赶紧制止,原因是.
实验一:探究铁制品生锈的条件

实验二:探究影响铁制品锈蚀快慢的因素(稀氨水和稀醋酸的质量分数相同)
| 实验序号 | ① | ② | ③ | ④ |
实验温度/℃ | 25 | 25 | 70 | 70 | |
试剂 | 稀氨水 | 稀醋酸 | 稀氨水 | 稀醋酸 | |
出现铁锈 所需时间 | 1天 未见锈蚀 | 5分钟 | 1天 未见锈蚀 | 1分钟 |
-
(1) 实验一的乙中植物油的作用是。
-
(2) 由实验一探究铁制品生锈结果可知铁锈中含有的元素是。
-
(3) 实验②和④可探究因素对铁制品锈蚀快慢的因素;欲探究试剂酸碱性对铁制品锈蚀快慢的影响,应选择的实验是(填实验序号)。
-
(4) 由实验二表中实验现象得出的结论是 。
-
(1) 天然水有硬水和软水之分,硬水给人们的生活和生产带来很多麻烦,生活中可用来区分硬水和软水,常用的方法来软化硬水;
-
(2) 衣服面料中的腈纶和羊毛可用法区别;
-
(3) 电动汽车,低碳环保,真正实现了节能减排,备受人们青睐。电动汽车在进行铅酸电池充电时,发生的反应为:
2PbSO4+2H2O
 Pb+2H2SO4+x,则x的化学式为;
Pb+2H2SO4+x,则x的化学式为; -
(4) 汽车外壳材料主要是钢,汽车表面喷漆,主要是为了防锈,钢铁在空气中锈蚀,实际上是铁跟空气中的共同作用的结果。
-
(1) “衣”:某品牌男上衣服标签上标着“80%毛、20%氨纶”,氨纶属于纤维(填“合成”或“天然”)
-
(2) “食”:食品包装袋中(如薯片)充有氮气,其作用是。
-
(3) “住”:房屋装修后,可在室内放置活性炭来吸收装饰材料释放的有毒气体,这是利用活性炭的。性。
-
(4) “行”:自行车是绿色出行的交通工具,自行车支架表面制度,是为了防止其与空气中的。发生反应而生锈。
-
(1) 妈妈做她最爱吃的“红烧肉”时加入了“加铁酱油”,其中“加铁酱油”中的“铁”指(填“元素”或“原子”),身体一旦缺铁可能患有的疾病是;
-
(2) 她发现加洗洁精能轻松除去碗碟上的油污.这是利用了洗洁精的作用;
-
(3) 妈妈说,要多喝牛奶,牛奶可以补充人体所需六大营养素中的;
-
(4) 她洗漱时发现卫生间内铁质的置物架生锈了,置物架生锈与有关,为了防止铁制品生锈,可采取哪些措施(填一点).
-
(5) 加油站、面粉加工厂应张贴下列标志中的;

-
(6) 小明同学刚做完CO2的性质实验后,用烧杯罩住两支点燃的、高矮不同的蜡烛(如图),竟看到了高蜡烛先熄灭的现象,请你帮他解释.

-
(1) 在钢铁表面涂油,可以防止钢铁生锈的主要原理是。
-
(2) 电动车蓄电池中所用的电解液是质量分数约为28%的硫酸,用300g质量分数为98%的浓硫酸稀释成28%的硫酸,需加水的质量为。
-
(3) 只用一种试剂就能一次性判断金属银、铝、锌的活动性顺序,该试剂是__________(填字母)。A . AgNO3溶液 B . Al2(SO4)3溶液 C . ZnSO4溶液
-
(1) 如图所示实验中热水的作用是。

-
(2) 配制一定溶质质量分数的氯化钠溶液时,量取水的操作如图所示,则所配溶液的溶质质量分数会。(填“偏大”或“偏小”)。

-
(3) 如图实验中能得到铁生锈的条件之一是。

-
(4) 如图实验中高锰酸钾可以溶解在水中,却几乎不溶于汽油,此实验说明同种物质在不同种溶剂里不同。

(知识回顾)用如图所示实验进行铁钉腐蚀的研究。一段时间后试管A、B中铁钉几乎没有生锈,而试管C中铁钉明显锈蚀,试管D、E中铁钉严重锈蚀。

-
(1) 由A、B、C的现象可知,铁的锈蚀是铁跟(填化学式)等物质作用的过程。
-
(2) 试管B中使用“煮沸并迅速冷却的蒸馏水”,其目的是。
-
(3) (实验探究)向试管D中(含生锈铁钉)加入过量10%稀盐酸,浸泡。可观察到铁锈逐渐消失,铁钉表面有气泡产生,溶液呈黄色,一段时间后黄色变为浅绿色。
写出铁锈溶于盐酸的化学方程式:。
-
(4) 推测试管D中溶液由黄色变为浅绿色,可能是因为氯化铁与某些物质发生反应所致。现进行如下3个实验(持续10小时,已知氢气不影响该反应)。
序号
实验I
实验Ⅱ
实验Ⅲ
实验内容

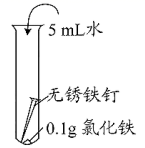

现象
溶液颜色始终呈黄色
产生红褐色沉淀
溶液逐渐由黄色变浅绿色
①设计实验I的目的是。
②综合分析上述3个实验,试管D中溶液由黄色变为浅绿色的原因是。
-
(5) (拓展延仲)研究水样的pH、水中溶解氧浓度与钢铁腐蚀速率的关系。查阅相关文献得到如下资料。
如图表示水样温度22℃、氧含量6mL·L-1时,钢铁腐蚀速率与水样pH的关系。当pH<4时,钢铁腐蚀速率明显增大的原因是。

-
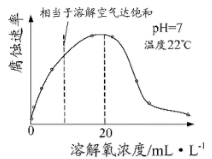
(6) 如图表示温度22℃、pH=7时,钢铁腐蚀速率与水中溶解氧浓度的关系。当溶解氧超过20mL·L-1时,钢铁腐蚀速率明显下降的原因可能是。
-
(1) 制作材料中属于金属材料的是(选填一种物质编号)。
-
(2) 豆浆机外壳在潮湿的空气中会锈蚀,这是铁与空气中的和水蒸气等物质发生化学反应的结果。
-
(3) 将豆渣和豆浆分离的方法类似于我们实验中的操作。
-
(4) 制作材料中的铜能与浓硝酸反应,反应的化学方程式为
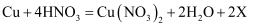 , X的化学式为。
, X的化学式为。
-
(1) 今年新冠病毒肆虐全球,抗疫过程我们用到了多种材料。修建火神山、雷神山两座医院时,用到了大量铝合金材料,铝合金密度小、硬度大、耐腐蚀。铝制品耐腐蚀的原因是(请用 化学反应方程式表示)。
-
(2) 近年来,我国高铁建设促进了经济、社会的快速发展。制造铁轨的材料是铁合金,与纯铁相比较,铁合金具有的优良性能(答一点)。
-
(3) 早在明代宋应星所著的《天工开物》里就对铁器的生产和使用有所记载,到了现代,炼铁技术得到进一步发展。炼铁的原理是利用一氧化碳与氧化铁 的反应,请写出该反应的化学方程式,该反应(填“属于”或“不属于”)置换反应。
-
(4) 钢窗表面喷漆不仅美观,而且可有效防止铁与空气中的 接触而生锈。
-
(5) 为了防止家中常用的铁锅生锈,你的做法是;除防止金属腐蚀外,请再写出一条保护金属资源的有效途径:。
-
(6) 工业上可用稀盐酸除去铁锈,该反应的化学方程式为
-
(1) 下列物品中,主要利用金属导电性的是____(填字母)。A . 铜导线 B . 铁锅 C . 金项链 D . 铝箔
-
(2) 对钢铁制品进行“烤蓝”处理,使其表面生成一层致密的氧化膜,氧化膜能有效防止钢铁锈蚀的原理是什么?
-
(3) 利用图所示装置探究锌和银的金属活动性强弱,所用无色溶液可能是(答出一种即可)。

-
(4) 下图装置是进行“一氧化碳还原氧化铁”及其产物检验的实验。(已知草酸在浓硫酸存在并加热的条件下,可分解生成CO、CO2和H2O)

①装置C中酒精灯加网罩的目的是。
②写出氧化铁被还原的化学方程式:。
③实验过程中观察到澄清石灰水没有变浑浊,试分析其原因:。
④装置B的作用是除去混合气体中的二氧化碳和水蒸气,实验结束后请你设计实验证明装置B中有NaOH剩余。(写出实验方法、现象和结论)
-
(5) 某化学兴趣小组对生锈的废铁锅中铁的含量进行测定。该化学兴趣小组的同学将一废铁锅粉碎后,称取20g碎屑放入烧杯中,缓慢加入50g稀硫酸并不断搅拌(除铁、氧化铁以外的物质都不与稀硫酸反应),充分反应后,溶液呈酸性,烧杯中剩余物质的质量为69.5g。求该废铁锅中铁的质量分数。




