用水稀释改变浓度的方法 知识点
用水稀释改变浓度的方法
用水稀释改变浓度的方法就是指为了某种需要,向浓溶液中加入适量的水(如果是稀释浓硫酸时,应该将浓硫酸沿器壁慢慢地注入水中,并用玻璃棒不断搅拌),将其稀释的所要求的浓度的方法。
注意事项
要想顺利达到这个目的,必须做到以下几点:
首先,要进行准确地计算;由于溶液稀释前后,溶质的质量是不变的。
然后,要进行准确地称量(或量取);一般只需要用量筒量取所加水的体积即可,注意读数时一定要平视量筒内凹液面的最低处。
最后,将所量取的水慢慢地倒入盛浓溶液的烧杯中(不能洒落到烧杯外面),并用玻璃棒不断搅拌。切不可在量筒内进行稀释的实验操作。
用水可以稀释溶液的浓度,在稀释前后,溶质的质量不变,只是水的质量增加,溶质的质量分数变小。
用水稀释改变浓度的方法就是指为了某种需要,向浓溶液中加入适量的水(如果是稀释浓硫酸时,应该将浓硫酸沿器壁慢慢地注入水中,并用玻璃棒不断搅拌),将其稀释的所要求的浓度的方法。
注意事项
要想顺利达到这个目的,必须做到以下几点:
首先,要进行准确地计算;由于溶液稀释前后,溶质的质量是不变的。
然后,要进行准确地称量(或量取);一般只需要用量筒量取所加水的体积即可,注意读数时一定要平视量筒内凹液面的最低处。
最后,将所量取的水慢慢地倒入盛浓溶液的烧杯中(不能洒落到烧杯外面),并用玻璃棒不断搅拌。切不可在量筒内进行稀释的实验操作。
用水可以稀释溶液的浓度,在稀释前后,溶质的质量不变,只是水的质量增加,溶质的质量分数变小。
用水稀释改变浓度的方法 知识点题库
水是一种重要的自然资源。下列对水的认识正确的是
A . 在河水中加入明矾可除去所有杂质
B . 提倡长期用纯水(蒸馏水)烧菜、煮饭等
C . 水体有自净能力,未经处理的生活污水可任意排放
D . 在淡水资源缺乏的海岛上,可考虑用蒸馏法从海水中提取淡水
如果要将100g溶质质量分数为20%的硝酸钾溶液稀释成溶质质量分数为10%的硝酸钾溶液,需加水的质量为
A . 50g
B . 90g
C . 100g
D . 200g
将100g溶质质量分数为10%的蔗糖溶液稀释到5%,需加入水的质量为( )
A . 10g
B . 50g
C . 90g
D . 100g
下列涉及学科观点的有关说法正确的是( )
A . 根据微粒观:水是由氢原子和氧原子构成的
B . 根据转化观:一氧化碳和二氧化碳在一定条件下可相互转化
C . 根据结构观:氩原子和氯离子最外层电子数相同,化学性质相同
D . 根据守恒观:10mL质量分数40%的硫酸,加10mL水后质量分数变为20%
浓H2SO4在空气中敞口放置一段时间后,其溶质的质量分数会(填“增大”、“减小”或“不变”);将20g质量分数为98%的浓H2SO4稀释为10%的H2SO4 , 需要水的质量为g.
下列图象一定不能正确反映其对应关系的是( )
A .  某温度下,向一定量的氯化钠溶液中不断加入水
B .
某温度下,向一定量的氯化钠溶液中不断加入水
B . 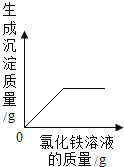 向一定量的盐酸和氯化铁的混合溶液中逐滴加入氢氧化钠溶液
C .
向一定量的盐酸和氯化铁的混合溶液中逐滴加入氢氧化钠溶液
C .  向一定量的氢氧化钠溶液中逐滴加水稀释
D .
向一定量的氢氧化钠溶液中逐滴加水稀释
D . 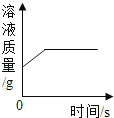 一定量的稀硫酸与锌粒反应,溶液的质量与反应时间的关系
一定量的稀硫酸与锌粒反应,溶液的质量与反应时间的关系
 某温度下,向一定量的氯化钠溶液中不断加入水
B .
某温度下,向一定量的氯化钠溶液中不断加入水
B .  向一定量的盐酸和氯化铁的混合溶液中逐滴加入氢氧化钠溶液
C .
向一定量的盐酸和氯化铁的混合溶液中逐滴加入氢氧化钠溶液
C .  向一定量的氢氧化钠溶液中逐滴加水稀释
D .
向一定量的氢氧化钠溶液中逐滴加水稀释
D .  一定量的稀硫酸与锌粒反应,溶液的质量与反应时间的关系
一定量的稀硫酸与锌粒反应,溶液的质量与反应时间的关系
用5g质量分数为98%的浓硫酸稀释为质量分数为20%的稀硫酸,需要水的质量是 g;在所得的溶液中滴加酚酞试液,再继续滴加氢氧化钠溶液,当溶液由色变为红色时,所得溶液的溶质是,该反应的基本反应类型是.
如图是A、B的溶解度曲线.t2℃时分别将100gA、B的饱和溶液降温至t1℃,析出固体质量AB(填“>”、“<”或“=”);把t2℃时150gA的饱和溶液稀释为20%,需加水 g.

欲用溶质质量分数为15%的氯化钠溶液配制300g溶质质量分数为10%的氯化钠溶液,求需15%的氯化钠溶液多少克?(解题步骤)
汽车、电动车一般使用铅蓄电池.某铅蓄电池使用的酸溶液是质量分数为20%的稀硫酸.请回答下列有关问题:
-
(1) 若使用100g质量分数为98%的浓硫酸(密度为1.84g/cm3)配制该稀硫酸时,需要蒸馏水(密度为1g/cm3)的体积为 mL(精确到0.1);需要硫酸的质量为 g.
-
(2) 用量筒量取浓硫酸时俯视读数,所配溶液溶质质量分数 20%(填“大于”、“小于”或“等于”).
将80g质量分数为35%的浓盐酸,稀释成10%的稀盐酸,需加水的质量为( )
A . 80g
B . 100g
C . 200g
D . 280g
下列图像关系合理的是( )
A .  向pH=10的NaOH溶液中加入水
B .
向pH=10的NaOH溶液中加入水
B . 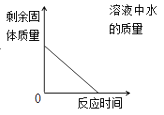 加热KClO3和MnO2固体混合物制取O2
C .
加热KClO3和MnO2固体混合物制取O2
C . 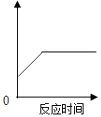 双氧水和二氧化锰制氧气
D .
双氧水和二氧化锰制氧气
D . 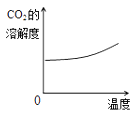 从冰箱里拿出汽水打开瓶盖后有大量气泡冒出
从冰箱里拿出汽水打开瓶盖后有大量气泡冒出
 向pH=10的NaOH溶液中加入水
B .
向pH=10的NaOH溶液中加入水
B .  加热KClO3和MnO2固体混合物制取O2
C .
加热KClO3和MnO2固体混合物制取O2
C .  双氧水和二氧化锰制氧气
D .
双氧水和二氧化锰制氧气
D .  从冰箱里拿出汽水打开瓶盖后有大量气泡冒出
从冰箱里拿出汽水打开瓶盖后有大量气泡冒出
食盐在生产和生活中具有广泛的用途,是一种重要的资源,海水中储量很丰富。

-
(1) 海水晒盐的原理是。
-
(2) 晒盐过程中得到粗盐和卤水。卤水的主要成分及其溶解度的变化如右图。t2℃时,MgCl2的溶解度为g。将t2℃时MgCl2、KCl和MgSO4三种物质的饱和溶液分别降温至t1℃时,析出晶体的是(填化学式)。
-
(3) 将纯净的氯化钠固体配制成溶液。20℃时,向4个盛有50g水的烧杯中,分别加入一定质量的氯化钠并充分溶解。4组实验数据如下表:
实验序号
①
②
③
④
加入氯化钠的质量/g
4.5
9
18
20
溶液质量/g
54.5
59
68
68
关于上述实验的叙述不正确的是 (填字母序号)。
A . ①②所得溶液是该温度下的不饱和溶液 B . ③④所得溶液溶质的质量分数相等 C . 20℃时,氯化钠的溶解度为36g D . 20℃时,将④恒温蒸发25g水,过滤得18g固体
现有一瓶久置的过氧化氢溶液(标签如图所示)。已知过氧化氢溶液在存放过程中会缓慢分解。取该溶液 34g 于烧杯中,加入一定量的二氧化锰,完全反应后,称得烧杯内剩余物质的总质量是 33.8g,将杯内剩余物质过滤、洗涤、干燥后得滤渣 3g.请计算:

-
(1) 完全反应后生成氧气的质量。
-
(2) 求该瓶溶液中溶质的质量分数。
-
(3) 用该瓶溶液配制 100g 溶质质量分数为 3%的过氧化氢溶液需要加入水的质量。
在温度不变的条件下,下列欲使溶质的质量分数变为原来2倍的方法,最可行的是( )
A . 将20g硝酸钾饱和溶液蒸发掉10g水
B . 将20g硝酸钾不饱和溶液蒸发掉10g水
C . 在10g10%的硝酸钾溶液中,加入5g40%的硝酸钾溶液
D . 将10g硝酸钾不饱和溶液中加入10g硝酸钾固体
有40g5%的硝酸钾溶液,若将其质量分数增大到10%,应采用的方法是 ( )
A . 把溶剂蒸发掉一半
B . 加入40g溶质质量分数为15%的硝酸钾溶液
C . 把溶液倒掉20g
D . 加入2g硝酸钾固体
200g15%的食盐溶液欲使其质量分数变为30%,若蒸发溶剂水,需要蒸发多少克水?若需要加入溶质食盐,需要加入多少克食盐?(写出计算步骤,如果结果出现小数,保留小数点后一位)
现量取100mL溶质质量分数为90%的浓硫酸(密度为1.80g/mL),
-
(1) 100mL浓硫酸中含有溶质多少克?(写出必须的解题步骤)
-
(2) 若需要配制成20%的稀硫酸,还需要量取多少毫升的水?(写出必须的解题步骤)
化学兴趣小组测定某铁铜合金粉末中铜的质量分数,步骤如下:
-
(1) (配置稀盐酸)实验室现有溶质质量分数为36.5%的浓盐酸100g,稀释成溶质质量分数为7.3%的稀盐酸用于实验,需要加入水的体积为mL(ρ水=1.0g/mL)。若配置上述溶液,实际操作的实验步骤顺序是(填序号)。
①计算 ②混匀 ③量取 ④称量 ⑤溶解
-
(2) (测量实验)将一定质量稀盐酸加入装有铁铜合金粉末的试管中,观察到的现象是。
-
(3) (实验数据与计算)化学兴趣小组利用(1)中配置的稀盐酸进行了三次实验,实验数据如下表:
组别
一
二
三
稀盐酸质量/g
150
100
100
铁铜合金质量(粉)/g
20
20
25
烧杯中剩余物质量/g
169.8
119.8
124.8
求铁铜合金中铜的质量分数。(写出计算过程)
-
(4) (计算数据分析与反思)
若用生成的氢气质量求铁铜合金中铜的质量分数,可选择的实验组为第组数据。
实验室用质量分数为20.0%的稀硫酸处理含Ba(OH)2的废液。向100.0g废液中加入稀硫酸至溶液恰好呈中性,最终得到2.33 g沉淀。请计算:
-
(1) 配制490.0 g 20.0%的稀硫酸需质量分数为98.0%的浓硫酸g。
-
(2) 废液中Ba(OH)2的质量分数。
最近更新



