复分解反应及其应用 知识点
酸、碱、盐间的反应都属于复分解反应
复分解反应及其应用 知识点题库
 钠的氧化物
钠的氧化物  氢氧化钠溶液
氢氧化钠溶液 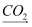 白色固体
白色固体【提出问题】常温下钠与氧气反应,产物有哪些?
【查阅资料】钠的氧化物,除氧化钠(Na2O)外还有过氧化钠(Na2O2),氧化钠与过氧化钠都能与水发生反应,方程式如下:Na2O+H2O═2NaOH;2Na2O2+2H2O═4NaOH+O2↑
-
(1) 【作出猜想】常温下钠与氧气反应的产物.
猜想1:Na2O,
猜想2:Na2CO3 ,
猜想3:①
-
(2) 【实验探究一】
实验操作
实验现象
实验结论
取少量钠的氧化物加入足量蒸馏水
②
猜想1正确
-
(3) 【继续探究】钠在空气中放置一段时间得到白色固体的成分
【作出猜想】
猜想一:Na2CO3
猜想二:Na2CO3和NaOH
【实验探究二】
实验操作
实验现象
实验结论
1.取少量白色固体加入足量
③
产生白色沉淀
白色固体成分为Na2CO3
和NaOH
2.过滤、取少量滤液加入④
⑤
-
(4) 【实验反思】
①类比氧化铜与盐酸的反应,写出氧化钠与盐酸反应的化学方程式.
②过氧化钠也能与盐酸反应,方程式为:2Na2O2+4HCl=4NaCl+2H2O+X,X的化学式为
③能与酸反应只生成盐和水的氧化物称为碱性氧化物,请判断Na2O2碱性氧化物(填“是”或“不是”).

-
(1) 反渗透膜法与滤纸过滤法在原理上都是利用混合体系中各物质的不同进行分离的方法.
-
(2) 过程③是氨碱法制纯碱的一个流程,需要向饱和食盐水中先后加入的两种物质是(写化学式).
-
(3) 过程④采用蒸发结晶的方法,而不采用冷却热饱和溶液方法,原因是.
-
(4) 如果要充分利用海边贝壳资源,过程⑤生成氢氧化镁的化学方程式是.
-
(5) 浓海水中Mg2+、SO42﹣、Ca2+ , 可用离子交换膜直接除去,若用化学沉淀法依次除去Mg2+、SO42﹣、Ca2+ , 需要的三种离子分别是(写离子符号).
-
(6) 离子交换膜是对特定离子的选择性透过膜,可以使带特定电量的离子透过.过程②中“某种离子交换膜”选择透过的离子特点是
【查阅资料】BaSO4是白色固体,难溶于水,也不与盐酸反应.
【实验一】同学们取4支试管,分别加入一定量4种溶液于试管中,再分别滴加少量的稀硫酸.
实验装置 | 实验现象 |
| 1号试管中无明显现象 |
2号试管中无明显现象 | |
3号试管中 。 | |
4号试管中有白色沉淀产生 |
-
(1) 3号试管中的实验现象是.
-
(2) 4号试管中发生复分解反应的化学方程式为.
-
(3) 【提出问题】3号、4号试管中的现象能证明硫酸与Na2CO3、BaCl2发生了复分解反应.
1号、2号试管中均没有观察到明显现象,如何证明硫酸与NaOH、NaCl是否发生了复分解反应?
【实验二】同学们又进行了以下实验.
实验装置
实验现象

5号试管中,滴加酚酞溶液后,溶液由无色变为红色;滴加一定量稀硫酸后,溶液由红色变为无色
6号试管中始终无明显现象
5号试管中的现象能证明NaOH与稀硫酸发生了复分解反应.图1为反应的微观示意图,从微观粒子变化的角度分析,该反应的实质是.
-
(4) 【反思与评价】
同学们发现3号、4号试管中的微粒数也有变化:4号试管中的Ba2+、SO42﹣因生成沉淀而减少,3号试管中减少的微粒是.
-
(5) 欲进一步探究2号试管中的两种物质是否发生了复分解反应,又补充了以下如图2实验.
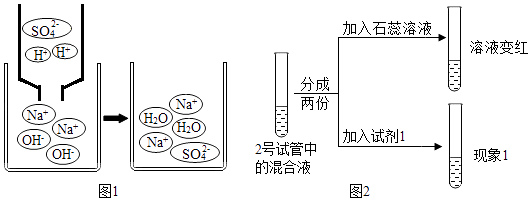
该实验证明两种物质不能发生复分解反应.请结合实验中的信息,回答下列问题:
①滴加石蕊溶液的目的是.
②试剂1和现象1分别是.
-
(6) 根据此次探究活动,你认为下列说法正确的是 (填序号).A . 酸、碱、盐之间并不是都能发生复分解反应 B . 从微观上看,复分解反应的实质是溶液中某些离子相互结合使离子数目减少 C . 判断化学反应发生,可依据有新物质生成,也可依据某一反应物消失 D . 证明复分解反应没有发生,可验证某一反应物依然存在.
①NaOH溶液、MgCl2溶液、硝酸 ②BaCl2溶液、NaNO3溶液、稀硫酸
③CuCl2溶液、FeCl2溶液、锌粒 ④NaCl溶液、AgNO3溶液、盐酸
⑤Fe2(SO4)3溶液、NaNO3溶液、Ba(OH)2溶液

-
(1) 反应①的化学方程式是 ,该反应过程中(填“吸收”或“放出”)大量热。
-
(2) 反应②所属基本反应类型是 反应。
(提出问题)白色固体中含有哪些物质?(若涉及到微溶物质按可溶处理)
(初步探究)
-
(1) 取样,加水溶解,得到无色溶液,由此可知:固体中一定不含。
-
(2) 同学们继续实验,如图所示:取少量无色溶液于试管中,滴加酚酞溶液,溶液变红,再通入二氧化碳气体,发现溶液中产生白色沉淀,溶液变为无色。
(猜想与假设)同学们做出合理猜想,白色固体可能是:
猜想一:氢氧化钙
猜想二:氢氧化钙、硝酸钡
猜想三:
-
(3) (继续探究)
为了进一步确定白色固体成分,取少量原无色溶液于试管中,加入①,无明显实验现象,证明一定没有。最终确定白色体的成分是③(填化学式)。
-
(4) (反思与收获)
通过上述探究活动同学们获得的启示是:探究固体或溶质成分时主要是依据各物质的不同,设计实验,选取合适的药品,通过实验现象来加以判断的。

某同学取200g酸性硫酸铜溶液,用滴管向该溶液中逐滴滴入氢氧化钠溶液,并绘出加入氢氧化钠溶液质量与产生沉淀质量的关系图。认真阅读后用规范的解题过程,计算出所用氢氧化钠溶液的溶质质量分数。
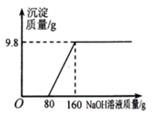

-
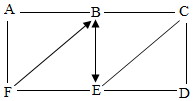
(1) B和C反应的化学方程式是。基本反应类型是。
-
(2) D生成A的化学方程式是(写一个)。
-
(3) 若F与其他物质类别不同,E和F反应的微观实质是。
 ),下列分析正确的是( )
),下列分析正确的是( )
 R+CO2
C . R(OH)2+2HCl=RCl2+2H2O
D . R(OH)2
R+CO2
C . R(OH)2+2HCl=RCl2+2H2O
D . R(OH)2  RO+H2O
RO+H2O


-
(1) E的化学式为;其用途是(任写一种)。
-
(2) B转化为D的化学方程式。其基本反应类型是。B与I反应的化学方程式。A转化为B的实验现象是。

-
(1) 在干冰、金刚石、氯化钠三种物质中,由离子构成的是。
-
(2) 图1描述了稀盐酸与硝酸银溶液反应的微观实质,C处应填入的符号为。
-
(3) 在稀盐酸中加入适量镁条的实验中:
①宏观表征:可以观察到的主要现象为,固体逐渐溶解;
②微观表征:如图2表示反应前后溶液中的主要离子,写出
 所表示的微粒符号;
所表示的微粒符号;③符号表征:写出化学方程式。
-
(4) 以化合价为纵坐标,以物质的类别为横坐标所绘制的图象叫价类图。如图3为铁的价类图,请分析该图后填写:某化合物化学式为(NH4)2Fe(SO4)2 , 它代表的点是(填“A,B,C,D,E”)。
-
(1) 分别写出A、C、D、E四种物质的化学式。ACDE
-
(2) 写出B转化成E的化学方程式:。
-
(3) 足量的E与D的粉末发生反应的现象是。




