纯碱的制取 知识点题库
氨碱法生产纯碱的主要反应原理如下:
①NaCl+NH3+CO2+H2O═NaHCO3+NH4Cl
②2NaHCO3![]() Na2CO3+CO2↑+H2O.对上述信息的有关理解错误的是( )
Na2CO3+CO2↑+H2O.对上述信息的有关理解错误的是( )
(1)NaCl+NH3+CO2+H2O=NaHCO3+NH4Cl
(2)2NaHCO3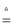 Na2CO3+CO2+H2O
Na2CO3+CO2+H2O
对上述信息的有关理解不正确的是( )
-
(1) 加入稀盐酸发生反应的化学方程式为;
-
(2) 求解样品中碳酸钠质量(x)的比例式为;
-
(3) 样品中碳酸钠的纯度为;
-
(4) 若向反应后的溶液中加入54.5g水,则所得溶液中溶质和溶剂的质量最简比为;
-
(5) 工业上常用碳酸钠和氢氧化钙反应来制取氢氧化钠.若要用这种方法制得20t含氢氧化钠80%的工业烧碱,需要上述用侯氏制碱法获得的工业纯碱产品的质量是.

-
(1) 设备1中分离操作的名称是.
-
(2) 煅烧炉中发生的化学反应,属于基本反应类型中的反应.
-
(3) 以上流程中,可循环使用的物质有.

-
(1) 上述流程中,用到的原料有空气、焦炭、水、、饱和的氯钠溶等.
-
(2) 上述流程中,已知步骤②发生的是化合反应,步骤⑤发生的是分解反应,则⑤的反应条件是.
-
(3) 上述流程中,可循环利用的物质是二氧化碳和.
-
(4) 上述流程中,“一种氮肥”中阴离子的符号是.

-
(1) 操作a的名称是。
-
(2) 写出NH4Cl的一种用途。
-
(3) 反应①的微观示意图如下,请在方框中补全相应微粒的图示。

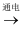 2NaOH+H2↑+Cl2↑,某化学兴趣小组为了探究久置的工业烧碱的成分,进行了如下实验:
2NaOH+H2↑+Cl2↑,某化学兴趣小组为了探究久置的工业烧碱的成分,进行了如下实验:
-
(1) ①取少量样品于烧杯中,加入过量稀盐酸,观察到有气泡产生,说明样品中含有。
②继续向烧杯中加入硝酸银溶液,出现白色沉淀,甲同学得出结论:样品中还含有氯化钠,乙同学对该结论提出了质疑,认为不一定含有氯化钠,其理由是;丙同学提出只需将试剂换成就可以确定氯化钠是否存在。
③丁同学认为还需要确认样品中是否含有氢氧化钠,于是大家取少量样品配成溶液后进行以下实验:
实验操作
现象
结论
样品中有氢氧化钠
通过实验,兴趣小组同学得出结论:该工业烧碱中含有Na2CO3、NaCl和NaOH。
-
(2) 同学们还想测定该烧碱中碳酸钠的质量分数。他们取10克烧碱样品配成溶液,向其中逐滴加入BaCl2溶液,产生沉淀的量与所加BaCl2的量关系如图所示。(NaOH和BaCl2不反应)

求样品中Na2CO3的质量分数。( 写出计算过程)
-
(3) B点处所得溶液中溶质有。

-
(1) A物质的化学式是,B物质的俗称是,C物质的名称是。
-
(2) 向A的块状固体上滴加水,观察到大量的水蒸气产生,该现象说明。
-
(3) 举出B物质在农业生产中的一种用途:。
-
(4) 反应②的化学方程式为,该反应可以用来检验二氧化碳气体,实验现象是。
-
(5) 反应③的基本反应类型是,该反应前后碳元素的化合价(填“改变”或“不改变”)。
-
(1) 某化学兴趣小组将碳酸钠溶液加入到盛有氢氧化钙溶液的小烧杯中,该反应的化学方程式是。充分反应后过滤,得到滤渣和滤液。
-
(2) 【提出问题】滤液中溶质的成分是什么?
【做出猜想】猜想一:NaOH 猜想二:NaOH和Ca(OH) 2
猜想三:NaOH和 猜想四:NaOH、Na2CO3和Ca(OH) 2
经过讨论,大家认为猜想四不合理,原因是;
-
(3) 【实验探究】
实验步骤
现象
结论
实验Ⅰ:取滤液,向其中滴入适量Na2CO3溶液
猜想二不成立
实验Ⅱ:另取滤液,向其中加入足量
产生气泡
猜想成立
-
(4) 【反思与拓展】利用上述滤液获得氢氧化钠溶液,可向滤液中加入适量的溶液。

-
(1) 反应①的化学方程式,反应②的基本反应类型为。
-
(2) 纯碱的化学式为,所属物质的类别是。纯碱溶液能使酚酞显色。
-
(3) 工业上用分离液态空气 的方法制取氮气,属于变化(填“物理”或“化学”)。
-
(4) 操作a的名称是,实验室进行此操作所需的玻璃仪器有烧杯、玻璃棒、。
-
(5) 写出NH4Cl的一种用途。
|
温度/℃ |
10 |
20 |
30 |
40 |
|
|
溶解度/g |
Na2CO3 |
12.2 |
21.8 |
39.7 |
48.8 |
|
NaCl |
35.8 |
36.0 |
36.3 |
36.6 |
|
|
NaHCO3 |
8.2 |
9.6 |
11.1 |
12.7 |
|
-
(1) 10℃ ~40℃,溶解度随温度变化最小的物质为(填名称)。
-
(2) 将等质量的三种表中物质的饱和溶液从40℃降温至20℃,所得溶液中溶质的质量分数由大到小的顺序是(用化学式表示)。
-
(3) 制碱原理:向饱和NaCl溶液中通入足量NH3和CO2生成NaHCO3固体和NH4Cl,NaHCO3加热分解制得纯碱。
I.生成NaHCO3的化学方程式为。
II.结合上表,NaHCO3固体结晶析出的原因可能有(填字母序号)。
A.同温下NaHCO3溶解度小于NaCl
B.溶剂质量减少
C.生成的NaHCO3质量大于消耗的NaCl质量

-
(1) 粗盐中含有不溶性的泥沙和可溶性的Ca2+、Mg2+、
 ,为了除去以上杂质,可将粗盐溶于水,然后进行下列五项操作:①过滤;②加入过量的Na2CO3溶液;③加入适量盐酸;④加入过量的BaCl2溶液;⑤加入过量的NaOH溶液。请写出一种正确的操作顺序(填序号)。
,为了除去以上杂质,可将粗盐溶于水,然后进行下列五项操作:①过滤;②加入过量的Na2CO3溶液;③加入适量盐酸;④加入过量的BaCl2溶液;⑤加入过量的NaOH溶液。请写出一种正确的操作顺序(填序号)。
-
(2) 沉淀池中进行的反应是:CO2+NH3+H2O+NaCl=↓+NH4Cl。
-
(3) 煅烧炉中发生的反应化学方程式是。
-
(4) 以下说法正确的是。
A 沉淀池中通入氨气的目的是使溶液呈碱性,更利于二氧化碳的吸收;
B 得到的母液中至少含有两种溶质,且为碳酸氢钠的饱和溶液;
C 可循环利用的X物质为二氧化碳,Y物质中只有氯化钠;
D 操作1的名称为过滤。

已知:常温下,氨气的溶解度很大,CO2的溶解度很小。回答下列问题:
-
(1) 纯碱的化学式为。
-
(2) “侯氏制碱法”的反应温度一般控制为30-35℃,因为在此温度时, NaHCO3的溶解度较(填“大”或“小”)。
-
(3) 若向饱和食盐水中先通入CO2 , 会导致 NaHCO3产量减少,原因是。
-
(4) 写出步骤①、②发生的总反应方程式。
-
(5) “侯氏制碱法”中能循环利用的物质有NaCl、H2O和。
①
②
③
有关这三个化学反应的说法不正确的是( )
-
(1) 2021年10月16日中国神舟十三号载人飞船发射取得圆满成功,举国欢庆。航空航天技术已经成为一个国家科技、工业和国防实力的重要体现。航天工程中需要大量的金属材料,如铝合金、钛合金等。

①铝具有很好的抗腐蚀性的原因是(用化学方程式表示)。
②如图是钛(Ti)原子结构示意图,图中x=;其在化学反应中,易失去电子形成离子,其离子符号为。
③卫星上的太阳能电池是将能转化为电能的装置。
④火箭的姿控系统使用耐辐照石英玻璃作为光学材料,其主要成分为二氧化硅,其中硅元素的化合价为。
⑤国际空间站有的用固体燃料氧气发生器制取氧气,很多宇航员将其亲切地称为“氧气蜡烛”,原理是点燃氯酸钠(NaClO3)和铁的固体粉末,产物中还有氧化亚铁和一种常见可做调味品的盐。写出该反应的化学方程式。
-
(2) 1926年我国著名化学家侯德榜先生创立了侯氏制碱法,促进了世界制碱技术的发展。
①“侯氏制碱法“过程中,向饱和的氯化钠溶液中先后通入的两种气体是(填化学式),生成物中先结晶析出(填化学式)。
②Na2CO3和NaCl两种物质的溶解度曲线如图所示。若把t1℃时Na2CO3和NaCl的饱和溶液,均升温到t2℃,则t2℃时Na2CO3溶液的溶质质量分数NaCl溶液的溶质质量分数(填“大于”、“小于”、“等于之一)。
③t2℃时,NaCl的饱和溶液溶质质量分数36%(填写“大于”、“等于”、“小于”之一)
④t2℃时,向50g水中加入40gNa2CO3固体,经充分搅拌后,所得溶液的质量为g。

【查阅资料】
过碳酸钠俗称固体双氧水,外观为白色结晶或结晶性粉末,易溶于水,水溶液中含有Na2CO3和H2O2。
I.探究“茶垢清洁剂”遇热水产生气体的成分
【进行实验】
向盛有适量“茶垢清洁剂”的大试管中加入足量热水,观察到有大量无色气泡产生。
-
(1) 【解释与结论】
证明产生气体是氧气的实验方法为。
-
(2) H2O2反应生成氧气的化学方程式为。
-
(3) Ⅱ.探究制备过碳酸钠的最佳条件
【进行实验】取6.0g35%H2O2溶液加入烧杯中,加入稳定剂15mL;边搅拌,边加入3.5gN2CO3固体,搅拌下使过碳酸钠完全析出,分析产品质量。分别在不同温度下进行4次实验,结果见下表。
序号
t/℃
活性氧百分含量/%
产率/%
①
5~10
13.94
85.49
②
10~15
14.02
85.78
③
15~20
15.05
88.38
④
20~25
14.46
83.01
【解释与结论】
以上实验的目的是。
-
(4) 比较实验③和④发现温度越高而过碳酸钠的产率越低,其原因可能是。
-
(5) 【反思与评价】
欲进一步证明过碳酸钠溶液中含有碳酸盐,所需试剂是。
-
(6) 若要继续探究制作过碳酸钠的最佳原料比(35%H2O2溶液与Na2CO3的质量比),除应用相同的实验仪器和操作步骤外,还需其他相同的条件是。
 Na2CO3 + CO2↑ + H2O。下列说法错误的是( )
Na2CO3 + CO2↑ + H2O。下列说法错误的是( )



