质量守恒定律及其应用 知识点
微观解释:反应前后原子种类和个数不变,原子质量不变;
应用:(1)利用质量守恒定律确定方程式中未知物质化学式;
(2)利用反应前后各物质质量关系确定各物质的质量;
(3)利用质量守恒定律确定密闭容器中各物质的反应情况及质量关系。
质量守恒定律及其应用 知识点题库
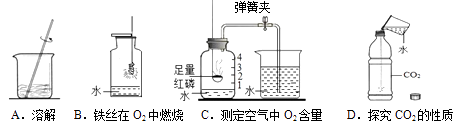
①水加热沸腾一段时间后质量减少,符合质量守恒定律
②铁在氧气中燃烧后,生成物的质量大于铁质量,符合质量守恒定律
③高锰酸钾加热分解后,剩余固体质量比高锰酸钾减少了,符合质量守恒定律
④3g硫在5g氧气中充分燃烧,生成了8g二氧化硫,符合质量守恒定律.

①电解水可证明水由氢、氧两种元素组成,该反应的化学方程式为。
②高铁酸钾(化学式K2FeO4)目前被广泛应用于自来水净化处理领域。高铁酸钾中铁元素的化合价为,该物质中铁元素处于(填“游离态”或“化合态”)。
③水是重要的溶剂。配制6%的氯化钠溶液50g,需要用到的仪器是。
A.酒精灯 B.玻璃棒 C.烧杯 D.量筒
④水在化学实验中的作用不可忽视。下列实验中水起吸收热量作用的是。
⑤“84消毒液”主要成分是次氯酸钠(NaClO),制取的化学方程式为:
2NaOH + X → NaClO +NaCl+H2O,则X的化学式。 次氯酸钠(NaClO)的摩尔质量为, 1.5mol NaClO中约含氯原子个,
其中氧元素的质量是g。

A.该反应中丙与丁的分子个数比为4:1 B.该反应属于化合反应
C.该反应前后原子的数目发生改变 D.
物质 | X | Y | Z | W |
反应前的质量 | 10 | 5 | 2 | 30 |
反应后的质量 | m | 39 | 2 | 2 |
| 物 质 | 氧 气 | 二氧化碳 | 水蒸气 | W |
| 反应前质量/g | 50 | 1 | 1 | 23 |
| 反应后质量/g | 2 | 45 | 28 | x |
| 物质 | 甲 | 乙 | 丙 | 丁 |
| 反应前的质量/g | 30 | 55 | 20 | 70 |
| 反应后的质量/g | 0 | 100 | X | 5 |
根据质量守恒定律判断,X的值为( )
| 物质 | 甲 | 乙 | 丙 | 丁 |
| 反应前质量/g | 1 | 20 | 15 | 2 |
| 反应后质量/g | m | 29 | 0 | 8 |
| 物质 | X | Y | Z | W |
| 反应前的质量(g) | 2 | 1 | 16 | 16 |
| 反应后的质量(g) | 12 | m | 8 | 14 |
-
(1) 分类角度:CO2属于(填字母)。
a.单质
b.氧化物
c.有机物
-
(2) 微观角度:我国研制的一种新型催化剂可将CO2和H2转化为甲醇(CH5OH)和X,若用“
 ”表示氢原子;“
”表示氢原子;“  ”表示氧原子,“
”表示氧原子,“  ”表示碳原子,该反应的微观示意图如下:
”表示碳原子,该反应的微观示意图如下: 
画出X分子的微观示意图:。
-
(3) 性质角度: 三百多年前,人们发现一些洞穴内有一种能使燃烧的木柴熄灭的气体,后来该气体被证实是CO2。据此推测CO2具有的化学性质是。
-
(1) 请写出镁条与氧气反应的化学方程式:;
-
(2) 小明发现燃烧产物的质量大于反应物镁条的质量,认为这个反应不遵守质量守恒定律。我(填“同意”或“不同意”)小明的观点,因为。
-
(3) 小红按如图装置改进实验,验证了质量守恒定律,却发现产物中还有少量黄色固体。

[提出问题]黄色固体是什么?
[查阅资料]
①氧化镁为白色固体;
②镁能与氮气反应生成黄色的氮化镁(Mg3N2)固体;
③氮化镁可与水剧烈反应产生氨气,该气体能使湿润的红色石蕊试纸变蓝。
[作出猜想]黄色固体为Mg3N2。
[实验探究]请设计实验,验证猜想。
实验操作
实验现象
实验结论
取少量于试管中,加入少量,将湿润的红色石蕊试纸放在试管口
黄色固体为氮化镁
-
(4) [反思交流]
①若用镁条代替红磷完成测定空气中氧气含量的实验,不考虑其他因素的影响,进入水的体积会(填“大于”、“小于”或“等于”)瓶内空气总体积的
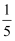 。
。②空气中的氮气的含量远大于氧气的含量,可是镁条在空气中燃烧的产物氧化镁却远多于氮化镁,合理的解释是。
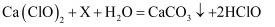 。下列说法正确的是( )
。下列说法正确的是( )
-
(1) 求生成二氧化碳的质量?
-
(2) 石灰石的样品中CaCO3的质量分数?
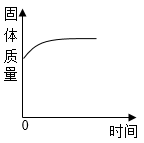 在空气中加热铜粉
B .
在空气中加热铜粉
B . 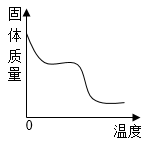 氧化汞受热分解
C .
氧化汞受热分解
C .  石灰石与盐酸反应
D .
石灰石与盐酸反应
D . 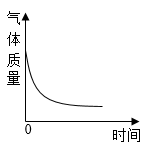 锌与稀硫酸反应
锌与稀硫酸反应



