蒸馏与分馏 知识点题库
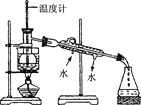
① ;
② ;
③ .
-
(1) 植物芳香油的提取方法有 、压榨和 等.具体采用哪种方法要根据植物原料的特点来决定.
-
(2) 玫瑰精油适合用 提取,其理由是玫瑰精油具有易挥发、难溶于水、化学性质稳定的特点.蒸馏时收集的蒸馏液不是纯的玫瑰精油,而是 .经冷凝管冷却后,混合物又会重新分出 层和水层.如果蒸馏过程中不进行冷却,则精油提取量会减少,原因是
-
(3) 橘皮精油的提取原料是橘皮,但橘皮易焦糊,宜采用 法提取橘皮精油,其中将柑橘皮干燥去水,并用石灰水浸泡,其目的是

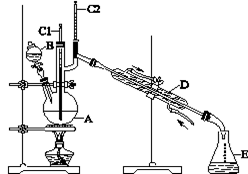
CH3CH2CH2CH2OH 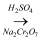 CH3CH2CH2CHO ,反应物和产物的相关数据列表如下:
CH3CH2CH2CHO ,反应物和产物的相关数据列表如下:
| 沸点/℃ | 密度/(g·cm-3) | 水中溶解性 | |
| 正丁醇 | 117.2 | 0.810 9 | 微溶 |
| 正丁醛 | 75.7 | 0.801 7 | 微溶 |
实验步骤如下:将6.0 g Na2Cr2O7放入100 mL烧杯中,加30 mL水溶解,与5 mL浓硫酸形成混合溶液,将所得溶液小心转移至B中。在A中加入4.0 g正丁醇和几粒沸石,加热。当有蒸气出现时,开始滴加B中溶液。滴加过程中保持反应温度为90~95 ℃,在E中收集90 ℃以下的馏分。将馏出物倒入分液漏斗中,分去水层,有机层干燥后蒸馏,收集75~77 ℃馏分,产量2.0 g。
回答下列问题:
-
(1) 实验中,Na2Cr2O7溶液和浓硫酸添加的顺序为。
-
(2) 加入沸石的作用是。
若加热后发现未加沸石,应采取的正确方法是。
-
(3) 上述装置图中,D仪器的名称是,E仪器的名称是。
-
(4) 分液漏斗使用前必须进行的操作是。
-
(5) 将正丁醛粗产品置于分液漏斗中分水时,正丁醛在层(填“上”或“下”)。
-
(6) 反应温度应保持在90~95 ℃,其原因是
-
(7) 本实验中,正丁醛的产率为%(结果保留两位小数)。
 B . 制少量蒸馏水
B . 制少量蒸馏水  C . 收集NO2气体
C . 收集NO2气体 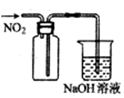 D . 配制一定浓度的溶液
D . 配制一定浓度的溶液 

已知:乙醚[(C2H5)2O]沸点34.5℃,易挥发、易燃、低毒,挥发后点燃易发生爆炸,微溶于水,密度比水小。含Fe3+的HCl溶液,在HCl浓度较高时,用3倍体积的含HCl的乙醚溶液萃取,可形成易溶于乙醚的缔合物[(C2H5)2O·H]+·[FeCl4]-;降低HCl浓度,该缔合物解离。请回答:
-
(1) 经操作A可得溶液Ⅰ、Ⅱ,具体操作为:静置后,。
-
(2) 适量加入的试剂甲,最好是难溶性还原剂,原因是。
-
(3) 蒸馏装置如图所示,装置中存在的不正确是、。
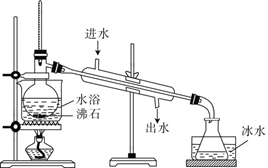
-
(4) 下列有关说法错误的是。
A 滴定管在使用前需用待装液润洗,锥形瓶则不用润洗
B 判断经操作A后,Fe3+是否有残留,可以使用KSCN溶液检测
C 开始滴定前,滴定管尖嘴处悬有标准液液滴,滴定终点时尖嘴处无悬液,则测得的Fe3+浓度偏高
D 溶液由黄色变为浅紫色时,滴定到达终点
-
(5) 先除去溶液中溶解的HCl,再用0.0500mol·L-1 KMnO4溶液进行滴定,实验三次,达到终点时平均消耗KMnO4溶液12.00 mL。根据该实验数据,试样X中c(Fe3+)为。
⑴从煤焦油中提取二甲苯
⑵从海水中提取粗盐
⑶十六烷转变为辛烷和辛烯
⑷轻柴油转变为乙烯、丙烯等不饱和烃
⑸煤转化为焦炭、煤焦油等
⑹工业上由氧化铝制取金属铝
⑺从铁矿石中提取金属铁,铁矿石被
⑻提纯氢氧化铁胶体(除去其中的杂质离子)
a.过滤 b.裂解 c.分馏 d.裂化 e.干馏 f.还原 g.电解 h.溶解 i.渗析 j.蒸发 k.氧化
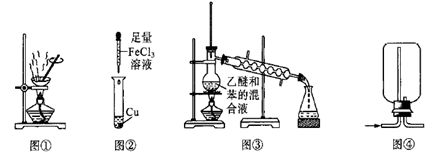

已知:
Ⅰ.FeCl2、FeCl3不溶于氯苯、二氯苯;
Ⅱ.C6H5Cl、C6H4Cl2二者互溶,不溶于水;沸点分别为132℃、173℃。
回答下列问题:。
-
(1) 仪器a的名称为,该仪器(填“能”或“不能”)用于石油的分馏。
-
(2) 该团队用3.25g FeCl3与过量氯苯反应,实验结束后将三颈烧瓶中的物质倒出,过滤、洗涤、干燥后得到粗产品,回收滤液中氯苯的方法为(填操作名称)。
-
(3) 经讨论后,分为甲、乙两组用不同方法测定FeCl3的转化率。
①甲组:用0.40mol·L-1NaOH标准液滴定锥形瓶内的溶液,可选用的指示剂为;若终点时消耗18.50mL NaOH标准液,则FeCl3转化率为%。
②乙组:将粗产品制成250mL溶液,取出25.00mL,用0.0200mol·L-1标准KMnO4溶液滴定(已知:本实验条件下,Cl-不参与反应:KMnO4还原产物为Mn2+)。达到滴定终点时的现象为,经平行实验测得平均消耗标准液16.00mL,则甲组测定结果(填“高于”或“低于”)乙组测定结果。
③某检测机构对粗产品进行测定,经数据分析测得FeCl3的转化率为79.95%。与乙组和检测机构的测定结果对比,若无操作失误,甲组产生较大误差可能的原因为。
 ,
,  与
与  互为同位素
C . “凡酸坏之酒,皆可蒸烧”中涉及蒸馏操作
D . 古代的鎏金工艺利用了电解原理
互为同位素
C . “凡酸坏之酒,皆可蒸烧”中涉及蒸馏操作
D . 古代的鎏金工艺利用了电解原理
 CH3CH2CH2CHO。反应物和产物的相关数据列表:
CH3CH2CH2CHO。反应物和产物的相关数据列表:沸点/℃ | 密度(g/cm3) | 水中溶解性 | 摩尔质量(g/mol) | |
正丁醇 | 117.2 | 0.8109 | 微溶 | 74 |
正丁醛 | 75.7 | 0.8017 | 微溶 | 72 |
实验步骤:将6.0 gNa2Cr2O7放入100 mL烧杯中,加30 mL水溶解,再缓慢加入5 mL浓硫酸,将所得溶液小心转移至B中,在A中加入3.7 g正丁醇和几粒沸石、加热,当有蒸汽出现时,开始滴加B中溶液。滴加过程中保持反应温度为90-95℃,在E中收集90℃以下的馏分。将馏出物倒入分液漏斗中,分去水层,有机层干燥后蒸馏,收集75-77℃的馏分,产量2.7 g。
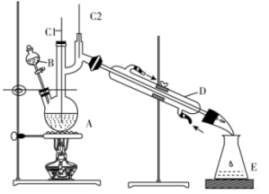
回答下列问题:
-
(1) 上述装置图中B仪器的名称是。
-
(2) 下列说法正确的是____。A . 该实验中,仪器A,B中的溶液可以互换 B . 实验中可以通过移动酒精灯的位来进行温度控制 C . 应先加热A至90-95℃,再通冷凝水 D . 收集75-77℃馏分,严格控温是为了提高产品的纯度
-
(3) 反应温度应保持在90-95℃,其原因是。
-
(4) 本实验中,正丁醛的产率为 %。
选项 | 物质 | 除杂试剂 | 方法 |
A | 酒精(水) | CaO | 蒸馏 |
B | 乙酸乙酯(乙酸) | NaOH溶液 | 分液 |
C | 甲烷(乙烯) | 酸性高锰酸钾溶液 | 洗气 |
D | 苯(溴) | KI溶液 | 分液 |



