氯离子的检验 知识点题库
-
(1) 上述十种物质中有两种物质在水溶液中可发生反应,离子方程式为:H++OH﹣=H2O,该反应的化学方程式为.
-
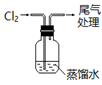
(2) 实验室制备试剂⑦的方法是:.
-
(3) 可用于治疗胃酸过多的试剂是(填序号)
-
(4) 若某溶液中同时存在Fe3+和Fe2+ , 则可用于验证其中含Fe2+的试剂是(填序号);若某溶液中存在Na+、K+、SO42﹣、Cl﹣四种离子,若检验Cl﹣的存在可选用的试剂是(填序号),具体操作方法是.
-
(5) 用98%的浓H2SO4(ρ=1.84g/cm3)配制500ml0.5mol/L的稀H2SO4 , 所需浓H2SO4的体积为 ml(小数点后保留一位有效数字)
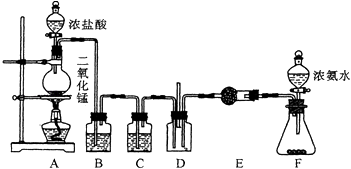
请回答下列问题:
-
(1) F中所装的固体试剂是
-
(2) 洗气瓶B的作用是.C、E都是干燥装置,其中E中干燥管内所装的试剂是
-
(3) 反应开始后装置D中出现浓厚的白烟并在容器内壁凝结,活动小组拟继续通过实验鉴定该固体的成分.请你协助他们完成该实验探究.
步骤①:取固体样品加少量水溶解,分装于两支试管中.向其中一支试管中加入浓NaOH溶液,加热,将湿润的红色石蕊试纸放在试管口附近,红色石蕊试纸变蓝,证明该固体中含有
步骤②:
-
(4) 从绿色化学的角度考虑该装置中有一明显不合理之处,请你提出改进的意见..
 、
、  、
、 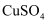 、
、 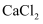 、
、  中的几种物质组成。某同学为了鉴别它们,做了如下实验:
中的几种物质组成。某同学为了鉴别它们,做了如下实验: ①将固体混合物溶于水,搅拌后得到无色透明溶液;
②在①所得的溶液中滴加 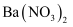 溶液,有白色沉淀生成,并继续滴加至沉淀完全;
溶液,有白色沉淀生成,并继续滴加至沉淀完全;
③过滤,然后向所得白色沉淀中加入过量稀硝酸,沉淀部分溶解。
根据该同学的实验结果回答下列问题:
-
(1) 原混合物中肯定有,肯定没有,可能含有。
-
(2) 写出上述实验过程中发生反应的离子方程式:。
-
(3) 要检验可能含有的物质可采用的方法是。
(资料)I2 遇到淀粉溶液变蓝,常用于检验碘的存在。
|
实验① |
实验② |
实验③ |
实验④ |
实验⑤ |
|
|
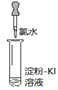
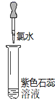
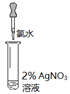
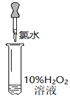
实验操作 (试管中溶液均为1 mL,均滴入5滴氯水) |
| | | | |
| 实验现象 | 蒸馏水由无色逐渐变为浅黄绿色 | 溶液变蓝 | 石蕊溶液先变红,后褪色 | 产生白色沉淀 | 产生大量无色气泡 |
-
(1) 实验②的现象可推断氧化性:Cl2I2(填“>”或“<”)。
-
(2) 证明氯水中含有Cl-的是实验(填序号),用离子方程式表示该实验中涉及的反应、。
-
(3) 实验③中溶液变红是由于溶液中含有(填微粒符号,下同);使溶液褪色的微粒是。
-
(4) 同学们根据“H2O2在催化剂作用下可发生分解”的性质,认为实验⑤中现象不能说明氧化性Cl2>H2O2。为证实Cl2将H2O2氧化,可继续补充实验:(填操作、现象)。
-
(5) 同学们发现久置的氯水会失去漂白性,溶液由黄绿色变为无色。为探究氯水失效的原因,进行实验:用强光照射盛有氯水的密闭广口瓶,并用传感器测定广口瓶中数据,得到如下曲线。
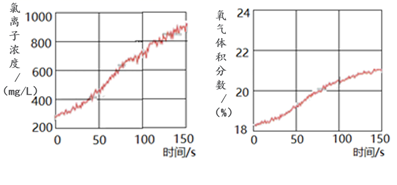
解释上两图中曲线变化的原因。若在上述整个实验过程中测定溶液的pH, pH的变化是。
①滴加Mg(NO3)2溶液;②过滤;③滴加AgNO3溶液;④滴加Ba(NO3)2溶液
| 选项 | 操作 | 现象 | 结论 |
| A | 将少量BaSO4固体用饱碳酸钠溶液浸泡,过滤后向滤渣中加入HCl | 滤渣溶解,并产生气泡 | Ksp(BaCO3)<Ksp(BaSO4) |
| B | 足量双氧水滴入酸性高锰酸钾溶液中 | 溶液褪色 | H2O2具有漂白性 |
| C | 向溶液X中通入氯化氢气体 | 生成白色沉淀 | 溶液X中一定含有Ag+ |
| D | 常温下,用pH计测定0.1mol•L-1NH4CN溶液的pH | pH=8.6 | 电离平衡常数:K(NH3•H2O)>K(HCN) |
| 序号 | 实验操作、现象 | 结论 |
| A | 向一种未知溶液中滴加AgNO3溶液,有白色沉淀 | 未知溶液中一定含有 |
| B | 向一种未知溶液中滴加盐酸,产生能使澄清石灰水变浑浊的无色无味的气体 | 未知溶液中一定含有 |
| C | 未知溶液进行焰色试验,焰色为黄色 | 该未知溶液中含钠元素 |
| D | 向紫色石蕊溶液中滴加氯水,溶液先变红后褪色 | Cl2具有酸性和漂白性 |
①氯气的性质很活泼,它与氢气混合后立即发生爆炸
②实验室制取氯气时,为了防止环境污染,多余的氯气可以用氢氧化钠溶液吸收
③久置的氯水漂白性增强
④检验HCl气体中是否混有Cl2的方法是将气体通入硝酸银溶液看是否有白色沉淀生成
⑤除去Cl2中的HCl,可使气体通过饱和食盐水
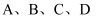 为四种可溶性盐,它们的阳离子分别是
为四种可溶性盐,它们的阳离子分别是 中的某一种,阴离子分别是
中的某一种,阴离子分别是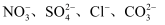 中的某一种。
中的某一种。
-
(1) 根据所学知识推断这四种盐的化学式分别为。
-
(2) 设计实验确定此猜想:
①将四种盐分别加入试管中,并加水溶解,可观察到溶液颜色的情况为。
②向①的四支试管中分别加入稀盐酸,可观察到的现象为。
-
(3) 检验上述四种溶液中的某一种中含有氯离子的方法为。
选项 | 实验目的 | 实验操作 |
A | 检验溶液中的 | 取样,向其中加入 |
B | 除去附着在试管内壁的硫 | 加水冲洗 |
C | 鉴别 | 取样,分别与熟石灰混合研磨,闻气味 |
D | 鉴别 | 取样,分别向其中滴加 |
实验目的 | 实验操作与现象 | |
A | 测定84消毒液的pH | 用洁净玻璃棒蘸取少量84消毒液滴在pH试纸上 |
B | 证明NaCl样品中含有钾盐 | 做焰色试验,通过蓝色钴玻璃观察到紫色火焰 |
C | 除去CO2 , 提纯CO | 将含有少量CO2的CO气体缓缓通过足量的过氧化钠粉末,淡黄色粉末变为白色 |
D | 验证某苏打样品中含有NaCl | 取少量样品于试管中,加水溶解,再加入足量稀盐酸,最后滴加AgNO3溶液,有白色沉淀生成 |
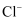


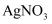 溶液
溶液 与
与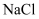 固体
固体 溶液与
溶液与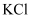 溶液
溶液 溶液
溶液


